
【题目】现有下列反应:
①2H2O+Cl2+SO2=H2SO4+2HCl
②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
针对上述两个反应回答:
(1)用单线桥标出①中电子转移的方向和数目_____;
(2)写出②的离子化学方程式____;
(3)Cl2、SO2和KMnO4的氧化性由强到弱的顺序为____;
(4)反应②中氯化氢表现出的性质是____。
a.还原性 b.酸性 c.氧化性
【答案】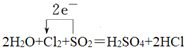 2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O KMnO4 >Cl2>SO2 ab
2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O KMnO4 >Cl2>SO2 ab
【解析】
(1)2H2O+Cl2+SO2=H2SO4+2HCl中Cl元素由0价降低为-1价,共得到2个电子,S元素由+4价升高为+6价,共失去2个电子,据此分析解答;
(2)2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O中KMnO4、HCl、KCl、MnCl2 可以拆成离子形式,据此书写离子方程式;
(3)氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,氧化剂的氧化性强于还原剂的氧化性,据此分析判断;
(4)在参加反应的盐酸中,有部分盐酸的化合价变化,部分不变,据此分析判断。
(1)2H2O+Cl2+SO2=H2SO4+2HCl中Cl元素由0价降低为-1价,共得到2个电子,S元素由+4价升高为+6价,共失去2个电子,电子转移的方向和数目用单线桥表示为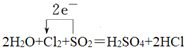 ,故答案为:
,故答案为: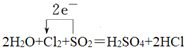 ;
;
(2)2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O 的离子方程式为2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O,故答案为:2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O;
(3)氧化还原反应中,氧化剂的氧化性强于还原剂的氧化性,根据反应①得氧化性是:Cl2>SO2;氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,根据反应②得出氧化性是:KMnO4>Cl2,所以氧化性:KMnO4>Cl2>SO2,故答案为:KMnO4>Cl2>SO2;
(4)反应②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O中氯化氢生成氯气表现还原性,生成氯化钾、氯化锰表现酸性,故答案为:ab。


科目:高中化学 来源: 题型:
【题目】(1)在质量分数为28%的KOH水溶液中,OH-与H2O数目之比是________。
(2)由硫酸钾、硫酸铁和硫酸组成的混合溶液,其中c(H+)=0.1 mol/L,c(Fe3+)=0.3 mol/L,c(SO42-)=0.6 mol/L,则c(K+)为________。
(3)相同物质的量浓度的氯化钠、氯化镁、氯化铝溶液,分别与硝酸银溶液反应,当生成沉淀的质量之比为3∶2∶1时,消耗三种盐溶液的体积比为________。
(4)A物质按下式分解:2A=B↑+ 2C↑ + 2D↑,测得生成的混合气体在相同条件下的密度是O2密度的m倍,则A的摩尔质量为______________。
(5)某状况下a L氨气(此时气体摩尔体积为Vm)溶解在一定量的水中形成b mL氨水溶液,所得溶液的密度为ρ g/mL,则该氨水的物质的量浓度可表示为________mol/L;氨水的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应①:Fe(s)+CO2(g)![]() FeO(s)+CO(g),其化学平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其化学平衡常数为K1;化学反应②:Fe(s)+H2O(g)![]() FeO(s)+H2(g),其化学平衡常数为K2,在温度973 K和1173 K的情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其化学平衡常数为K2,在温度973 K和1173 K的情况下,K1、K2的值分别如下:
温度 | K1 | K2 |
973 K | 1.47 | 2.38 |
1 173 K | 2.15 | 1.67 |
(1)通过表格中的数值可以推断:反应①是_______(填“吸热”或“放热”)反应。
(2)现有反应③:CO2(g)+H2(g)![]() CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=______。
CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=______。
(3)根据反应①与②可推导出K1、K2与K3之间的关系式为__________,据此关系式及上表数据,能推断出反应③是________(填“吸热”或“放热”)反应。
(4)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有______ 、_____ (填写字母序号)。
A.缩小反应容器的容积 B.扩大反应容器的容积
C.升高温度 D.使用合适的催化剂
E.设法减小平衡体系中的CO的浓度
(5)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:

①图甲中t2时刻发生改变的条件是__________。
②图乙中t2时刻发生改变的条件是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)等质量的CO和SO2分别装入同温同体积的容器,所含氧原子之比___,压强之比___。
(2)在标准状况下,由CO和CO2组成的混合气体8.96L,质量是16g。此混合物中CO和CO2的物质的量之比是___,混合气体的平均摩尔质量是___。
(3)将标准状况下aL的HCl(g)溶于1000g水,得到的盐酸的密度为bg/cm3,则该盐酸的物质的量浓度为___mol·L-1。
(4)1.204╳1023个NH4+的物质的量为__mol,质量为____g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置或操作正确的是( )
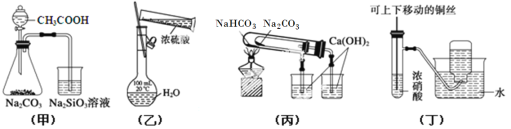
A. 用甲图装置验证CH3COOH、H2CO3和H2SiO3的酸性强弱
B. 用乙图装置配制一定浓度的稀硫酸
C. 用丙图装置验证NaHCO3和Na2CO3的热稳定性
D. 用丁图装置制备并收集少量NO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在相应的条件下可能大量共存的是( )
A. 能使pH试纸变红的溶液中:CO32-、K+、Cl-、Na+
B. 由水电离产生的c(OH-)=1×10-10mol·L-1的溶液中:NO3-、Mg2+、Na+、SO42-
C. 在![]() =1×10-12的溶液中:NH4+、Fe2+、Cl-、NO3-
=1×10-12的溶液中:NH4+、Fe2+、Cl-、NO3-
D. ![]() =10-10mol·L-1的溶液中:Na+、HCO3-、Cl-、K+
=10-10mol·L-1的溶液中:Na+、HCO3-、Cl-、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气通入NaOH溶液中会发生反应:Cl2+2NaOH=NaCl+NaClO+H2O,该反应的氧化产物是
A.Cl2B.NaOHC.NaClD.NaClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.油脂的皂化反应得到高级脂肪酸盐和甘油
B.纤维素和淀粉互为同分异构体
C.氨基酸之间能发生反应,合成更复杂的多肽,构成蛋白质
D.紫外线的杀菌作用主要原因是蛋白质的变性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com