
【题目】常温下,pH=l 的某溶液 A 中除H+外,还含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、 Cl-、I-、SO42-中的4种,且溶液中各离子的物质的量浓度均为0.1mol·L-1。现取该溶液进行有关实验,实验结果如下图所示,下列有关说法正确的是

A. 该溶液中一定有上述离子中的NO3-、Al3+、SO42-、Cl-四种离子
B. 实物消耗Cu14.4g,则生成气体丁的体积为3.36L
C. 该溶液一定没有Fe3+,但是无法确定是否含有I-
D. 沉淀乙一定有BaCO3,可能有BaSO4
【答案】A
【解析】pH=1的某溶液A中含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、Cl-、I-、SO42-中的4种,且溶液中各离子的物质的量浓度均为0.1mol/L。由于pH=1的某溶液中H+浓度为0.1mol/L,则说明溶液中无CO32-。向溶液中加入过量的(NH4)2CO3溶液,生成的无色气体甲为CO2,生成的白色沉淀甲是CO32-和溶液中的弱碱阳离子双水解生成的,由于生成的沉淀为白色,故此弱碱阳离子为Al3+,还能说明溶液中不含Fe3+、Fe2+;向溶液中加入过量的Ba(OH)2溶液,生成的气体乙为NH3,由于前面加入的过量的(NH4)2CO3溶液能引入NH4+,故不能确定原溶液中含NH4+。前面加入的过量的(NH4)2CO3溶液能引入CO32-,故生成的白色沉淀乙一定含BaCO3。向溶液乙中加铜和硫酸,有遇空气变红棕色的气体丙生成,说明溶液中含NO3-.由于溶液显酸性,即含硝酸,则I-不能有。综上分析可知,溶液中一定无CO32-、Fe3+、Fe2+、I-,一定含0.1mol/LH+、0.1mol/LAl3+、0、1mol/LNO3-,由于溶液必须显电中性,且除H+外只能含4种离子,故溶液中一定含Cl-、SO42-。即溶液中一定无NH4+、K+、Na+、CO32-、Fe3+、Fe2+、I-,一定含Cl-、SO42-、H+、Al3+、NO3-。A、该溶液中一定有上述离子中的NO3-、Al3+、SO42-、Cl-四种离子,故A正确;B、实验消耗Cu14.4g即0.225mol,设生成的气体丙NO的物质的量为xmol,根据得失电子数守恒可知:0.225mol×2=xmol×3,解得x=0.15mol,则0.15molNO与氧气反应后生成的气体丁NO2也为0.15mol,但由于状态不明确,故NO2的体积不一定是3.36L,故B错误;C、溶液中一定不含I-,故C错误;D、由于原溶液中含SO42-,故沉淀乙一定有BaCO3,也一定含BaSO4,故D错误;故选A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列有关AgCl沉淀的溶解平衡的说法中正确的是( )
A.AgCl沉淀生成和沉淀溶解不断进行,但速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.升高温度,AgCl沉淀的溶解度减小
D.在有AgCl沉淀生成的溶液中加入NaCl固体,AgCl沉淀溶解的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选项中两种气体的分子数一定相等的是
A.质量相等的N2和COB.体积相等的O2和N2
C.氧原子数相等的CO2和COD.原子总数相等的O2和N2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:

溶质的物质的量 | 溶液的密度 | |
硫酸 | c1 | ρ1 |
氨水 | c2 | ρ2 |
(1)表中硫酸的质量分数为_____(不写单位,用含c1、ρ1的代数式表示)。
(2)物质的量浓度为c1mol·L-1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为_____mol·L-1。
(3)物质的量浓度为c2mol·L-1的氨水与![]() c2mol·L-1的氨水等质量混合,所得溶液的密度_____ (填“大于”、“小于”或“等于”,下同)ρ2g·cm-3,所得溶液的物质的量浓度_____
c2mol·L-1的氨水等质量混合,所得溶液的密度_____ (填“大于”、“小于”或“等于”,下同)ρ2g·cm-3,所得溶液的物质的量浓度_____![]() c2mol·L-1(设混合后溶液的体积变化忽略不计)。
c2mol·L-1(设混合后溶液的体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组研究采用BMED 膜堆(示意图如右),模拟精制浓海水为原料直接制备酸碱。BMED膜堆包括阳离子交换膜、阴离子交换膜和双极膜(A、D)。已知: 在直流电源的作用下,双极膜内中间界面层发生水的解离,生成H+和OH-。下列说法错误的是( )
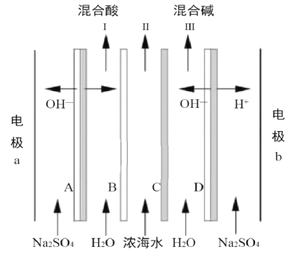
A. 电极a连接电源的正极 B. B为阳离子交换膜
C. 电解质溶液采用Na2SO4溶液可避免有害气体的产生 D. Ⅱ排出的是淡水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是( )
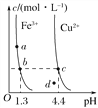
A. Ksp[Fe(OH)3]<Ksp[Cu(OH)2]
B. 加适量NH4Cl固体可使溶液由a点变到b点
C. c、d两点代表的溶液中c(H+)与c(OH-)乘积相等
D. Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应原理对生产有重大的指导意义。回答下列问题:
(1)有两个温度相同的密闭容器A和B,容器A保持容积不变,容器B保持压强不变,起始时向容积相等的A、B中分别充入等量的C(碳)和H2O(g),发生反应:C(s)+H2O(g)![]() CO(g)+ H2(g) (正反应为吸热反应),并分别达到平衡。
CO(g)+ H2(g) (正反应为吸热反应),并分别达到平衡。
①H2O的体积分数:V(A)%_____V(B)%。(填“>”、“<” “=”)
②达到平衡后,在两容器中分别通入等量的氦气,则A中H2O的转化率_______(填“增大” “减小”、“不变”);B中化学平衡_________移动(填“不”“向正反应方向”“向逆反应方向”)。
(2)某温度下,测得0.01mol·L-1 NaOH溶液的pH=10,则在该温度下Kw=______;在此温度下,将pH=11的NaOH溶液aL与pH=2的H2SO4溶液bL混合,若所得溶液为中性,则a:b=_______(假设混合时体积不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B、N、Co均为新型材料的重要组成元素。请回答下列问题:
(1)基态Co原子核外电子占据_________种不同的能级,其中有__________个未成对电子。
(2)Co能形成[Co(CNO)6]3-。
①1mol该离子中含有σ键的数目为_____________________。
②与CNO-互为等电子体的分子为_______________(填化学式,任写一种)
③C、N、O三种基态原子的第一电离能由大到小的顺序为___________(用元素符号表示)。
④相同压强下,CO晶体的熔点高于N2晶体的原因为____________________________。
(3)多硼酸根的结构之一为链状(如图1),化学式为______________,其中B原子的杂化形式为______________。

(4)BN晶体有多种结构,其中立方氮化硼具有金刚石型结构(如图2)。
①晶体的最小环中含有____________个B原子。
②若晶胞参数为anm,晶胞密度为ρg·cm-3,则阿伏加德罗常数的值可表示为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com