
【题目】石膏转化为硫酸钾和CaCl2的工艺流程如下:
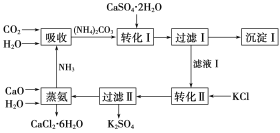
(1)CO2是一种很重要的副产品,工业上获得CO2的途径是_____(用化学方程式表示)。
(2)转化Ⅰ中发生反应的离子方程式为______,过滤Ⅰ得到的滤渣的主要成分是_____。过滤Ⅰ得到的滤液是______,检验滤液中含有CO32-的方法是_______________。
(3)转化Ⅱ中发生反应的化学方程式为_____,转化Ⅱ中可获得K2SO4的原因是___________。
(4)上述工艺流程中体现绿色化学理念的是__________________________。
(5)氯化钙结晶水合物是目前常用的无机储热材料,选择的依据是____。
a.熔点较低(29 ℃熔化) b.能制冷 c.无毒 d.能导电
【答案】CaCO3![]() CaO+CO2↑ CaSO4+CO32-===CaCO3↓+SO42- CaCO3 (NH4)2SO4 取少量滤液于试管中,滴加稀HCl,若有无色无味能使澄清石灰水变浑浊的气体产生,则证明滤液中含有CO32-,若无明显现象,则滤液中不含CO32- 2KCl+(NH4)2SO4===K2SO4↓+2NH4Cl KCl、(NH4)2SO4、K2SO4、NH4Cl四种物质的溶解度受温度的影响不同 氨在工艺中循环使用、使用的原料无毒(其他合理答案也可) ac
CaO+CO2↑ CaSO4+CO32-===CaCO3↓+SO42- CaCO3 (NH4)2SO4 取少量滤液于试管中,滴加稀HCl,若有无色无味能使澄清石灰水变浑浊的气体产生,则证明滤液中含有CO32-,若无明显现象,则滤液中不含CO32- 2KCl+(NH4)2SO4===K2SO4↓+2NH4Cl KCl、(NH4)2SO4、K2SO4、NH4Cl四种物质的溶解度受温度的影响不同 氨在工艺中循环使用、使用的原料无毒(其他合理答案也可) ac
【解析】
根据流程图进行分析解答:首先是CO2和H2O、NH3反应生成(NH4)2CO3,在加入石膏生成沉淀CaCO3和(NH4)2SO4,过滤后再加入KCl,生成K2SO4和NH4Cl,再加入CaO和水即可得到CaCl2![]() 6H2O。
6H2O。
(1)工业上常利用高温煅烧石灰石的方法制二氧化碳气体,反应的方程式为CaCO3![]() CaO+CO2↑,故答案为:CaCO3
CaO+CO2↑,故答案为:CaCO3![]() CaO+CO2↑。
CaO+CO2↑。
(2)转化I是碳酸铵和石膏悬浊液反应生成CaCO3和(NH4)2SO4,反应的离子方程为CaSO4+CO32-=CaCO3↓+SO42-,过滤I得到的滤渣的主要成分是CaCO3,过滤I得到的滤液是(NH4)2SO4,检验滤液中含有CO32-的方法是:取少量滤液于试管中,滴加稀HCl,若有无色无味能使澄清石灰水变浑浊的气体产生,则证明滤液中含有CO32-;若无明显现象,则滤液中不含CO32-;故答案为:CaCO3;(NH4)2SO4;取少量滤液于试管中,滴加稀HCl,若有无色无味能使澄清石灰水变浑浊的气体产生,则证明滤液中含有CO32-,若无明显现象,则滤液中不含CO32-。
(3)转化I的滤液中的溶质为(NH4)2SO4和KC1的饱和溶液反应得到NH4Cl和K2SO4,反应方程式为2KCl+(NH4)2SO4=K2SO4↓+2NH4Cl;转化II中可获得K2SO4的原因是KCl、(NH4)2SO4、K2SO4、NH4Cl四种物质的溶解度受温度的影响不同,故答案为: 2KCl+(NH4)2SO4=K2SO4↓+2NH4Cl; KCl、(NH4)2SO4、K2SO4、NH4Cl四种物质的溶解度受温度的影响不同。
(4)由绿色化学的特点可知,碳酸钙分解生成CO2和CaO都参与反应,硫酸钙和氯化钾转化为硫酸钾和氯化钙、氨在工艺中循环使用等都达到了原子利用率高,没有有害物质排放到环境中,所以符合绿色化学的特点;故答案为:氨在工艺中循环使用,使用的原料无毒,转化率高。
(5) 无机物类能作为储热的特点:密度大、腐蚀性小、成本低,氯化钙结晶水合物(CaCl2![]() 6H2O) 熔点低易熔化,且无毒腐蚀性小、成本低,所以是目前常用的无机储热材料,故ac符合题意,储热材料与溶解性、能制冷性、导电性无关,故bd不符合题意;答案为ac。
6H2O) 熔点低易熔化,且无毒腐蚀性小、成本低,所以是目前常用的无机储热材料,故ac符合题意,储热材料与溶解性、能制冷性、导电性无关,故bd不符合题意;答案为ac。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在一密闭容器中发生反应:2A(g)+2B(g) ![]() C(s)+3D(g) ΔH<0,达到平衡时采取下列措施,可以使正反应速率υ正增大、D的物质的量浓度c(D)增大的是( )
C(s)+3D(g) ΔH<0,达到平衡时采取下列措施,可以使正反应速率υ正增大、D的物质的量浓度c(D)增大的是( )
A. 缩小容积,增大压强B. 扩大容积,减小压强
C. 移走少量CD. 容积不变,充入“惰性”气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应式:mX(g)+nY(?)![]() pQ(s)+2mZ(g),已知反应已达平衡,此时c(X)=0.3mol/L,其他条件不变,若容器缩小到原来的
pQ(s)+2mZ(g),已知反应已达平衡,此时c(X)=0.3mol/L,其他条件不变,若容器缩小到原来的![]() ,c(X)=0.5mol/L,下列说法正确的是( )
,c(X)=0.5mol/L,下列说法正确的是( )
A.反应向逆方向移动B.Y可能是固体或液体
C.系数n>mD.Z的体积分数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,发生反应NH2COONH4(s)2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
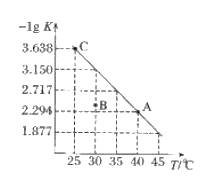
A. 该反应的△H>0
B. C点对应状态的平衡常数K(C)=103.638
C. NH3的体积分数不变时,该反应一定达到平衡状态
D. 30℃时,B点对应状态的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列卤代烃在KOH醇溶液中加热不反应的是( )
①![]() ②
②![]() ③(CH3)3C—CHBr2 ④CHCl2—CHBr2 ⑤
③(CH3)3C—CHBr2 ④CHCl2—CHBr2 ⑤![]() ⑥CH3Cl
⑥CH3Cl
A. ①③⑥B. ②③⑤C. ②④D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】充分燃烧2.8g某有机物A,生成8.8gCO2和3.6gH2O,这种有机物蒸气的相对密度是相同条件下N2的2倍.
(1)求该有机物的分子式________________.
(2)该有机物链状同分异构体的结构简式为:_________________________________________________________________、______________________________________________________、___________________________________________________.
(3)若有机物A在核磁共振氢谱中只有一个信号峰(即只有一种氢原子),则用键线式表示的结构简式为__________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHSO4在水中的电离方程式为:NaHSO4 = Na+ + H+ + SO42—。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( )
A.该温度高于25℃
B.由水电离出来的H+的浓度是1.0×10-10mol·L-1
C.NaHSO4晶体的加入抑制了水的电离
D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种中学化学常见的单质及其化合物相互转化的关系图如下:
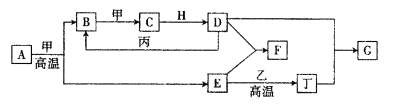
可供参考的信息有:
①甲、乙、丙、丁为单质,其余为化合物
②A由X和Y两种元素组成,其原子个数比为l︰2,元素质量之比为7︰8。
③B气体是引起酸雨的主要物质,H常温下为无色无味的液体,E常用作红色油漆和涂料。
试根据上述信息回答下列问题:
(1)A的化学式为___________,每反应lmol的A转移的电子数为_____________mol;
(2)F与丁单质也可以化合生成G,试写出该反应的离子方程式:______________________;
(3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①、②、③。
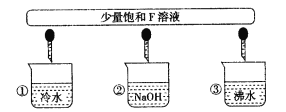
试将①、②、③对应的分散质具体的化学式填人下列方框中:________________
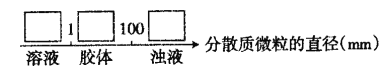
(4)化合物M与H组成元素相同,可以将G氧化为F,且不引进新的离子。试写出M在酸性环境下将G氧化为F的离子方程式:________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知淀粉、葡萄糖及A、B、C、D、E之间的相互转化关系如下图所示请回答:

(1)B中的官能团名称是___________________A的电子式是_________________。
(2)已知C与D发生加成反应生成E,其化学方程式为_______________________。
(3)下列说法正确的是_____。
A.题中的“某工艺”指的是裂解
B.可用溴的四氯化碳溶液鉴别B和C
C.E不溶于水,能使酸性高锰酸钾溶液褪色
D.A在热Cu丝催化氧化下可生成相对分子质量比它小2的有机物
(4)请补充完整证明反应①是否发生的实验方案:取反应①的溶液2 mL于试管中,______________。(实验中可供选择的试剂:10%的NaOH溶液、5%的CuSO4溶液、碘水)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com