
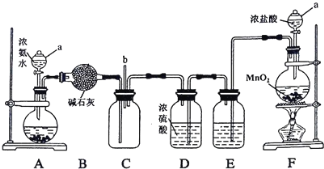
【题目】某化学兴趣小组利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气发生反应的装置。
请回答下列问题:
(1)仪器a的名称为_________;装置A的圆底烧瓶中盛放的固体物质可选用__________(填序号)。
a.氯化钠 b.氢氧化钠 c.碳酸钙
(2)装置F的圆底烧瓶中发生反应的离子方程式为___________;装置E的洗气瓶中盛放的试剂为 ____________。
(3)反应过程中,装置C的集气瓶中有大量白烟产生,另一种产物为空气的主要成分之一,该反应的化学方程式为 _________。
(4)从装置C的b处逸出的尾气中含有少量Cl2,为防止其污染环境,可将尾气通过盛有 ________溶液的洗气瓶。
【答案】分液漏斗 b MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 饱和氯化钠溶液 8NH3+3Cl2=N2+6NH4Cl 氢氧化钠
Mn2++Cl2↑+2H2O 饱和氯化钠溶液 8NH3+3Cl2=N2+6NH4Cl 氢氧化钠
【解析】
A装置制备氨气,利用B装置中的碱石灰干燥氨气,F装置制备氯气,E装置除去氯气中的氯化氢,D装置干燥氯气,在C装置中氯气氧化氨气,据此解答。
(1)根据仪器构造可判断仪器a的名称为分液漏斗;a.氯化钠与氨水不反应,不能制备氨气;b.氢氧化钠溶于水放热,且增大氢氧根的浓度,可以和氨水混合制备氨气;c.碳酸钙与氨水不反应,不能制备氨气;答案选b;
(2)浓盐酸和二氧化锰在加热条件下反应生成氯化锰、氯气和水,反应的方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O。浓盐酸易挥发,生成的氯气中含有氯化氢,E中装有饱和食盐水,食盐水中含有氯离子,能抑制氯气的溶解,作用为除去氯气中混有的氯化氢;
Mn2++Cl2↑+2H2O。浓盐酸易挥发,生成的氯气中含有氯化氢,E中装有饱和食盐水,食盐水中含有氯离子,能抑制氯气的溶解,作用为除去氯气中混有的氯化氢;
(3)C内出现浓厚的白烟为氯化铵,另一生成物是空气的主要成分之一为氮气,因此该反应的方程式为3Cl2+8NH3=N2+6NH4Cl;
(4)氯气是有毒气体,需要尾气处理,则可将尾气通过盛有氢氧化钠溶液的洗气瓶吸收。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】H2S2O3是一种弱酸,实验室欲用0.01 mol·L-1的Na2S2O3溶液滴定I2溶液,发生的反应为:I2+2Na2S2O32NaI+Na2S4O6,下列说法合理的是( )
A. 该滴定可选用如图所示装置示剂;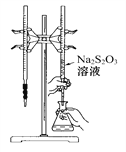
B. 该滴定可用甲基橙作指;
C. Na2S2O3是该反应的还原剂;
D. 该反应中每消耗2 mol Na2S2O3,电子转移数为4 mol;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是:
A. 反应达到平衡时,X的转化率为50% B. 反应可表示为X+3Y![]() 2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、R、X、Y、Z、L六种元素的原子序数依次增大,R和L是同主族元素,R的最外层电子数比次外层电子数少1,L的单质常温常压下是紫黑色固体。Q和X形成的离子化合物XQ是碱石灰的主要成分。X、Y、Z位于同一周期,Y的外围电子数是最外层电子数的6倍,Z位于ds区且不能和稀硫酸反应生成H2。请回答下列问题:
(1)Q的价层电子排布式为___________________,L的含氧酸HLO3中L的杂化方式为__________,酸根LO3-的离子构型为________________。
(2)ZR42-的配体是______,在ZSO4溶液中加入过量KCN,生成配合物[Z(CN)4]2—,则1mol该配合物中含有的π键的数目是_______。与Z同周期的元素中,与Z原子最外层电子数相等的元素还有_________(填元素符号)
(3)Y的氧化物呈如下图所示的无限链状结构,则该氧化物的化学式为______________。

(4)X和Z的晶体堆积模型相同,配位数为______________,已知X原子半径约为200pm,则晶体X的密度为__________________g/cm3(计算结果保留两位有效数字)。
(5)XL2晶体含有层状结构,其层内有强极性共价键,层间以范德华力相连接,则XL2的晶体类型是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次增大,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层电子数是次外层电子数的3倍。
(1)试推断它们各是什么元素?写出它们的元素符号:
A________,B___________,C__________,D___________。
(2)甲、乙、丙、丁均含有以上元素中的一种或几种组成的10电子微粒;
①甲为分子,且能刻蚀玻璃,则甲的化学式为______
②乙为气体,且遇到无色酚酞溶液变成红色,则乙的化学式为_______
③丙为阳离子,丁为阴离子,且丙和丁在加热条件下生成的两种物质也是10电子微粒,请写出该反应离子方式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、环境密切相关。如图为雾霾的主要成分示意图。下列说法不正确的是

A. 雾属于胶体,能产生丁达尔效应
B. SO2 和 N xOy 都属于酸性氧化物
C. 汽车尾气的大量排放是造成雾霾天气的人为因素之一
D. 重金属离子可导致蛋白质变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )
①Zn为正极,Cu为负极;
②H+向负极移动;
③电子是由Zn经外电路流向Cu;
④Cu极上有H2产生;
⑤若有1mol电子流过导线,则产生的H2为0.5mol;
⑥正极的电极反应式为Zn﹣2e﹣═Zn2+.

A.①②③ B.③④⑤ C.④⑤⑥ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某条件下,合成氨反应的数据如下:N2(g)+3H2(g) ![]() 2NH3(g)
2NH3(g)
N2 | H2 | NH3 | |
起始浓度(mol/L) | 1.0 | 3.0 | 0.2 |
2s末浓度(mol/L) | 0.6 | 1.8 | 1.0 |
4s末浓度(mol/L) | 0.4 | 1.2 | 1.4 |
当用氨气浓度的增加来表示该反应的化学反应速率时,下列说法错误的是( )
A. 2~4 s内的平均反应速率为0.2 mol·L-1·s-1
B. 前4 s内的平均反应速率为0.3 mol·L-1·s-1
C. 前2 s内的平均反应速率为0.4 mol·L-1·s-1
D. 2 s末的反应速率为0.4 mol·L-1·s-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com