
将0.1 mol/L CH3COOH溶液加水稀释或加少量CH3COONa晶体,都会引起( )
A.溶液的pH增加
B.CH3COOH电离程度变大
C.溶液的导电能力减弱
D.溶液中c(OH-)减小
科目:高中化学 来源: 题型:
现有等浓度的下列物质的溶液:①CH3COOH,②HClO,③NaClO,④H2CO3,⑤Na2CO3,⑥NaHCO3。按溶液pH由小到大排列正确的是( )
A.④①②⑤⑥③ B.④①②⑥⑤③
C.①④②⑥③⑤ D.①④②③⑥⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用铝土矿(主要成分是Al2O3、Fe2O3、SiO2)提纯Al2O3做冶炼铝的原料,提取的操作过程可用以下流程图表示:[已知:2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓,SiO2能被NaOH溶解]
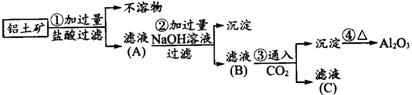
(1)请写出下列各步反应的化学方程式:
①________,________。 ②________,________。
③________,________。 ④________,________。
(2)若①步没有过滤操作而直接进入步骤②,对后面的操作会有什么影响?
查看答案和解析>>
科目:高中化学 来源: 题型:
氨在国民经济中占有重要的地位,请参与下列探究。
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气。
C(s)+H2O(g)H2(g)+CO(g)
ΔH=+131.3 kJ,ΔS=+133.7 J/K
该反应在低温下能否自发反应__________(填“能”或“否”)。
(2)已知在400℃时,N2(g)+3H2(g)2NH3(g)的K′=0.5。
①2NH3(g)N2(g)+3H2(g)的K=__________(填数值)。
②400℃时,在0.5 L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2 mol、1 mol、2 mol,则此时反应v(N2)正__________v(N2)逆(填“>”、“<”、“=”或“不确定”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
符合如图所示的热化学方程式是( )
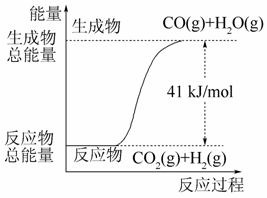
A.CO+H2O===CO2+H2 ΔH=+41 kJ/mol
B.CO(g)+H2O(g)===CO2(g)+H2(g) ΔH=-41 kJ/mol
C.CO2(g)+H2(g)===CO(g)+H2O(g) ΔH=+41 kJ/mol
D.CO2(g)+H2(g)===CO(g)+H2O(g) ΔH=-41 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表述中正确的是( )
A.NH4Cl溶液因水解而显酸性,故NH4Cl是弱电解质
B.纯碱溶液因水解而显碱性,水解的离子方程式为CO +2H2OH2CO3+2OH-
+2H2OH2CO3+2OH-
C.可乐因含碳酸而显酸性,电离方程式为H2CO32H++CO
D.配制FeCl3溶液时,先将FeCl3溶于较浓的盐酸中,然后再加水稀释到所需浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
向一定体积的密闭容器中加入2 mol A、0.6 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图(Ⅰ)所示,其中t0~t1阶段c(B)未画出。图(Ⅱ)为t2时刻后改变反应条件,化学反应速率随时间变化的情况,四个阶段改变的条件均不相同,每个阶段只改变浓度、温度、压强、催化剂中的一个条件,其中t3~t4阶段为使用催化剂。
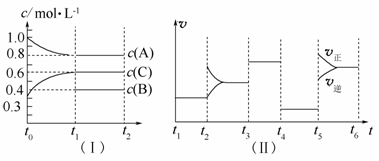
请回答下列问题:
(1)若t1=15 min,则t0~t1阶段以C物质的浓度变化表示反应速率为____________________________。
(2)t4~t5阶段改变的条件为__________,B的起始物质的量浓度为__________。各阶段平衡时对应的平衡常数如下表所示:
| t1~t2 | t2~t3 | t3~t4 | t4~t5 | t5~t6 |
| K1 | K2 | K3 | K4 | K5 |
则K1=__________(保留两位小数),K1、K2、K3、K4、K5之间的关系为________________________(用“>”、“<”或“=”连接)。
(3)t5~t6阶段保持容器内温度不变,若A的物质的量共变化了0.01 mol,而此过程中容器与外界的热交换总量为a kJ,写出此温度下该反应的热化学方程式__________________________________。
(4)在相同条件下,若起始时容器中加入a molA、b mol B和c mol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有下列几组物质(将正确答案字母填入空中)
A.金刚石和石墨 B.C2H6和C5H12 C.C2H4和C2H6
D.CH3CH2CH2CH3和CH3CH(CH3)2 E.35Cl和37Cl
属于同分异构体的是________;属于同素异形体的是_______;属于同系物的是________;属于同位素的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g,则下列有关叙述中正确的是
A.加入合金的质量可能为9.6g
B.沉淀完全时消耗NaOH溶液体积为150mL
C.参加反应的硝酸的物质的量为0.4mol
D.溶解合金时产生NO气体体积0.224L(以标准状况)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com