
【题目】根据下列物质的名称,就能确认是纯净物的是( )
A. 溴乙烷 B. 二溴乙烷 C. 已烯 D. 二甲苯
科目:高中化学 来源: 题型:
【题目】用10 mL的0.1 mol·L-1 BaCl2溶液恰好可使相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是( )
A. 3∶2∶2 B. 1∶2∶3 C. 1∶3∶3 D. 3∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最简式相同,但既不是同系物,又不是同分异构体的是( )
A. 辛烯和3甲基1丁烯 B. 苯和乙炔
C. 1氯丙烷和2氯丙烷 D. 甲基环己烷和己炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是非常重要的有机物。请回答下列问题:
(1)乙烯官能团的名称是___________________;
(2)用化学方程式表示乙烯的三种不同类别的性质(有机物用结构简式表示)
①_______________________________;
②___________________________;
③___________________________。
(3)如果用乙烯制作燃料电池,KOH作电解液。写出正负极反应式:
正极_________________________;
负极_________________________;
(4)相比较燃烧,形成原电池的相关说法正确的是 。
A. 形成原电池后能量利用率更高
B. 电池负极有火焰而正极没有
C. 电池工作时,电解液pH不变
D. 两极电极材料可以相同
(5)丁烷裂解有有两种方式,并同时进行。一是裂解为乙烯和乙烷;二是裂解为甲烷和丙烯。现有1mol丁烷,加热裂解,一段时间后,测得混合气体中含丁烷0.4mol。此时混合气体平均相对分子质量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列平衡体系中,升温或减压都能使平衡向正反应方向移动的是( )
A. N2(g)+3H2(g)![]() 2NH3(g) ΔH <0
2NH3(g) ΔH <0
B. N2(g)+O2(g)![]() 2NO(g) ΔH <0
2NO(g) ΔH <0
C. C(s)+2H2O(g)![]() CO2(g)+2H2(g) ΔH >0
CO2(g)+2H2(g) ΔH >0
D. 2SO2(g)+O2(g)![]() 2SO3(g) ΔH <0
2SO3(g) ΔH <0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.下面是中学化学中常用玻璃仪器组成的实验装置图(根据需要可在其中加入液体或固体)。

请回答下列问题:
(1)能用作干燥氨气的装置有___________(填字母);
(2)既能用于收集氯气又能用于收集一氧化氮气体的装置有___________(填字母);
(3)在氯气和铁反应实验中,能添加在制氯气和反应装置之间以除去氯气中氯化氢等杂质气体的装置有___________(填字母);
(4)若用C装置作二氧化硫与烧杯中氢氧化钠溶液反应的实验,则其中广口瓶的作用是__________。
II.我国化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下:
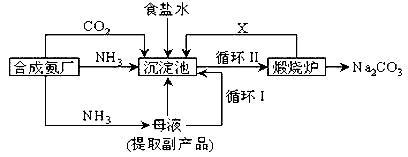
(1) 沉淀池中发生的化学反应方程式是______________________。
(2) 写出上述流程中X物质的分子式___________。
(3)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加___________。
(4) 向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有______________。
a.增大NH4+的浓度,使NH4Cl更多地析出
b.使NaHCO3更多地析出
c.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据碘与氢气反应的热化学方程式 (i)I2(g)+H2(g)![]() 2HI(g) △H=" -" 9.48kJ/mol ,(ii) I2(s)+H2(g)
2HI(g) △H=" -" 9.48kJ/mol ,(ii) I2(s)+H2(g)![]() 2HI(g) △H=" +" 26.48kJ/mol,下列判断正确的是
2HI(g) △H=" +" 26.48kJ/mol,下列判断正确的是
A. 254g I2(g)中通入2g H2(g),反应放热9.48 kJ
B. 1 mol固态碘与1mol气态碘所含的能量相差l7.00 kJ
C. 反应(i)的产物比反应(ii)的产物稳定
D. 反应(i) 拆开1mol I-I键与1mol H-H键需要的总能量小于拆开2mol H-I键需要的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设N0为阿伏加德罗常数的值。下列叙述正确的是( )。
A. 1.0 L 1.0 mol·L-1的NaAlO2水溶液中含有的氧原子数为2N0
B. 12 g石墨烯(单层石墨)中含有六元环的个数为0.5N0
C. 25 ℃时pH=13的NaOH溶液中含有OH-的数目为0.1N0
D. 1 mol的羟基与1 mol的氢氧根离子所含电子数均为9N0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅单质及其化合物应用范围很广。请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:
![]()
①写出由纯SiHCl3制备高纯硅的化学反应方程式:_____________。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式:____________________。
(2)化学研究性学习小组在探究硅的制取方法时,从资料查阅到下列信息:①Mg在高温条件下可与SiO2反应;②金属硅化物与稀H2SO4反应生成硫酸盐和SiH4;③SiH4在空气中自燃。
他们根据信息进行实验,当用足量稀H2SO4溶解第①步实验获得的固体产物时,发现有爆鸣声和火花;然后过滤、洗涤、干燥;最后称量、计算,测得其产率只有预期值的63%左右。
①第①步实验发生反应的化学方程式是 ;______ ____。
②用稀H2SO4溶解第①步实验获得固体产物时,产生爆鸣声和火花的原因是(用化学方程式表示)_________________, 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com