
【题目】已知充分燃烧ag乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量bkJ,则乙炔燃烧的热化学方程式正确的是( )
A.2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣2bkJ/mol
B.C2H2(g)+ ![]() O2(g)═2CO2(g)+H2O(l)△H=2bkJ/mol
O2(g)═2CO2(g)+H2O(l)△H=2bkJ/mol
C.2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4bkJ/mol
D.2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=bkJ/mol
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料。某AlN样品仅含有Al2O3杂质,为测定AlN含量,设计如下两种实验方案。(已知:AlN+NaOH+ H2O==NaAlO2+ NH3↑)
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。
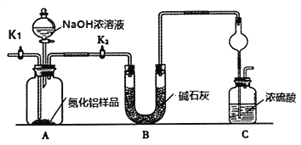
(1)上图C装置中球形干燥管的作用是_________________。
(2)完成以下实验步骤:组装好实验装置,检查装置气密性并加入实验药品,关闭K1,打开K2 ,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。
①检验装置气密性的方法是__________________________
②通入氮气的目的是__________________________________________________。
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见__________________。
【方案2】用下图装置测定m g样品中AlN的纯度(部分夹持装置已略去)。
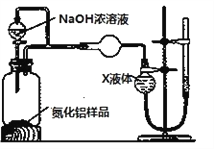
(4)为测定生成气体的体积,量气装置中的X液体可以是___________
A.CCl4 B.H2O C.NH4Cl溶液 D.苯
(5)若m g样品完全反应,测得生成气体的体积为V mL(已转换为标准状况),则AlN的质量分数是_____________________。
若其他操作均正确,但反应结束后读数时,右侧量气管中液面高于左侧球型管中液面,则最后测得AlN的质量分数会_________(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于加成反应的是( )
A.乙烯使酸性KMnO4溶液褪色
B.将苯滴入溴水中,振荡后水层接近无色
C.乙烯使溴水褪色
D.甲烷与氯气混合,光照一段时间后黄绿色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性
B. 常温下,铜片放入浓硫酸中,无明显变化,说明铜在冷的浓硫酸中发生钝化
C. 将分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水
D. Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行试验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
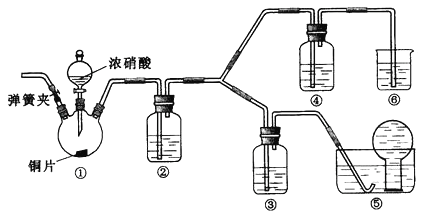
可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应![]()
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是_________
(2)滴加浓硝酸之前的操作是检验装置的气密性,加入药品,打开弹簧夹后_________
(3)装置①中发生反应的化学方程式是__________
(4)装置②的作用是_________,发生反应的化学方程式是___________
(5)该小组得出的结论所依据的试验现象是____________
(6)试验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下3个实验来判断两种看法是否正确。这些方案中可行的是___(选填序号字母)
a.加热该绿色溶液,观察颜色变化
b.加水稀释该绿色溶液,观察颜色变化
c.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验.
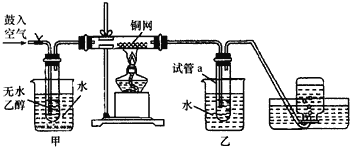
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式____________________;
(2)甲和乙两个水浴作用不相同,甲的作用是________________,乙的作用是_________________;
(3)下列反应原理可以用于检查司机是否酒后开车:
2K2Cr2O7+3C2H5OH+8H2SO4=2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O
(橙色) (绿色)
①若司机酒后开车,应显示出______色;
②生成1mol Cr3+转移的电子数为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【有机化学基础】I.有机物A、B、C、D、E之间发生如下的转化:

(1)写出C物质的结构简式:_____________________________。
(2)上述②~⑧转化反应中,属于取代反应的有_____________________________。
(3)属于加成反应的有________________。(用反应序号填写)
(4)向A的水溶液中加入新制的Cu(OH)2并加热时产生的实验现象是_____________________。
(5)B+D→E:_______________________________。
(6)乙烯生成聚乙烯:__________________________________________________。
II:已知葡萄糖在乳酸菌的作用下转化为乳酸,乳酸的结构简式为![]() 。
。
试回答:
(7)乳酸分子中含有____________和____________两种官能团(写名称)。
(8)乳酸与金属钠反应的化学方程式为_____________________________________。
(9)乳酸与Na2CO3溶液反应的化学方程式为________________________________。
(10)乳酸在浓硫酸作用下,两分子相互发生酯化反应生成环状酯,此环状酯的结构简式为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com