
【题目】A、B、C、D、E、F元素是原子序数依次增大的六种短周期元素。已知:元素A的原子半径在所有元素中最小,元素B的一种同位素可测定文物年代,D原子最外层电子数与核外电子总数之比为3∶4,E和D可以形成原子个数比为1∶1和 2∶1的两种离子化合物,F是同周期中简单离子中半径最小的元素。据此回答下列问题。
(1) F元素的原子结构示意图为________________,E在元素周期表中的位置为_______________。
(2) C元素与A元素形成一种离子CA![]() ,请写出检验溶液中存在该离子的实验操作、现象和结论: _____ ____。
,请写出检验溶液中存在该离子的实验操作、现象和结论: _____ ____。
(3) 写出F元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式:___________________。
(4) 由以上某些元素组成的化合物X、Y、Z、W有如下转化关系(已知:Y和Z在水溶液中存在微粒种类相同)。
![]()
① X化合物中含有的化学键类型有__________________________;
② X+Z→Y的离子方程式为_____________________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.58 kJmol-1
CH3OH(g)+H2O(g) △H1=-49.58 kJmol-1
反应Ⅱ:CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2H2(g)![]() CH3OH(g) △H3=-90.77 kJmol-1
CH3OH(g) △H3=-90.77 kJmol-1
回答下列问题:
(1)反应Ⅱ的△H2=__________,若反应Ⅰ、Ⅱ、Ⅲ平衡常数分别为K1、K2、K3,则K2=________(用K1、K3表示)。
(2)反应Ⅲ自发进行条件是___________(填“较低温度”、“较高温度”或“任何温度”)。
(3)在一定条件下2 L恒容密闭容器中充入3 mol H2和1.5 mol CO2,仅发生反应Ⅰ,实验测得不同反应温度与体系中CO2的平衡转化率的关系,如下表所示。
温度(℃) | 500 | T |
CO2的平衡转化率 | 60℅ | 40℅ |
①T______500℃(填“高于”或“低于”)。
②温度为500℃时,该反应10 min时达到平衡:
a.用H2表示该反应的速率为____________________;
b.该温度下,反应I的平衡常数K=______________。
(4)某研究小组将一定量的H2和CO2充入恒容密闭容器中并加入合适的催化剂(发生反应I、Ⅱ、Ⅲ),测得不同温度下体系达到平衡时CO2的转化率(a)及CH3OH的产率(b),如图所示。
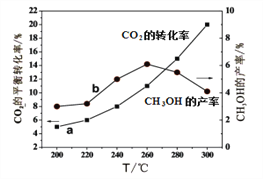
①该反应达到平衡后,为同时提高反应速率和甲醇的生成量,以下措施一定可行的是_____(选填编号)。
A.升高温度 B.缩小容器体积 C.分离出甲醇 D.增加CO2的浓度
②据图可知当温度高于260℃后,CO的浓度随着温度的升高而_________(填“增大”、“减小”、“不变”或“无法判断”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用二氧化碳废气生产化工产品是解决室温效应的有效途径之一,对用二氧化碳为主要原料生产的四种产品(如下图所示)的相关说法不正确的是
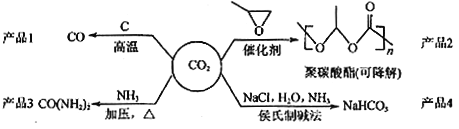
A.反应CO2(g)+C(s)=2CO(g)的△H>0,△S>0
B.用聚碳酸酯代替聚乙烯等传统塑料,可消除白色污染
C.CO(NH2)2与NH4CNO互为同分异构体,两者化学性质相同
D.侯氏制碱法的工艺过程中应用了物质溶解度的差异
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关糖类、油脂、蛋白质的叙述正确的是
A. 向淀粉溶液中加入碘水后,溶液变蓝色
B. 蛋白质纤维素、蔗糖、PVC都是高分子化合物
C. 硫酸铜溶液、硫酸铵溶液均可使蛋白质发生变性
D. 变质的油脂有难闻的特味气味,是由于油脂发生了水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于催化剂的说法,正确的是
A. 催化剂能使不起反应的物质发生反应
B. 催化剂在化学反应前后,化学性质和质量都不变
C. 催化剂不能改变化学反应速率
D. 任何化学反应都需要催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com