
【题目】在生物体内含量极少,且必不可少的化学元素是
A. Fe Mn Zn Mg B. Zn Cu Mn Ca C. H O Na Mg D. Zn Cu B
科目:高中化学 来源: 题型:
【题目】用下列方法制备胶体:①0.5 mol/L的BaCl2溶液和等体积2 mol/L的硫酸混合振荡;②把1 mol/L饱和的FeCl3溶液逐滴加入20 mL沸水中,边加边振荡;③1 mol/L NaOH溶液滴
到1 mol/L FeCl3溶液中,可行的是( )
A.①② B.①③
C.② D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,属于吸热反应的是( )
①液态水汽化 ②将胆矾加热变成白色粉末 ③浓硫酸稀释
④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰
A.①④ B.②③ C.②④ D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代传感信息技术在化学实验中有广泛的应用。某小组用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理(如图1所示),并测定电离平衡常数Kb。
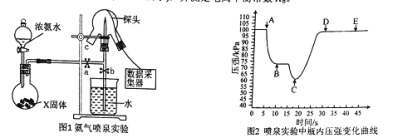
(1)实验室可用浓氨水和X固体制取NH3 , X固体可以是 。
A.生石灰 B.无水氯化钙 C.五氧化二磷 D.碱石灰
(2)检验三颈瓶集满NH3的方法是: 。
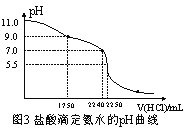
(3)关闭a,将带有装满水的胶头滴管的橡皮塞塞紧c口, ,引发喷泉实验,电脑绘制三颈瓶内气压变化曲线如图2所示。图2中 点时喷泉最剧烈。
(4)从三颈瓶中用 (填仪器名称)量取20.00 mL氨水至锥形瓶中,用 0.05000 mol/L HCl滴定。用pH计采集数据、电脑绘制滴定曲线如图3所示。
(5)据图3计算,当pH =11. 0 时,NH3H2O电离平衡常数Kb的近似值,Kb≈ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼、镁及其化合物在工农业生产中应用广泛。已知:硼镁矿主要成分为Mg2B2O5·H2O, 硼砂的化学式为Na2B4O7·10H2O。利用硼镁矿制取金属镁及粗硼的工艺流程如下:

回答下列有关问题:
(1)硼砂中B的化合价为__________,溶于热水后,常用H2SO4调pH到2~3制取H3BO3,反应的离子方程式为__________________。
(2)氧化物X为H3BO3晶体加热脱水的产物,其与Mg反应制取粗硼的化学方程式为______________,该反应中的氧化剂是(填化学式)_______________。
(3)硼酸是一种一元弱酸,它与水作用时结合水电离的OH-而释放出水电离的H+,这一变化的化学方程式为____________________。皮肤上不小心碰到氢氧化钠溶液,一般先用大量水冲洗,然后再涂上硼酸溶液,则硼酸与氢氧化钠反应的离子方程式为 。
(4)MgCl2·7H2O需要在HCl氛围中加热制MgCl2,其目的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是
A.向Al2(SO4)3溶液中加入过量NH3·H2O:Al3++4NH3·H2O===[Al(OH)4]-+4NH![]()
B. 铅酸蓄电池充电时的正极反应:PbO2+4H++SO![]() +2e-===PbSO4+2H2O
+2e-===PbSO4+2H2O
C.Fe2(SO4)3溶液与Ba(OH)2溶液反应:Fe3++SO42-+Ba2++3OH-===Fe(OH)3 ↓ + BaSO4↓
D.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:2NH4++Fe2++4OH-===Fe(OH)2↓+2NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.反应AlCl3+4NaOH===NaAlO2+3NaCl+2H2O,可以设计成原电池
B.Zn和稀硫酸反应时,加入少量CuSO4溶液能加快产生H2的速率
C.把Fe片和Cu片放入稀硫酸中,并用导线把二者相连,观察到Cu片上产生大量气泡,说明Cu与H2SO4能发生反应而Fe被钝化
D.Zn-Cu原电池工作过程中,溶液中H+向负极作定向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com