
【题目】对A+3B=2C+2D来说,下列四种不同情况下的反应速率最快的是
A. υ(A)=0.25 mol/(L·min) B. υ(B)=0.6 mol/(L·min)
C. υ(C)=0.5 mol/(L·min) D. υ(D)=0.6 mol/(L·min)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是短周期主族元素,且原子序数依次增大。在短周期中A元素原子半径最小,D元素原子半径最大,B的简单氢化物的水溶液呈碱性,C、E同主族,形成的化合物为EC2、EC3。回答下列问题:
(1)E在元素周期表中的位置为_____________________________。
(2)比较B与C简单氢化物的热稳定性:_____> 。(填化学式)
(3)D,C两元素组成的化合物D2C2的电子式为_____________________,D2C2与水反应的化学方程式为 ______________________________________________。
(4)下列事实能说明元素F的非金属性比元素E的非金属性强的是______。
A.元素F形成的单质比元素E形成的单质的熔点低
B.F和E两元素的简单氢化物受热分解,前者的分解温度高
C.F2通入到D2E的溶液中出现浑浊
D.F氢化物的酸性比E氢化物的酸性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用某些有机物之间的相互转换可以贮存太阳能,如原降冰片二烯(NBD)经过太阳光照转化成为四环烷(Q)的反应为
 △H=+88.62 kJ/mol
△H=+88.62 kJ/mol
(1)以下叙述错误的是______(填序号)
A.NBD的能量比Q的能量高 B.NBD和Q互为同分异构体
C.NBD的分子式为C7H8 D.NBD能使酸性高锰酸钾溶液褪色
(2)NBD有多种同分异构体,其中属芳香烃的只有一种,其结构简式为________。若用氘(D)原子取代NBD分子中的一个H原子,可得到的同分异构体共有_______种。
(3)试写出NBD与足量溴水充分反应的化学方程式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】长式周期表共有18个纵列,从左到右排为1~18列,即碱金属为第1列,稀有气体元素为第18列.按这种规定,下列说法正确的是( )
A.第14列元素中未成对电子数是同周期元素中最多的
B.只有第2列的元素原子最外层电子排布为ns2
C.第四周期第8列元素是铁元素
D.第15列元素原子的价电子排布为ns2np5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国成功研制的一种新型可充放电 AGDIB 电池(铝-石墨双离子电池)采用石墨、铝锂合金作为电极材料,以常规锂盐和碳酸酯溶剂为电解液。电池反应为 CxPF6+LiyAl=Cx+LiPF6+Liy-1+Al。放电过程如图,下列说法正确的是
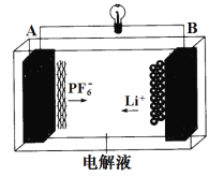
A. B为负极,放电时铝失电子
B. 电解液可以用常规锂盐和水代替
C. 充电时 A 电极反应式为 Cx + PF6- - e-= CxPF6
D. 废旧 AGDIB 电池进行“放电处理”时,若转移 1mol 电子,石墨电极上可回收 7gLi
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学中下列各物质间不能实现 (“→”表示一步完成)转化的是( )
(“→”表示一步完成)转化的是( )
A | B | C | D | |
a | CH3COOH |
| Cl2 | C |
b | CH3CHO | CH3CH2Br | HClO | CO |
c | CH3CH2OH | CH3CH2OH | HCl | CO2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A2+B2=2AB的反应历程可以看作如下(△H表示该过程的能量变化):
Ⅰ.A2=A+A △H1
Ⅱ.B2=B+B △H2
Ⅲ.A+B=AB △H3
则下列说法中正确的是
A. 当△H3+(△H1+△H2)>0时,该反应是吸热反应
B. 当2△H3+(△H1+△H2)>0时,该反应是放热反应
C. 当2△H3+(△H1+△H2)<0时,该反应是放热反应
D. 当△H3+(△H1+△H2)<0时,该反应是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)1.01×105Pa、0℃时气态单质Xn的密度为d g/L,则X的相对原子质量为________。
(2)NO和O2可发生反应:2NO+O2=2NO2,现有amolNO和bmolO2充分反应后氮原子与氧原子的个数比为_____。
(3)已知铝的相对原子质量为27,若阿伏加德罗常数取6.02×1023mol-1,则可估算一个铝原子的质量约为________g。
(4)设NA为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,那么c g氧气在标准状况下的体积约是______(用含NA的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓硫酸是常用的干燥剂,根据需要可将浓硫酸配成不同浓度的稀硫酸。回答下列问题:
(1)1L 0.5mol/L的H2SO4溶液中含有H2SO4 __________g,含有H+___________个,其电离方程式为__________________,将此溶液与足量的铝片反应,生成的气体在标准状况下体积为__________L,反应的离子方程式为_______________________。
(2)配制上述稀硫酸需要量取质量分数为98%,密度为1.84g/cm3的浓硫酸_______mL(结果保留一位小数)。配制此溶液需要的玻璃仪器除了烧杯、玻璃棒、胶头滴管外还需要__________。
(3)稀释浓硫酸的操作是__________________________________________________。
(4)下列操作使配制的硫酸溶液的物质的量浓度偏小的是_______________。
A.稀释浓硫酸时有液体溅出
B.容量瓶中有少量蒸馏水残留
C.浓硫酸稀释后溶液没有冷却到室温就转移
D.向容量瓶加水定容时仰视刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com