
【题目】丙烯是基本的有机化工原料,由丙烯经如下步骤可合成N异丙基丙烯酰胺,其可用于合成随温度变化的药物控制释放材料。
![]()
(1)丙烯的结构简式为___。
(2)反应Ⅰ的反应类型为___。
(3)反应Ⅱ___(填“能”或“不能”)用酸性KMnO4溶液作为氧化剂,理由是___。
(4)检验生成的B中是否含有A的方法是___;写出有关反应的化学方程式:___。
(5)M与A互称为同系物,相对分子质量比A大14,写出M所有可能的结构简式___。
(6)以B的钠盐作单体可以制成强吸水性树脂N,N属于___(填“线型”或“体型”)高分子材料,N的结构简式可表示为___。
(7)反应Ⅲ的另一种反应物的结构简式为___。
【答案】CH2=CHCH3 氧化反应 不能 酸性KMnO4溶液会将碳碳双键氧化 取适量生成的B先与一定量的NaOH溶液充分混合,再与适量新制氢氧化铜悬浊液共热,若产生砖红色沉淀,说明含有A,否则不含 CH2=CHCHO+2Cu(OH)2+NaOH![]() CH2=CHCOONa+Cu2O↓+3H2O
CH2=CHCOONa+Cu2O↓+3H2O 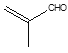 、
、![]() 、
、![]() 线型
线型 ![]()
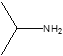
【解析】
丙烯的结构为CH2=CHCH3,发生反应Ⅰ后生成A(CH2=CHCHO),因此反应Ⅰ即氧化反应;A再发生氧化反应生成B(CH2=CHCOOH),由于A中除醛基外还含有碳碳双键,因此在转化醛基时,要选择合适的氧化剂,防止碳碳双键也发生反应;最后由B生成C,对比C和B的结构差异,推测反应Ⅲ为取代反应,可能是B(CH2=CHCOOH)和2-丙胺在催化剂的作用下发生的反应。
(1)丙烯的结构简式即为CH2=CHCH3;
(2)通过分析可知,反应Ⅰ的反应类型为氧化反应;
(3)碳碳双键也可被酸性高锰酸钾溶液氧化,因此由A制备B的过程中,为了防止碳碳双键被氧化,不能选用酸性高锰酸钾溶液做氧化剂;
(4)A的结构中含有醛基,而B中没有,因此检验是否含有醛基即可;先将B与一定量的NaOH溶液混合,中和掉羧基,再加入适量的新制Cu(OH)2悬浊液,加热观察现象,若有砖红色沉淀出现,则含有A,若无则不含A;相关的方程式为:CH2=CHCHO+2Cu(OH)2+NaOH![]() CH2=CHCOONa+Cu2O↓+3H2O;
CH2=CHCOONa+Cu2O↓+3H2O;
(5)由题可知,M的分子式比A的分子式中的碳原子数多1,M与A是同系物,所以M的结构可能有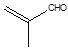 ,
,![]() ,
,![]() 三种;
三种;
(6)由题可知,N的结构为![]() ,属于线型高分子材料;
,属于线型高分子材料;
(7)通过分析可知,反应Ⅲ的另一种反应物为2-丙胺,结构简式为 。
。


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:
【题目】A、B是两种有刺激气味的气体。试根据下列实验事实填空。
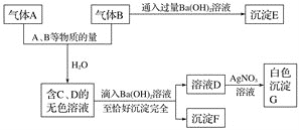
(1)写出A~F各物质的化学式:
A__________、B__________、C__________、D__________、E__________、F__________。
(2)写出A、B跟水反应的离子方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟基化合物在香料中占有重要的地位,下面所列的是一些天然的或合成的这类香料:
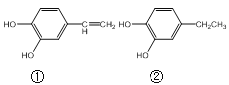

则下列说法正确的是( )
A.①与溴水反应后,溴水褪色说明分子中含有碳碳双键
B.③④相对质量相同,所以它们的质谱图相同
C.等物质的量的上述物质与足量的Na反应,产生氢气的量相同
D.1mol②与足量的溴水反应,消耗3molBr2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在处理废水时某反应体系中有6种粒子:N2、HCO3-、ClO-、CNO-、H2O、Cl-,在反应过程中部分离子浓度与反应进程关系如图所示。下列有关该反应的说法正确的是( )

A. 在上述反应体系中,CNO-是氧化剂
B. 还原产物与氧化产物的物质的量之比为1∶3
C. 在标准状况下,产生4.48 L N2时转移0.8 mol电子
D. 上述反应中,只有两种元素化合价发生了变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学探究Cu与NO的反应,查阅资料:①Cu与NO反应可生成CuO和N2,②酸性条件下,NO或NO2–都能与MnO4–反应生成NO3–和Mn2+
(1)实验室利用Cu和稀HNO3制备NO,写出反应的化学方程式_____________。
(2)选用如图所示装置完成Cu与NO的实验。(夹持装置略) 实验开始前,向装置中通入一段时间的N2。回答下列问题:
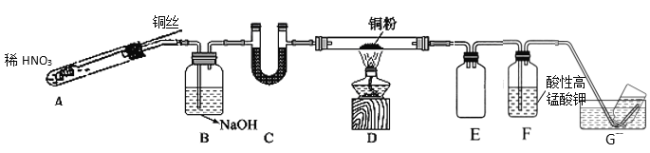
①使用铜丝的优点是_____________________装置E的作用为_______________。
②装置C中盛放的药品可能是_________;
③装置D中的现象是_______________;装置F中反应的离子方程式是_______________。
(3)测定NaNO2和NaNO3 混合溶液中NaNO2的浓度。 取25.00mL混合溶液于锥形瓶中,用0.1000mol·L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液体积/mL | 20.90 | 20.12 | 20.00 | 19.88 |
①第一次实验数据出现异常,造成这种异常的原因可能是_________(填字母代号)。
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
d.酸性KMnO4溶液中含有其他氧化性试剂
e.锥形瓶洗净后用待测液润洗
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为___________________。
③NaNO2 的物质的量浓度为__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用软锰矿![]() 主要成分为
主要成分为![]() ,另含少量铁,钙,铜等金属化合物
,另含少量铁,钙,铜等金属化合物![]() 作脱硫剂,通过如下简化流程,既脱除燃煤尾气中的
作脱硫剂,通过如下简化流程,既脱除燃煤尾气中的![]() ,又制得电池材料
,又制得电池材料![]() 反应条件已省略
反应条件已省略![]()
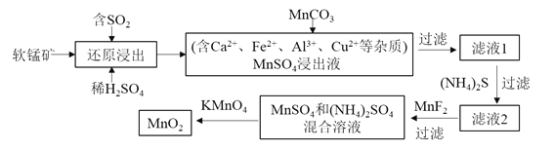
请回答下列问题:
![]() 上述还原浸出是脱硫过程,实现了 ______
上述还原浸出是脱硫过程,实现了 ______ ![]() 选填编号
选填编号![]() .
.
![]() 废气物的综合利用
废气物的综合利用
![]() 臭氧层空洞的减少
臭氧层空洞的减少
![]() 白色污染的减少
白色污染的减少
![]() 酸雨的减少
酸雨的减少
![]() 写出上述软锰矿经还原浸出生成
写出上述软锰矿经还原浸出生成![]() 的化学方程式是 ______ .
的化学方程式是 ______ .
![]() 用
用![]() 能除去还原浸出液中的
能除去还原浸出液中的![]() ,请用离子方程式解释其原因是 ______ .
,请用离子方程式解释其原因是 ______ .
![]() 加入
加入![]() 的目的主要是除去 ______ ;加入
的目的主要是除去 ______ ;加入![]() 的目的主要是除去 ______ ;
的目的主要是除去 ______ ;![]() 填离子符号
填离子符号![]()
![]() 下列各组试剂中,能准确测定一定体积燃煤尾气中
下列各组试剂中,能准确测定一定体积燃煤尾气中![]() 含量的是 ______
含量的是 ______ ![]() 填编号
填编号![]()
a.NaOH溶液、石蕊试液
b.稀![]() 酸化的
酸化的![]() 溶液
溶液
c.碘水、淀粉溶液
d.氨水、石蕊试液
![]() 用电化学法模拟工业处理
用电化学法模拟工业处理![]() 将硫酸工业尾气中的
将硫酸工业尾气中的![]() 通入如图装置
通入如图装置![]() 电均为惰性材料
电均为惰性材料![]() 进行实验,可用于制备硫酸,同时获得电能:
进行实验,可用于制备硫酸,同时获得电能:
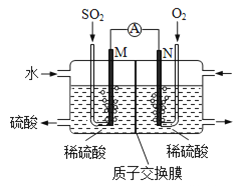
![]() 极发生的电极反应式为 ______ .
极发生的电极反应式为 ______ .
![]() 若使该装置的电流强度达到
若使该装置的电流强度达到![]() ,理论上每分钟应向负极通入标准状况下气体的体积为 ______
,理论上每分钟应向负极通入标准状况下气体的体积为 ______ ![]() 保留3位小数,已知:1个
保留3位小数,已知:1个![]() 所带电量为
所带电量为![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)4个碳原子间均以单键结合的方式有4种,请在下面的方框中补充另外3种结合方式:________________

(2)写出碳原子数为5的烷烃的同分异构体的结构简式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据实验操作和现象所得出的结论正确的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 等体积 | 相同时间内 |
|
B | 将湿润的淀粉- | 试纸只在 | 氧化性: |
C | 将光亮的镁条放入盛有 | 有大量气泡产生 | 生成的气体是 |
D | 向NaHCO3溶液中加入NaAlO2溶液 | 有白色沉淀生成 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下。

已知:![]() +CH3Cl
+CH3Cl![]() +HCl
+HCl
请回答下列问题:
(1)F的化学名称是__,②的反应类型是___。
(2)D中含有的官能团是__(写名称),D聚合生成高分子化合物的结构简式为___。
(3)反应③的化学方程式是___。
(4)反应⑥的化学方程式是___。
(5)芳香化合物N是A的同分异构体,其中核磁共振氢谱为三组峰的结构简式为___。
(6)参照有机物W的上述合成路线,设计以M为起始原料制备F的合成路线(无机试剂任选)___。
[示例:CH3CH2OH![]() CH2=CH2
CH2=CH2![]() BrCH2CH2Br]
BrCH2CH2Br]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com