
| A.给该反应体系适当加热 | B.向反应体系中加水稀释 |
| C.向反应体系中加入适量浓盐酸 | D.将铁片换成铁粉 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
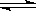 2NH3(g) (正反应放热),工业合成氨采用在500℃的条件下进行的原因是
2NH3(g) (正反应放热),工业合成氨采用在500℃的条件下进行的原因是| A.③④ | B.①② | C.①③ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
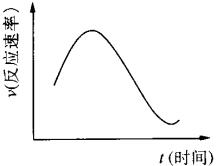
| A.①④ | B.③④ | C.①②③ | D.②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H=b的NaOH溶液10V mL时,溶液中的Cl-和Na+的物质的量相等,则a+b的值是
H=b的NaOH溶液10V mL时,溶液中的Cl-和Na+的物质的量相等,则a+b的值是 | A.13 | B.14 | C.15 | D.不能确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 ,某化学研究小组的同学分别设计了如图甲、乙、丙所示的实验。请回答相关问题:
,某化学研究小组的同学分别设计了如图甲、乙、丙所示的实验。请回答相关问题:
 ____。
____。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaOH(s) | B.KNO3 (s) | C.NaCl 水溶液 | D.NaHSO4(s) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碳酸钠溶液 | B.水 | C.硫酸钾溶液 | D.硝酸钠溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com