
| A、O2的能量一定高于SO2的能量 |
| B、2molSO2和1molO2的总能量一定高于2molSO3的总能量 |
| C、SO2的能量一定高于SO3的能量 |
| D、因该反应为放热反应,故不必加热就可发生 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、自然界中存在游离态铁 |
| B、铁在氧气中燃烧生成Fe2O3 |
| C、某些含铁的化合物可用作水处理剂 |
| D、铁红(Fe2O3)常用作红色油漆和涂料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第ⅥB族元素 |
| B、第ⅤA族元素 |
| C、镧系元素 |
| D、锕系元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.560L |
| B、1.12L |
| C、2.24L |
| D、3.36L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从溴水中提取溴可用植物油做萃取剂 |
| B、用热的纯碱溶液可区别植物油和矿物油 |
| C、含Ca2+、Mg2+的水使肥皂去污能力减弱是因为发生了沉淀反应 |
| D、生产盐酸和人造脂肪必须用氢气做原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若XY2是共价化合物,则X与Y的原子序数可能相差1 |
| B、若X与Y的原子序数相差5,则离子化合物XY2中X的离子半径比Y离子半径小 |
| C、若XY2是离子化合物,则X与Y的原子序数可能相差8 |
| D、若X与Y的原子序数相差6,则共价化合物XY2可溶于强碱溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
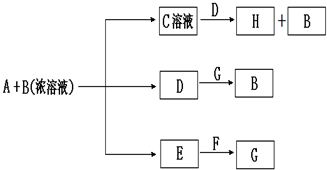
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | HA物质的量浓度 (mol/L) | NaOH物质的量浓度 (mol/L) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
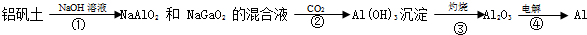
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com