
ЎҫМвДҝЎҝ№ӨТө·ПЖшЦРөД¶юСх»ҜБтәНөӘСх»ҜОпКЗҙуЖшЦчТӘОЫИҫОпЈ¬НСБтНСөӘКЗ»·ҫіЦОАнөДИИөгОКМвЎЈ»ШҙрПВБРОКМвЈә
ЈЁ1Ј©ТСЦӘөӘј°Жд»ҜәПОп·ўЙъИзПВ·ҙУҰЈә
N2(g)+O2(g)![]() 2NO(g) ҰӨH=+180kJЎӨmol-1
2NO(g) ҰӨH=+180kJЎӨmol-1
N2(g)+2O2(g)![]() 2NO2(g) ҰӨH=+68kJЎӨmol-1
2NO2(g) ҰӨH=+68kJЎӨmol-1
Фт2NO(g)+O2(g)![]() 2NO2(g)ҰӨH___kJЎӨmol-1ЎЈ
2NO2(g)ҰӨH___kJЎӨmol-1ЎЈ
ЈЁ2Ј©АыУГKMnO4НСіэ¶юСх»ҜБтөДАлЧУ·ҪіМКҪОӘЈә___
ўЩЎхMnO![]() +ЎхSO2+ЎхH2O
+ЎхSO2+ЎхH2O![]() ЎхMnO
ЎхMnO![]() +Ўх +Ўх ЎЈЈЁФЪЎ°ЎхЎұАпМоИлПөКэЈ¬ФЪЎ°__ЎұЙПМоИлОўБЈ·ыәЕЈ©
+Ўх +Ўх ЎЈЈЁФЪЎ°ЎхЎұАпМоИлПөКэЈ¬ФЪЎ°__ЎұЙПМоИлОўБЈ·ыәЕЈ©
ўЪФЪЙПКц·ҙУҰЦРјУИлCaCO3ҝЙТФМбёЯSO2ИҘіэВКЈ¬ФӯТтКЗ___ЎЈ
ЈЁ3Ј©CaSO3УлNa2SO4»мәПҪ¬ТәҝЙУГУЪНСіэNO2Ј¬·ҙУҰ№эіМОӘЈә
I.CaSO3(s)+SO![]() (aq)
(aq)![]() CaSO4(s)+SO
CaSO4(s)+SO![]() (aq)
(aq)
II.SO![]() (aq)+2NO2(g)+H2O(l)
(aq)+2NO2(g)+H2O(l)![]() SO
SO![]() (aq)+2NO
(aq)+2NO![]() (aq)+2H+(aq)
(aq)+2H+(aq)
Ҫ¬ТәЦРCaSO3ЦКБҝТ»¶ЁКұЈ¬Na2SO4өДЦКБҝУлNO2өДИҘіэВКұд»ҜЗчКЖИзНјЛщКҫЎЈ

aөгәуNO2ИҘіэВКҪөөНөДФӯТтКЗ___ЎЈ
ЈЁ4Ј©јмІвСМөАЖшЦРNOxә¬БҝөДІҪЦиИзПВЈә
I.Ҫ«VLЖшСщНЁИлККБҝЛб»ҜөДH2O2ИЬТәЦРЈ¬К№NOxНкИ«ұ»Сх»ҜОӘNO![]() Ј»
Ј»
II.јУЛ®ПЎКНЦБ100.00mLЈ¬БҝИЎ20.00mLёГИЬТәЈ¬УлV1mLc1molЎӨL-1FeSO4ұкЧјИЬТәЈЁ№эБҝЈ©ід·Ц»мәПЈ»
III.УГc2molЎӨL-1KMnO4ұкЧјИЬТәөО¶ЁКЈУаөДFe2+Ј¬ЦХөгКұПыәДV2mLЎЈ
ўЩNOұ»H2O2Сх»ҜОӘNO![]() өДАлЧУ·ҪіМКҪОӘ___ЎЈ
өДАлЧУ·ҪіМКҪОӘ___ЎЈ
ўЪөО¶Ё№эіМЦРЦчТӘК№УГөДІЈБ§ТЗЖчУР___әНЧ¶РОЖҝөИЎЈ
ўЫөО¶Ё№эіМЦР·ўЙъПВБР·ҙУҰЈә
3Fe2++NO+4H+=NOЎь+3Fe3++2H2O
MnO![]() +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O
СМЖшЖшСщЦРNOxХЫәПіЙNO2өДә¬БҝОӘ__mgЎӨm-3ЎЈ
Ўҫҙр°ёЎҝ-112 2MnO4-+1SO2+2H2O![]() 2MnO42-+ SO42-+4H+ CaCO3УлH+ЧчУГЈ¬c(H+)ПВҪөЈ¬Н¬КұЙъіЙөДCa2+УлSO42-ҪбәПЙъіЙCaSO4К№өГc(SO42-)ПВҪөЖҪәвХэПтТЖ¶ҜЈ¬ҙУ¶шМбёЯSO2өДИҘіэВК aөгәуc(SO42-)№эёЯКұЈ¬ТФ·ҙУҰIIЖҪәвөДДжПтТЖ¶ҜОӘЦчЈ¬NO2ИҘіэВКҪөөН 2NO+3H2O2=2NO3-+2H++2H2O ЛбКҪөО¶Ё№Ь
2MnO42-+ SO42-+4H+ CaCO3УлH+ЧчУГЈ¬c(H+)ПВҪөЈ¬Н¬КұЙъіЙөДCa2+УлSO42-ҪбәПЙъіЙCaSO4К№өГc(SO42-)ПВҪөЖҪәвХэПтТЖ¶ҜЈ¬ҙУ¶шМбёЯSO2өДИҘіэВК aөгәуc(SO42-)№эёЯКұЈ¬ТФ·ҙУҰIIЖҪәвөДДжПтТЖ¶ҜОӘЦчЈ¬NO2ИҘіэВКҪөөН 2NO+3H2O2=2NO3-+2H++2H2O ЛбКҪөО¶Ё№Ь ![]()
ЎҫҪвОцЎҝ
ЈЁ1Ј©УЙёЗЛ№¶ЁВЙјЖЛгҝЙөГЈ»
ЈЁ2Ј©ўЩ¶юСх»ҜБтУлёЯГМЛбјШИЬТә·ўЙъСх»Ҝ»№Фӯ·ҙУҰЙъіЙГМЛбГМЎўБтЛбјШЎўБтЛбәНЛ®Ј»
ўЪПт·ҙУҰЦРјУИлCaCO3Ј¬CaCO3Ул·ҙУҰЙъіЙөДH+әНSO42-·ҙУҰЈ¬К№H+әНSO42-өДЕЁ¶ИјхРЎЈ¬К№ЖҪәвПтХэ·ҙУҰ·ҪПтТЖ¶ҜЈ»
ЈЁ3Ј©УЙ·ҙУҰIIҝЙЦӘЈ¬ИфБтЛбёщЕЁ¶И№эҙуЈ¬ЖҪәвПтДж·ҙУҰ·ҪПтТЖ¶ҜЈ¬¶юСх»ҜөӘөДЕЁ¶ИФцҙуЈ»
ЈЁ4Ј©ўЩТ»Сх»ҜөӘУл№эСх»ҜЗв·ўЙъСх»Ҝ»№Фӯ·ҙУҰЙъіЙПхЛбәНЛ®Ј»
ўЪKMnO4ұкЧјИЬТәҫЯУРЗҝСх»ҜРФЈ¬»бёҜКҙПрҪә№ЬЈ»
ўЫУЙөГК§өзЧУКэДҝКШәгәНөӘФӯЧУёцКэКШәгјЖЛгҝЙөГЎЈ
ЈЁ1Ј©Ҫ«ТСЦӘ·ҙУҰТАҙОұаәЕОӘўЩўЪЈ¬УЙёЗЛ№¶ЁВЙҝЙЦӘЈ¬ўЪЎӘўЩөГТ»Сх»ҜөӘУлСхЖш·ҙУҰөДИИ»ҜС§·ҪіМКҪ2NO(g)+O2(g)![]() 2NO2(g)Ј¬ФтҰӨH=ЈЁ+68kJЎӨmol-1Ј©ЎӘЈЁ+180kJЎӨmol-1Ј©=-112 kJЎӨmol-1Ј¬№Кҙр°ёОӘЈә-112Ј»
2NO2(g)Ј¬ФтҰӨH=ЈЁ+68kJЎӨmol-1Ј©ЎӘЈЁ+180kJЎӨmol-1Ј©=-112 kJЎӨmol-1Ј¬№Кҙр°ёОӘЈә-112Ј»
ЈЁ2Ј©ўЩ¶юСх»ҜБтҫЯУР»№ФӯРФЈ¬ёЯГМЛбјШИЬТәҫЯУРЗҝСх»ҜРФЈ¬¶юСх»ҜБтУлёЯГМЛбјШИЬТә·ўЙъСх»Ҝ»№Фӯ·ҙУҰЙъіЙГМЛбГМЎўБтЛбјШЎўБтЛбәНЛ®Ј¬ФтЕдЖҪөДАлЧУ·ҪіМКҪОӘ2MnO4-+1SO2+2H2O![]() 2MnO42-+SO42-+4H+Ј¬№Кҙр°ёОӘЈә2MnO4-+1SO2+2H2O
2MnO42-+SO42-+4H+Ј¬№Кҙр°ёОӘЈә2MnO4-+1SO2+2H2O![]() 2MnO42-+SO42-+4H+Ј»
2MnO42-+SO42-+4H+Ј»
ўЪПт·ҙУҰЦРјУИлCaCO3Ј¬CaCO3Ул·ҙУҰЙъіЙөДH+әНSO42-·ҙУҰЈ¬К№H+әНSO42-өДЕЁ¶ИјхРЎЈ¬К№ЖҪәвПтХэ·ҙУҰ·ҪПтТЖ¶ҜЈ¬ҙУ¶шҝЙТФМбёЯSO2ИҘіэВКЈ¬№Кҙр°ёОӘЈәCaCO3УлH+ЧчУГЈ¬c(H+)ПВҪөЈ¬Н¬КұЙъіЙөДCa2+УлSO42ЎӘҪбәПЙъіЙCaSO4К№өГc(SO42-)ПВҪөЖҪәвХэПтТЖ¶ҜЈ¬ҙУ¶шМбёЯSO2өДИҘіэВКЈ»
ЈЁ3Ј©УЙ·ҙУҰIIҝЙЦӘЈ¬ИфБтЛбёщЕЁ¶И№эҙуЈ¬ЖҪәвПтДж·ҙУҰ·ҪПтТЖ¶ҜЈ¬¶юСх»ҜөӘөДЕЁ¶ИФцҙуЈ¬ИҘіэВКПВҪөЈ¬№Кҙр°ёОӘЈәaөгәуc(SO42-)№эёЯКұЈ¬ТФ·ҙУҰIIЖҪәвөДДжПтТЖ¶ҜОӘЦчЈ¬NO2ИҘіэВКҪөөНЈ»
ЈЁ4Ј©ўЩТ»Сх»ҜөӘҫЯУР»№ФӯРФЈ¬№эСх»ҜЗвҫЯУРСх»ҜРФЈ¬Т»Сх»ҜөӘУл№эСх»ҜЗв·ўЙъСх»Ҝ»№Фӯ·ҙУҰЙъіЙПхЛбәНЛ®Ј¬·ҙУҰөДАлЧУ·ҪіМКҪОӘ2NO+3H2O2=2NO3-+2H++2H2OЈ¬№Кҙр°ёОӘЈә2NO+3H2O2=2NO3-+2H++2H2OЈ»
ўЪKMnO4ұкЧјИЬТәҫЯУРЗҝСх»ҜРФЈ¬»бёҜКҙПрҪә№ЬЈ¬ЛщТФөО¶Ё№эіМЦРУҰСЎУГЛбКҪөО¶Ё№ЬЈ¬№Кҙр°ёОӘЈәЛбКҪөО¶Ё№ЬЈ»
ўЫУЙөГК§өзЧУКэДҝКШәгҝЙөГЈәn(Fe2+)= 3n(NO3-)+5n(MnO4-)Ј¬n(NO3-)=![]() Ј¬УЙөӘФӯЧУёцКэКШәгҝЙЦӘn(NO2)= n(NO3-)=
Ј¬УЙөӘФӯЧУёцКэКШәгҝЙЦӘn(NO2)= n(NO3-)=![]() molЈ¬ФтСМЖшЖшСщЦРNOxХЫәПіЙNO2өДә¬БҝОӘ
molЈ¬ФтСМЖшЖшСщЦРNOxХЫәПіЙNO2өДә¬БҝОӘ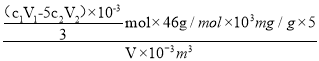 =
=![]() mgЎӨm-3Ј¬№Кҙр°ёОӘЈә
mgЎӨm-3Ј¬№Кҙр°ёОӘЈә![]() ЎЈ
ЎЈ


 КАјН°ЩНЁЦчМеҝОМГРЎС§ҝОКұН¬ІҪҙпұкПөБРҙр°ё
КАјН°ЩНЁЦчМеҝОМГРЎС§ҝОКұН¬ІҪҙпұкПөБРҙр°ё
| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ CO2өДЧКФҙ»ҜАыУГТ»ЦұКЗ»ҜС§јТГЗ№ШЧўөДЦШТӘҝОМвЈ¬ЦРҝЖФәҙуБ¬»ҜС§ОпАнСРҫҝЛщЙијЖБЛТ»ЦЦРВРН¶а№ҰДЬёҙәПҙЯ»ҜјБЈ¬іЙ№ҰөШКөПЦБЛCO2ЦұҪУјУЗвЦЖИЎёЯРБНйЦөЖыУНЈә![]() (·ҙУҰўЩ)Ј¬ёГСРҫҝіЙ№ыұ»ЖАјЫОӘЎ°CO2ҙЯ»ҜЧӘ»ҜБмУтөДН»ЖЖРФҪшХ№ЎұЎЈ
(·ҙУҰўЩ)Ј¬ёГСРҫҝіЙ№ыұ»ЖАјЫОӘЎ°CO2ҙЯ»ҜЧӘ»ҜБмУтөДН»ЖЖРФҪшХ№ЎұЎЈ
(1)ТСЦӘЗвЖшөДИјЙХИИОӘ![]() Ј¬ИфТӘАыУГ
Ј¬ИфТӘАыУГ![]() өДИјЙХИИЗуaөДЦөЈ¬Фт»№РиТӘЦӘөАТ»ёц·ҙУҰөД
өДИјЙХИИЗуaөДЦөЈ¬Фт»№РиТӘЦӘөАТ»ёц·ҙУҰөД![]() Ј¬ёГ·ҙУҰКЗ________________________________ЎЈ·ҙУҰўЩФЪТ»¶ЁМхјюПВҫЯУРЧФ·ўРФЈ¬Фтa_______________0(МоЎ°>Ўұ»тЎ°<Ўұ)ЎЈ
Ј¬ёГ·ҙУҰКЗ________________________________ЎЈ·ҙУҰўЩФЪТ»¶ЁМхјюПВҫЯУРЧФ·ўРФЈ¬Фтa_______________0(МоЎ°>Ўұ»тЎ°<Ўұ)ЎЈ
(2)ПтДіГЬұХИЭЖчЦР°ҙТ»¶ЁН¶БПұИідИл![]() Ўў
Ўў![]() Ј¬ҝШЦЖМхјюК№Жд·ўЙъ·ҙУҰЈә
Ј¬ҝШЦЖМхјюК№Жд·ўЙъ·ҙУҰЈә![]() ЎЈІвөГ
ЎЈІвөГ![]() өДЖҪәвЧӘ»ҜВКУлОВ¶ИЎўС№ЗҝЦ®јдөД№ШПөИзНј1ЛщКҫЈә
өДЖҪәвЧӘ»ҜВКУлОВ¶ИЎўС№ЗҝЦ®јдөД№ШПөИзНј1ЛщКҫЈә
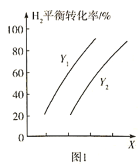
ФтXұнКҫ______________Ј¬![]() ___________
___________![]() (МоЎ°>Ўұ»тЎ°<Ўұ)ЎЈУыМбёЯ
(МоЎ°>Ўұ»тЎ°<Ўұ)ЎЈУыМбёЯ![]() өДЖҪәвЧӘ»ҜВКІўМбёЯөҘО»КұјдДЪ
өДЖҪәвЧӘ»ҜВКІўМбёЯөҘО»КұјдДЪ![]() өДІъБҝЈ¬ҝЙІЙИЎөДҙлК©КЗ______________________(МоБҪЦЦ)ЎЈ
өДІъБҝЈ¬ҝЙІЙИЎөДҙлК©КЗ______________________(МоБҪЦЦ)ЎЈ
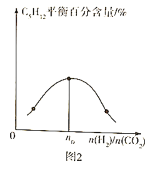
(3)ҝШЦЖТ»¶ЁОВ¶ИЎўҙЯ»ҜјБЈ¬°ҙІ»Н¬Н¶БПұИ![]() Ҫ«·ҙУҰОпНЁИлөҪДіГЬұХИЭЖчЦРЈ¬ІвөГЖҪәвКұ
Ҫ«·ҙУҰОпНЁИлөҪДіГЬұХИЭЖчЦРЈ¬ІвөГЖҪәвКұ![]() өД°Щ·Цә¬БҝУлН¶БПұИЦ®јдөД№ШПөИзНј2ЛщКҫЈ¬Фт
өД°Щ·Цә¬БҝУлН¶БПұИЦ®јдөД№ШПөИзНј2ЛщКҫЈ¬Фт![]() ____________ЎЈ
____________ЎЈ
(4)ФЪоЙ-ооЛ«ҪрКфҙЯ»ҜјБөДЧчУГПВЈ¬CH3OHЎўCO2ЎўH2ҝЙёЯР§өШЧӘ»ҜОӘТТЛбЈ¬·ҙУҰ·ҪіМКҪОӘ![]() ЎЈТ»¶ЁОВ¶ИПВЈ¬ПтДіёХРФИЭЖчЦРНЁИлөИОпЦКөДБҝөДИэЦЦФӯБПЖшЈ¬ІвөГМеПөЦРөДЧЬС№ЗҝУлКұјдөД№ШПөИзПВұнЛщКҫЈә
ЎЈТ»¶ЁОВ¶ИПВЈ¬ПтДіёХРФИЭЖчЦРНЁИлөИОпЦКөДБҝөДИэЦЦФӯБПЖшЈ¬ІвөГМеПөЦРөДЧЬС№ЗҝУлКұјдөД№ШПөИзПВұнЛщКҫЈә
t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
p/kPa | 3 | 2.7 | 2.5 | 2.35 | 2.26 | 2.2 | 2.2 |
Фт·ҙУҰҝӘКјөҪҙпөҪЖҪәвөД№эіМЦРЈ¬![]() ______________
______________![]() ______________
______________![]() ЎЈ
ЎЈ
(5)МјІ¶ЧҪјјКхөД·ўХ№ТІУРАыУЪCO2ФЪЧКФҙУҰУГ·ҪГжөГөҪід·ЦАыУГЎЈіЈОВПВЈ¬ИфДіҙОУГNaOHИЬТәІ¶ЧҪҝХЖшЦРөДCO2ЛщөГИЬТәөДpH=10Ј¬ІўІвөГИЬТәЦР![]() Ј¬Фт
Ј¬Фт![]() _____________
_____________![]() ЎЈ
ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝОТ№ъУөУРЧФЦчЦӘК¶ІъИЁөДпЁ(Rb)ФӯЧУЦУЈ¬Гҝ3000НтДкОуІоҪц1ГлЎЈRbКЗөЪОеЦЬЖЪөЪўсAЧеФӘЛШЈ¬ПВБР№ШУЪ37RbөДЛө·ЁХэИ·өДКЗЈЁ Ј©
A.ФӘЛШөДҪрКфРФЈәKЈҫRb
B.ЦРЧУКэОӘ50өДRbөДәЛЛШЈә![]() Rb
Rb
C.УлН¬ЦЬЖЪФӘЛШ53IөДФӯЧУ°лҫ¶ұИЈәRbЈјI
D.ЧоёЯјЫСх»ҜОп¶ФУҰөДЛ®»ҜОпөДјоРФЈәKOHЈјRbOH
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝөвФЪҝЖСРУлЙъ»оЦРУРЦШТӘУҰУГЎЈДіРЛИӨРЎЧйУГ0.2 %өн·ЫИЬТәЎў0.50 molЎӨLЈӯ1KIЎў0.20 molЎӨLЈӯ1K2S2O8Ўў0.10 molЎӨLЈӯ1Na2S2O3өИКФјБЈ¬МҪҫҝ·ҙУҰМхјю¶Ф»ҜС§·ҙУҰЛЩВКөДУ°ПмЎЈТСЦӘЈәS2O82-Ј«2IЈӯ=2SO42-Ј«I2(Вэ) I2Ј«2 S2O32-=2IЈӯЈ«S4O62-(ҝм)
ЈЁ1Ј©ОӘМҪҫҝ·ҙУҰОпЕЁ¶И¶Ф»ҜС§·ҙУҰЛЩВКөДУ°ПмЈ¬ЙијЖөДКөСй·Ҫ°ёИзПВұнЈә
КөСйРтәЕ | Ме»эV/mL | ||||
K2S2O8ИЬТә | Л® | KIИЬТә | Na2S2O3ИЬТә | өн·ЫИЬТә | |
10.0 | 0.0 | 4.0 | 4.0 | 2.0 | |
9.0 | 1.0 | 4.0 | 4.0 | 2.0 | |
8.0 | V8 | 4.0 | 4.0 | 2.0 | |
ұнКҫV8ЈҪ________mLЈ¬АнУЙКЗ__________________ЎЈ
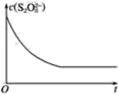
ЈЁ2Ј©ТСЦӘДіМхјюПВЈ¬ЕЁ¶Иc(S2O82-)Јӯ·ҙУҰКұјдtөДұд»ҜЗъПЯИзНјЛщКҫЈ¬ИфұЈіЦЖдЛыМхјюІ»ұдЈ¬ЗлФЪЧшұкНјЦРЈ¬·Цұр»ӯіцҪөөН·ҙУҰОВ¶ИәНјУИлҙЯ»ҜјБКұc(S2O82-)ЈӯtөДұд»ҜЗъПЯКҫТвНј(ҪшРРПаУҰөДұкЧў)ЎЈ_________
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝіЈОВПВЈ¬Ҫ«Т»¶ЁЕЁ¶ИөДСОЛбәНҙЧЛбјУЛ®ПЎКНЈ¬ИЬТәөДөјөзДЬБҰЛжИЬТәМе»эұд»ҜөДЗъПЯИзНјЛщКҫЎЈПВБРЛө·ЁЦРХэИ·өДКЗЈЁ Ј©
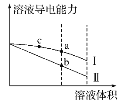
A.БҪИЬТәПЎКНЗ°өДЕЁ¶ИПаН¬
B.aЎўbЎўcИэөгИЬТәөДpHУЙҙуөҪРЎЛіРтОӘaЈҫbЈҫc
C.aөгөДKwЦөұИbөгөДKwЦөҙу
D.aөгЛ®өзАлөДc(HЈ«)ҙуУЪcөгЛ®өзАлөДc(HЈ«)
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ·Цұр°ҙПВНјјЧЎўТТЛщКҫЧ°ЦГҪшРРКөСйЈ¬НјЦРБҪёцЙХұӯАпөДИЬТәОӘН¬ЕЁ¶ИөДПЎБтЛбЈ¬ТТЦРAОӘөзБчұнЎЈЗл»ШҙрПВБРОКМвЈә
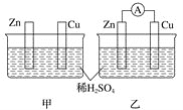
(1)ТФПВРрКцЦРЈ¬ХэИ·өДКЗ_______________(МоЧЦДё)ЎЈ
AЈ®јЧЦРРҝЖ¬КЗёәј«Ј¬ТТЦРНӯЖ¬КЗХэј«
BЈ®БҪЙХұӯЦРНӯЖ¬ұнГжҫщУРЖшЕЭІъЙъ
CЈ®БҪЙХұӯЦРИЬТәpHҫщФцҙу
DЈ®ІъЙъЖшЕЭөДЛЩ¶ИјЧЦРұИТТЦРВэ
EЈ®ТТөДНвөзВ·ЦРөзБч·ҪПтZnЎъCu
FЈ®ТТИЬТәЦР![]() ПтНӯЖ¬·ҪПтТЖ¶Ҝ
ПтНӯЖ¬·ҪПтТЖ¶Ҝ
(2)ұд»Ҝ№эіМЦРДЬБҝЧӘ»ҜөДЦчТӘРОКҪЈәјЧОӘ___________Ј»ТТОӘ______ЎЈ
(3)ФЪТТКөСйЦРЈ¬ДіН¬С§·ўПЦІ»ҪцФЪНӯЖ¬ЙПУРЖшЕЭІъЙъЈ¬¶шЗТФЪРҝЖ¬ЙПТІІъЙъБЛЖшМеЈ¬·ЦОцФӯТтҝЙДЬКЗ___ЎЈ
(4)ФЪТТКөСйЦРЈ¬Из№ы°СБтЛб»»іЙБтЛбНӯИЬТәЈ¬ЗлРҙіцНӯөзј«өДөзј«·ҙУҰ·ҪіМКҪј°ЧЬ·ҙУҰАлЧУ·ҪіМКҪЈәНӯөзј«Јә____Ј¬ЧЬ·ҙУҰЈә___ЎЈөұөзВ·ЦРЧӘТЖ0.25 molөзЧУКұЈ¬ПыәДёәј«ІДБПөДЦКБҝОӘ_____g(ZnөДПа¶ФФӯЧУЦКБҝ65)ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝФЪ100ЎжКұЈ¬Ҫ«0.200 molөДЛДСх»Ҝ¶юөӘЖшМеідИл2 LХжҝХөДГЬұХИЭЖчЦРЈ¬ГҝёфТ»¶ЁөДКұјд¶ФёГИЭЖчДЪөДОпЦКҪшРР·ЦОцЈ¬өГөҪИзПВұнёсЈә
| 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4) | 0.100 | c1 | 0.050 | c3 | a | b |
c(NO2) | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
КФМоҝХЈә
(1)ёГ·ҙУҰөД»ҜС§·ҪіМКҪОӘN2O4![]() 2NO2ЎЎЈ¬ҙпөҪЖҪәвКұЈ¬ЛДСх»Ҝ¶юөӘөДЧӘ»ҜВКОӘ__________%Ј¬ұнЦРc2________c3Ўўa______b(МоЎ°>ЎұЎўЎ°<Ўұ»тЎ°ЈҪЎұ)ЎЈ
2NO2ЎЎЈ¬ҙпөҪЖҪәвКұЈ¬ЛДСх»Ҝ¶юөӘөДЧӘ»ҜВКОӘ__________%Ј¬ұнЦРc2________c3Ўўa______b(МоЎ°>ЎұЎўЎ°<Ўұ»тЎ°ЈҪЎұ)ЎЈ
(2) 20 sКұЛДСх»Ҝ¶юөӘөДЕЁ¶Иc1ЈҪ________mol/LЈ¬ФЪ0 sЎ«20 sКұјд¶ОДЪЈ¬ЛДСх»Ҝ¶юөӘөДЖҪҫщ·ҙУҰЛЩВКОӘ________mol/(LЎӨs)ЎЈ
(3)ИфФЪПаН¬ЗйҝцПВЧоіхПтёГИЭЖчідИлөДКЗ¶юСх»ҜөӘЖшМеЈ¬ТӘҙпөҪЙПКцН¬СщөДЖҪәвЧҙМ¬Ј¬¶юСх»ҜөӘөДЖрКјЕЁ¶ИКЗ________mol/LЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝФЪДіТ»әгОВЎўәгИЭөДГЬұХИЭЖчЦР·ўЙъ·ҙУҰЈә3H2(g)+N2(g)![]() 2NH3(g)ЎЎҰӨH<0ЎЈt1КұҝМ·ҙУҰҙпөҪЖҪәвЈ¬ФЪt2КұҝМёДұдДіТ»МхјюЈ¬Жд·ҙУҰ№эіМИзНјЛщКҫЎЈПВБРЛө·ЁХэИ·өДКЗ
2NH3(g)ЎЎҰӨH<0ЎЈt1КұҝМ·ҙУҰҙпөҪЖҪәвЈ¬ФЪt2КұҝМёДұдДіТ»МхјюЈ¬Жд·ҙУҰ№эіМИзНјЛщКҫЎЈПВБРЛө·ЁХэИ·өДКЗ

A. ўсЎўўтБҪ№эіМҙпөҪЖҪәвКұЈ¬ЖҪәвіЈКэЈәKўс<Kўт
B. ўсЎўўтБҪ№эіМҙпөҪЖҪәвКұЈ¬NH3өДМе»э·ЦКэЈәўс<ўт
C. ўсЎўўтБҪ№эіМҙпөҪЖҪәвөДұкЦҫЈәЖшМеөДЖҪҫщГЬ¶ИІ»ФЩ·ўЙъұд»Ҝ
D. t2КұҝМёДұдөДМхјюҝЙТФКЗПтГЬұХИЭЖчЦРјУH2әНN2өД»мәПЖш
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТСЦӘ·ҙУҰ![]() КЗҝЙДж·ҙУҰЎЈЙијЖИзНјЧ°ЦГ(
КЗҝЙДж·ҙУҰЎЈЙијЖИзНјЧ°ЦГ(![]() ҫщОӘКҜД«өзј«)Ј¬·ЦұрҪшРРПВКцІЩЧчЈә
ҫщОӘКҜД«өзј«)Ј¬·ЦұрҪшРРПВКцІЩЧчЈә
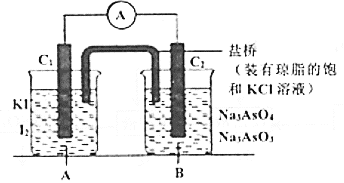
ўЩПтBЙХұӯЦРЦрөОјУИлЕЁСОЛбЎЈўЪПтBЙХұӯЦРЦрөОјУИл![]() ИЬТәЎЈҪб№ы·ўПЦөзБчұнЦёХлҫщ·ўЙъЖ«ЧӘЎЈ
ИЬТәЎЈҪб№ы·ўПЦөзБчұнЦёХлҫщ·ўЙъЖ«ЧӘЎЈ
(1)ўЩ№эіМЦР![]() °фЙП·ўЙъөД·ҙУҰОӘ_________Ј»
°фЙП·ўЙъөД·ҙУҰОӘ_________Ј»
ўЪ№эіМЦР![]() °фЙП·ўЙъөД·ҙУҰОӘ___________ЎЈ
°фЙП·ўЙъөД·ҙУҰОӘ___________ЎЈ
(2)ІЩЧчўЪ№эіМЦРЈ¬СОЗЕЦРөД![]() ТЖПт_________ЙХұӯИЬТә(МоЎ°AЎұ»тЎ°BЎұ)ЎЈ
ТЖПт_________ЙХұӯИЬТә(МоЎ°AЎұ»тЎ°BЎұ)ЎЈ
ЧКБПЈә![]() ЎЈПт
ЎЈПт![]() Т»¶ЁЕЁ¶ИөД
Т»¶ЁЕЁ¶ИөД![]() ИЬТәЦРјУИл
ИЬТәЦРјУИл![]() ИЬТәЈ¬ҙпЖҪәвәуЈ¬Па№ШОўБЈЕЁ¶ИИзПВЈә
ИЬТәЈ¬ҙпЖҪәвәуЈ¬Па№ШОўБЈЕЁ¶ИИзПВЈә
ОўБЈ |
|
|
|
ЕЁ¶И |
|
| a |
(3)a=________________ЎЈёГЖҪәвМеПөЦРіэБЛә¬УР![]() әН
әН![]() НвЈ¬ЕР¶ПИЬТәКЗ·сТ»¶Ё»№ә¬УРЖдЛыә¬өвОўБЈ______________(МоЎ°КЗЎұ»тЎ°·сЎұ)ЎЈ
НвЈ¬ЕР¶ПИЬТәКЗ·сТ»¶Ё»№ә¬УРЖдЛыә¬өвОўБЈ______________(МоЎ°КЗЎұ»тЎ°·сЎұ)ЎЈ
(4)ТСЦӘЈәјЧҙјУлЛ®ХфЖшЦШХыЦЖЗвҝЙЦұҪУУГУЪИјБПөзіШЎЈ
·ҙУҰЈә![]()
·ҙУҰЈә![]()
Фт![]() ______________
______________![]()
(5)ТСЦӘЈә25ЎжКұЈ¬![]() ЎЈТҪС§ЙПҪшРРПы»ҜПөНіөДXЙдПЯНёКУКұЈ¬іЈК№УГ
ЎЈТҪС§ЙПҪшРРПы»ҜПөНіөДXЙдПЯНёКУКұЈ¬іЈК№УГ![]() ЧчДЪ·юФмУ°јБЎЈОёЛбЛбРФәЬЗҝ(pHФјОӘ1)Ј¬ө«·юУГҙуБҝ
ЧчДЪ·юФмУ°јБЎЈОёЛбЛбРФәЬЗҝ(pHФјОӘ1)Ј¬ө«·юУГҙуБҝ![]() ИФИ»КЗ°ІИ«өДЈ¬
ИФИ»КЗ°ІИ«өДЈ¬![]() І»ИЬУЪЛбөДФӯТтКЗ(УГИЬҪвЖҪәвФӯАнҪвКН)Јә_________ЎЈОу·юЙЩБҝ
І»ИЬУЪЛбөДФӯТтКЗ(УГИЬҪвЖҪәвФӯАнҪвКН)Јә_________ЎЈОу·юЙЩБҝ![]() Ј¬УҰҫЎҝмУГҙуБҝөДТ»¶ЁЕЁ¶ИөД
Ј¬УҰҫЎҝмУГҙуБҝөДТ»¶ЁЕЁ¶ИөД![]() ИЬТәёш»јХЯПҙОёЈ¬әцВФПҙОё№эіМЦР
ИЬТәёш»јХЯПҙОёЈ¬әцВФПҙОё№эіМЦР![]() ИЬТәЕЁ¶ИөДұд»ҜЈ¬ТӘК№ІРБфФЪОёТәЦРөД
ИЬТәЕЁ¶ИөДұд»ҜЈ¬ТӘК№ІРБфФЪОёТәЦРөД![]() ЕЁ¶ИОӘ
ЕЁ¶ИОӘ![]() Ј¬УҰ·юУГөД
Ј¬УҰ·юУГөД![]() ИЬТәөДЧоөНЕЁ¶ИОӘ_______
ИЬТәөДЧоөНЕЁ¶ИОӘ_______![]() ЎЈ
ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com