
������ʵ��д�����з�Ӧ���Ȼ�ѧ����ʽ��
��1����25�桢101kPa�£�1g�״�ȼ������CO2��Һ̬ˮʱ����22.68kJ�����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ ��
��2����CH4����ԭNOx�������������������Ⱦ�����磺
CH4(g)��4NO2(g) =4NO(g)��CO2(g)��2H20(g) ��H����574 kJ��mol��1
CH4(g)��4NO(g) =2N2(g)��CO2(g)��2H2O(g) ��H����1160 kJ��mol��1
���ñ�״����4.48L CH4��ԭNO2��N2����������ת�Ƶĵ�������Ϊ (�����ӵ�������ֵ��NA��ʾ)���ų�������Ϊ__ _____kJ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ�߶���10���¿���ѧ�Ծ��������棩 ���ͣ������
��18�֣�25 ��ʱ������ƽ�ⳣ����
��ѧʽ | CH3COOH | H2CO3 | HClO | |
����ƽ�ⳣ�� | 1��8��10��5 | K1 4��3��10��7 K2 5��6��10��11 | 3��0��10��8 | |
�ش��������⣺
��1�������������ӽ�����ӵ������ɴ�С��˳����_____________�������ţ�
a��CO32- b��ClO- c��CH3COO- d��HCO3-
��2�����з�Ӧ���ܷ������ǣ� ��
a��CO32- + CH3COOH��CH3COO- + CO2 �� + H2O
b��ClO- + CH3COOH��CH3COO- + HClO
c��CO32- + HClO��CO2 �� + H2O + ClO-
d��2 ClO- + CO2 + H2O��CO32-+ 2 HclO
��3��������ˮϡ��0��10 mol��L-1�Ĵ���,�����и�ʽ��ʾ����ֵ��ˮ�������Ӷ��������_________��
A��c��CH3COOH��/c��H+�� B��c��CH3COO-��/c��CH3COOH��
C��c��H+��/ KW D��c��H+��/c��OH-��
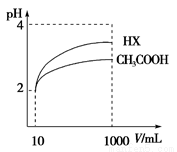
��4�����Ϊ10 mL pH��2�Ĵ�����Һ��һԪ��HX�ֱ��ˮϡ����1000mL��ϡ����pH�仯��ͼ����HX�ĵ���ƽ�ⳣ��________������ڡ��������ڡ���С�ڡ��������ƽ�ⳣ����ϡ�ͺ�HX��Һ��ˮ���������c��H����________������Һ��ˮ���������c��H����������ڡ��������ڡ���С�ڡ���
��5����20 mL���������Ļ����Һ�У���μ���0��05 mol��L��1Ba��OH��2��Һʱ�����ɳ����������仯���ɴ˶��������Һ��pH�ı仯��ͼ��ʾ�����㣺
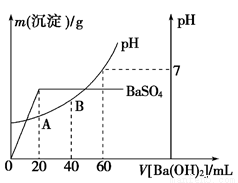
��ԭ�����Һ��c��H������___________________��c��Cl������_________________��
��A���pH��_________________��
�۽�0��15 mol��L-1ϡ����V1mL��0��1 mol��L-1NaOH��ҺV2mL���,������ҺpHΪ1,��V1��V2=
����Һ����仯���Բ��ƣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������ʡĵ�����и���9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA��ʾ�����ӵ�������ֵ��������������ȷ����
A��10 L 0.l mol?L-1��Na2CO3��Һ����������һ������3NA
B����״���£�22.4 L HF�ķ�����ΪNA
C��1 mol Fe��22.4 L��Cl2����״���£���ȼ�գ�ת�Ƶĵ�������Ϊ3NA
D��һ��������ij�ܱ�����ʢ��0.1 mol N2��0.3 mol H2����ַ�Ӧ��ת�Ƶ�����Ϊ0.6NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꼪��ʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��������������
A�����Ӱ뾶��Al3����Mg2����Na����F��
B���ȶ��ԣ�HF��HCl��HBr��HI
C�����ԣ�H4SiO4��H3PO4��H2SO4��HClO4
D�����ԣ�Al(OH)3��Mg(OH)2��Ca(OH)2��KOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꼪��ʡ�߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪ά����A�Ľṹ��ʽ���£���������˵����ȷ����
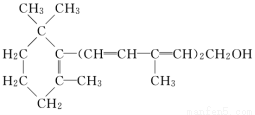
A��ά����A��һ�ִ�
B��ά����A��һ�������к�������̼̼˫��
C��ά����A��һ����������33����ԭ��
D��ά����A����ʹ���CCl4��Һ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶�9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��100g̼����ȫȼ�����������У�COռ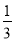 ��CO2ռ
��CO2ռ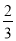 ����C(s)+
����C(s)+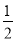 O2(g) =CO(g)����H=-110.35kJ/mol��CO(g)+
O2(g) =CO(g)����H=-110.35kJ/mol��CO(g)+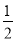 O2(g)=CO2(g)����H=-282.57 kJ/mol������Щ̼��ȫȼ����ȣ���ʧ��������
O2(g)=CO2(g)����H=-282.57 kJ/mol������Щ̼��ȫȼ����ȣ���ʧ��������
A��392.92kJ B��2489.44kJ
C��784.92kJ D��3274.3kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ�Ž�����У������һ��������ѧ�Ծ��������棩 ���ͣ������
��8�֣�þ�Ǻ�ˮ�к����϶�Ľ���Ԫ�أ�����þ��þ�Ͻ��Լ�þ�Ļ������ڿ�ѧ�о���ҵ��������;�dz��㷺��
��1��Mg2Ni��һ�ִ���Ͻ���֪��
Mg(s)+H2(g)===MgH2(s) ��H1== ��74��5kJ/mol
Mg2Ni(s)+2H2(g)===Mg2NiH4(s) ��H2== ��64��4kJ/mol
Mg2Ni(s)+2MgH2(s)===2Mg(s)+Mg2NiH4(s) ��H3
��H3== kJ/mol
��2����ҵ�Ͽ��õ�����ڵ���ˮ�Ȼ�þ���þ�������Ȼ�þ������ˮ�ǹؼ��Ĺ���֮һ��һ������������Ȼ�þ������ˮ�ķ����ǣ��Ƚ�MgCl2•6H2Oת��ΪMgCl2•NH4Cl•nNH3��Ȼ����700���Ѱ��õ���ˮ�Ȼ�þ���Ѱ���Ӧ�Ļ�ѧ����ʽΪ ���ö��Ե缫��������Ȼ�þ�������ĵ缫��ӦʽΪ ��
��3���������Mg(AlH4)2��110�橁200��ķ�ӦΪ��Mg(AlH4)2===MgH2+2Al+3H2����ÿ����27gAlת�Ƶ��ӵ����ʵ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ�����и�����ѧ�ڵڶ���������⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�˵����ȷ����
A�����ں�������ϸ���һЩͭ�飬����Լ���������ǵĸ�ʴ��
B��2NO(g)+2CO(g) N2(g)+2CO2(g)�ڳ��������Է����У���÷�Ӧ�Ħ�H>0��
N2(g)+2CO2(g)�ڳ��������Է����У���÷�Ӧ�Ħ�H>0��
C������0��1 mol��L-1 Na2CO3��Һ��CO32-ˮ��̶Ⱥ���Һ��pH������
D�������������Ҵ���������Ӧ(��H<0)����������Ũ���Ტ���ȣ��÷�Ӧ�ķ�Ӧ���ʺ�ƽ�ⳣ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ�����и�����ϰ���ϵ�һ���¿���ѧ�Ծ�A�������棩 ���ͣ�ѡ����
����ʵ�鷽���У����ܲⶨNa2CO3��NaHCO3�������Na2CO3������������
A��ȡa�˻�����ּ��ȣ�����b��
B��ȡa�˻����������ϡ�����ַ�Ӧ�����ȡ����ɡ����գ���b�˹���
C��ȡa�˻����������ϡ�����ַ�Ӧ���ݳ������ü�ʯ�����գ�����b��
D��ȡa�˻����������Ba(OH)2��Һ��ַ�Ӧ�����ˡ�ϴ�ӡ���ɣ���b�˹���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com