
【题目】Ⅰ.中和热的测定是高中重要的定量实验。取50mL 0.55mol/L的NaOH溶液与50mL 0.25mol/L的硫酸溶液置于如图所示的装置中进行中和热的测定实验,回答下列问题:

(1)仪器A的名称是____________。
(2)实验测得的数据如下表:
温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | 3.4 |
2 | 25.9 | 25.9 | 25.9 | 29.2 | |
3 | 26.4 | 26.2 | 26.3 | 29.8 | |
近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。ΔH=__________ ( 取小数点后一位)。
(3)若改用60mL 0.25mol·L-1H2SO4和50mL 0.55mol·L-1NaOH溶液进行反应与上述实验相比,所放出的热量______,若实验操作均正确,则所求中和热_____。
II、某课外活动小组拟探究H+浓度对MnO2与H2O2反应速率的影响。
(4)现取等量MnO2和下表有关物质,在相同温度下进行4组实验,分别记录收集20.0mL氧气所需时间。
实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
10%H2O2的体积/mL | 5.0 | 5.0 | V1 | V2 |
20%硫酸的体积/mL | 0 | 0.5 | 1.0 | V3 |
水的体积/mL | 15 | 14.5 | V4 | 13.5 |
所需时间t/s | t1 | t2 | t3 | t4 |
已知酸条件下时:MnO2+H2O2+2H+=Mn2++O2↑+2H2O
①实验I发生反应的化学方程式为 ________,实验II中MnO2的作________。
②上表中V1=_______mL,V3=_______mL。
③若实验测得t2>t3>t4,则可得出的实验结论是______。
【答案】环形玻璃搅拌棒 -56.8 KJ/mol 不相等 相等 2H2O2![]() 2H2O +O2↑ 氧化剂 5.0 1.5 酸浓度越大,反应速率越快
2H2O +O2↑ 氧化剂 5.0 1.5 酸浓度越大,反应速率越快
【解析】
(1)由图可以看出A为环形玻璃搅拌棒;
(2)依据中和热的计算公式:ΔH=-![]() KJ/mol,求算;
KJ/mol,求算;
(3)改用60mL 0.25mol·L-1H2SO4和50mL 0.55mol·L-1NaOH溶液进行反应,生成H2O的物质的量不同,则放出的热量不相等,由中和热的定义可知,中和热不变;
(4)①未加硫酸,二氧化锰做催化剂,H2O2发生分解反应,在有硫酸的条件下发生反应:MnO2+H2O2+2H+=Mn2++O2↑+2H2O,反应中MnO2的作氧化剂;
②因为四个实验是对比实验,都产生相同的O2,故而需要n(H2O2)相同,且要测算产生等量O2所需的时间,所以混合容易的体积应相同,保证浓度相等;
③实验测得t2>t3>t4,是Ⅱ、Ⅲ、Ⅳ三个实验中,硫酸的浓度不同造成的,由此可以得出结论。
(1)由图可以看出A为环形玻璃搅拌棒;
本题答案为:环形玻璃搅拌棒。
(2)加入的氢氧化钠和硫酸的体积都是50mL,50ml、0.55 mol/L NaOH溶液和50ml、0.25 mol/L硫酸溶液,反应中生成水的物质的量是0.025mol,因为两溶液的密度均为1 g/cm3,所以混合溶液的质量为100g,由表中数据可知:ΔH=-![]() =
= ![]() 56.8KJ/mol,
56.8KJ/mol,
本题答案为:-56.8 KJ/mol。
(3)改用60mL 0.25mol·L-1H2SO4和50mL 0.55mol·L-1NaOH溶液进行反应,生成H2O的物质的量不同,则放出的热量不相等,依据中和热的定义可知,中和热不变;
本题答案为:不相等,相等。
(4)①未加硫酸,二氧化锰做催化剂,H2O2发生分解反应:2H2O2![]() 2H2O +O2↑,在有硫酸的条件下发生反应:MnO2+H2O2+2H+=Mn2++O2↑+2H2O,反应中MnO2的作氧化剂;
2H2O +O2↑,在有硫酸的条件下发生反应:MnO2+H2O2+2H+=Mn2++O2↑+2H2O,反应中MnO2的作氧化剂;
本题答案为:2H2O2![]() 2H2O +O2↑,氧化剂。
2H2O +O2↑,氧化剂。
②因为四个实验是对比实验,都产生相同的O2,故而需要n(H2O2)相同,所以V1=5mL,
且要测算产生等量O2所需的时间,所以混合容易的体积应相同,保证浓度相等;V3=1.5mL;
本题答案为:5,1.5。
③实验测得t2>t3>t4,是Ⅱ、Ⅲ、Ⅳ三个实验中,硫酸的浓度不同造成的,由此可以得出硫酸的浓度越大,反应速率越快,得到等量O2所需时间越小;
本题答案为:酸浓度越大,反应速率越快。


科目:高中化学 来源: 题型:
【题目】我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法。
Ⅰ.已知:2CO(g) + O2(g) = 2CO2(g) △ H = 566kJ/mol;2Fe(s)+![]() O2(g)= Fe2O3(s) △ H = 825.5kJ/mol
O2(g)= Fe2O3(s) △ H = 825.5kJ/mol
反应:Fe2O3(s) + 3CO(g)![]() 2Fe(s) + 3CO2(g) △H =_____kJ/mol。
2Fe(s) + 3CO2(g) △H =_____kJ/mol。
Ⅱ.反应 Fe2O3(s) + 3CO(g)![]() 2Fe(s) + 3CO2(g)在1000℃的平衡常数等于4.0。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡。
2Fe(s) + 3CO2(g)在1000℃的平衡常数等于4.0。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡。
(1)欲提高 CO 的平衡转化率,促进 Fe2O3的转化,可采取的措施是_____
a.提高反应温度 b.增大反应体系的压强 c.选取合适的催化剂 d.及时吸收或移出部分CO2 e.粉碎矿石,使其与平衡混合气体充分接触
Ⅲ.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:

CO(g) + 2H2(g)![]() CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题:
(1)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2) =_____。
(2)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表:
容器 | 反应物投入的量 | 反应物的转化率 | CH3OH的浓度 | 能量变化(Q1,Q2,Q3均大于 0) |
甲 | 1mol CO 和 2mol H2 | a1 | c1 | 放出Q1kJ 热量 |
乙 | 1mol CH3OH | a2 | c2 | 吸收Q2kJ 热量 |
丙 | 2mol CO 和 4mol H2 | a3 | c3 | 放出Q3kJ 热量 |
则下列关系正确的是_____。
a. c1 = c2 b..2Q1 = Q3 c..2a1 = a3 d..a1+ a2= 1 e.该反应若生成1mol CH3OH,则放出(Q1 + Q2)kJ 热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置为新型电池,放电时电池的总反应式为NaBr3+2Na2S2=3NaBr+Na2S4,下列说法正确的是( )
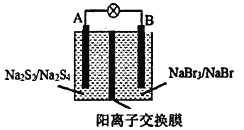
A.放电时A电极的反应式为2Na2S2+2e﹣═Na2S4+2Na+
B.放电时Na+从左向右通过阳离子交换膜
C.外电路中的电流方向为A→灯泡→B
D.放电时B电极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL0.1 molL﹣1 CH3COOH溶液中逐滴加入0.1molL﹣1的NaOH溶液,溶液中由水电离出的OH﹣浓度在此滴定过程变化如图所示,下列说法正确的是( )

A.a~e点,e点时水的电离程度最大
B.b、d两点溶液的pH相同
C.c点表示酸碱恰好完全反应,溶液中c(OH﹣)═c(CH3COOH)+c(H+)
D.d点所示溶液中c(Na+)>c( CH3COOH)>c( CH3COO﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.钠与水反应:Na+2H2O=Na++2OH-+H2↑
B.硫酸铝溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O
C.将氯气通入氯化亚铁溶液:2Fe2++Cl2=2Fe3++2Cl-
D.将![]() 通入到
通入到![]() 溶液中:
溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了①~⑩十种元素在周期表中的位置。
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ④ | ⑩ | |||||
3 | ⑤ | ⑥ | ⑦ | ③ | ⑧ | ⑨ | ||
回答下列问题:
(1)①、④按原子个数比1:1 组成的分子的电子式为____________________ ;由②、④两种元素组成的一种无毒化合物的结构式为 _____________________。
(2)这10种元素中,化学性质最不活泼的元素是_____________(填元素符号,下同),得电子能力最强的原子是__________________,失电子能力最强的单质与水反应的化学方程式是_________________________。
(3)用化学方程式表示②和⑨两种元素的非金属性强弱:________________________ 。
(4)元素③的气态氢化物和元素⑧的气态氢化物中,易于制备的是 ____________________(填化学式)
(5)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应,其离子方程式为 ______________________________。
(6)元素 ①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式:___________________ ;写出一种离子化合物的化学式:______________________。
(7)写出⑥的单质置换出②的单质的化学方程式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列生产或实验事实引出的相应结论不正确的是( )
选项 | 事实 | 结论 |
A | 工业制硫酸中,在矿石处理阶段,将矿石粉碎再煅烧 | 增大反应物的接触面积,加快化学反应速率 |
B | A、B两支试管中分别加入等体积5%的H2O2,在B试管中加入MnO2,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
C | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间变短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
D | 一定条件下:H2(g)+I2(g) | c(I2)增大,I2物质的量增多 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1 mol·L-1NaOH溶液滴定20 mL 0.1 mol·L-1CH3COOH溶液的滴定曲线如图所示。下列说法正确的是

A. 点①所示溶液中:c(Na+)>c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)
B. 点②所示溶液中:c(Na+)+c(H+)=c(CH3COO-) +c(CH3COOH) +c(OH-)
C. 点③所示溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D. 在整个滴定过程中:溶液中![]() 始终不变
始终不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯与一卤代烷在催化剂作用下可生成苯的同系物:![]() +CH3X→
+CH3X→![]() +HX,在催化剂存在下,由苯和下列各组物质合成乙苯最好应选用的是
+HX,在催化剂存在下,由苯和下列各组物质合成乙苯最好应选用的是
A.CH2=CH2和HClB.CH3CH3和I2
C.CH2=CH2和Cl2D.CH3CH3和HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com