
【题目】下表中实线是元素周期表的部分边界,其中上边界并未用实线画出. 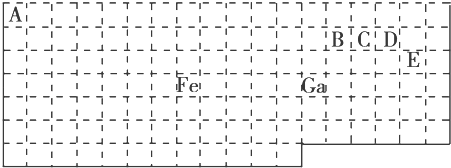
根据信息回答下列问题:
(1)基态Ga原子的最外层电子排布式为
(2)铁元素位于元素周期表的区;Fe和CO易形成配合物Fe(CO)5 , 在Fe(CO)5中铁的化合价为 .
(3)已知:原子数目和价电子总数均相同的微粒互为等电子体,等电子体具有相似的结构特征.与CO互为等电子体的分子和离子分别为和(填化学式).
(4)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有 .
(5)根据VSEPR模型预测ED4﹣的空间构型为 . B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的分子为(写2种).
【答案】
(1)4s24p1
(2)d;0
(3)N2;CN﹣
(4)CH4、CH3OH
(5)正四面体;CO2 CCl4
【解析】解:(1.)Ga位于第四周期第IIIA族,最外层有3个电子,其最外层电子排布式为4s24p1;所以答案是:4s24p1;
(2.)元素周期表五区的划分是根据最后排入的电子名称命名的.Fe原子是26号元素,Fe原子的基态核外电子排布式为:1s22s22p63s23p63d64s2 ,
这些电子排列时遵循能量最低原理(先排能量低的后排能量高的),这些能级的能量大小顺序为:1s<2s<2p<3s<3p<4s<3d,根据能量最低原理先排4s电子后排3d电子,所以 最后排入的是3d电子,根据命名规则属d区,根据化合物化合价的代数和为0,Fe与CO易形成配合物Fe(CO)5化合价的代数和为0,CO的化合价的代数和为0,所以答案是:d;0;(3.)根据等电子体的定义,CO的等电子体必须是双原子分子或离子,且电子总数相等.对于原子,原子序数=原子核外电子总数,所以,如果是分子,只要原子序数之和相等即可.CO中C是6号元素,O是8号元素,原子序数之和为14,N是7号元素,且可形成双原子分子,所以分子是N2 . 所以答案是:N2、CN﹣;
(4.)在CH4中价层电子对数=σ键电子对数(4)+中心原子上的孤电子对数(0),所以碳原子采取sp3杂化.在CO分子中价层电子对数=σ键电子对数(1)+中心原子上的孤电子对数(1),所以碳原子采取sp杂化.CH3OH中,价层电子对数=σ键电子对数(4)+中心原子上的孤电子对数(0),所以碳原子采取sp3杂化.所以答案是:CH4、CH3OH;
(5.)根据元素周期表知,E是Cl元素,D是O元素,ED4﹣是ClO4﹣离子,价层电子对数=σ键电子对数+中心原子上的孤电子对数,价层电子对数=4+ ![]() (7+1﹣4×2)=4,根据VSEPR理论预测ED4﹣离子的空间构型为正四面体型.C、N、O、Cl是四种元素,两两形成的化合物且每个原子最外层都达到8电子稳定结构的化合物有:CO2 CCl4 , 所以答案是:正四面体;CO2 CCl4 .
(7+1﹣4×2)=4,根据VSEPR理论预测ED4﹣离子的空间构型为正四面体型.C、N、O、Cl是四种元素,两两形成的化合物且每个原子最外层都达到8电子稳定结构的化合物有:CO2 CCl4 , 所以答案是:正四面体;CO2 CCl4 .


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下列分析正确的是
A. 异丁烷的二氯代物有4种
B. 区别蛋白质和淀粉可用浓硝酸做颜色反应
C. 石蜡油分解产物均能使酸性KMnO4溶液褪色
D. 甲苯的硝化反应方程式为: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石油产品A(C3H6)为主要原料,合成具有广泛用途的有机玻璃PMMA。流程如下(部分产物和条件省略)

试回答下列问题:
(1)B的名称________;X试剂为_______(化学式);D中官能团名称_________。
(2)E→G的化学方程式为________________________________________,反应类型是_________。
(3)T是G的同分异构体,1molT与足量新制Cu(OH)2悬浊液反应最多生成2molCu2O沉淀,T的结构有________种(不含立体结构)。
(4)若高分子化合物PMMA的相对分子质量为1.5×106,其聚合度为_______。
(5)参照上述流程,以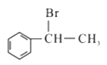 为原料合成
为原料合成 (其它原料自选)。设计合成路线:________________________。
(其它原料自选)。设计合成路线:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究题
Ⅰ.某烃A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振谱表明分子中只有一种类型的氢.
(1)写出A的结构简式 .
(2)A中的碳原子是否都处于同一平面?(填“是”或者“不是”).
(3)Ⅱ.2006年5月,齐齐哈尔第二制药厂生产的假药“亮菌甲素注射液”导致多名患者肾功能衰竭.“亮菌甲素”的结构简式为: 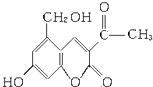
它配以辅料丙二醇溶成针剂用于临床.假药中使用廉价的二甘醇作为辅料,二甘醇为工业溶剂,有很强的毒性.请回答下列问题:
①下列有关“亮菌甲素”的叙述正确的是(填字母).
A.“亮菌甲素”能与H2发生加成反应
B.不能使酸性KMnO4溶液褪色
C.“亮菌甲素”的分子式是C12H10O5
D.“亮菌甲素”分子中含氧官能团只有2种
②丙二醇的分子式是C3H8O2 , 已知两个羟基连在同一个碳原子上的物质不存在.写出其所有属于醇类的同分异构体的结构简式.
③依据核磁共振氢谱分析,二甘醇分子中有3个吸收峰,其峰面积之比为2:2:1.又知二甘醇中含碳、氧元素的质量分数相同,且氢元素的质量分数为9.4%,1mol二甘醇与足量金属钠反应生成1mol H2 . 写出二甘醇的结构简式. .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.用苯可以萃取溴水中的溴单质
B.蒸馏时,应将温度计水银球插入液面下
C.为了使过滤速率加快,可用玻璃棒在过滤器中轻轻搅拌,加速液体流动
D.凡是给玻璃仪器加热,都要垫石棉网,以防仪器炸裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法正确的是( )
A.明矾可用作净水剂
B.甲醛可用作食品防腐剂
C.氢氧化钠可用来治疗胃酸过多
D.铝制容器可长期存放酸性食物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Na2CO3和NaHCO3的叙述正确的是
A. Na2CO3俗名苏打,NaHCO3俗名纯碱
B. 受热时,NaHCO3比Na2CO3容易分解
C. Na2CO3溶液显碱性,NaHCO3溶液显酸性
D. Na2CO3和NaHCO3各lmol分别与足量的盐酸充分反应,产生CO2质量不相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com