
【题目】4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性,回答下列问题: 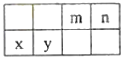
(1)元素x在周期表中的位置是第周期,第族,其单质可采用电解熔融的方法制备.
(2)m、n、y三种元素最高价氧化物的水化物中,酸性最强的是 , 碱性最强的是 . (填化学式)
(3)气体分子(mn)2的电子式为 . (mn)2成为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式为 .
【答案】
(1)三;IIA;氯化镁
(2)HNO3;Al(OH)3
(3)![]() ;2NaOH+(CN)2=NaCN+NaCNO+H2O
;2NaOH+(CN)2=NaCN+NaCNO+H2O
【解析】解:这几种元素都是短周期元素,且为相邻主族,根据元素在周期表中的位置知,m和n位于第二周期、x和y位于第三周期,x原子核外电子数是m的2倍,y的氧化物具有两性,则y是Al元素,根据元素位置知,x是Mg元素、m是C元素、n元素N元素,(1)元素x是Mg元素,在周期表中的位置是第三周期第IIA族,其单质可以采用电解熔融氯化镁的方法制备, 所以答案是:三;IIA;氯化镁;(2)m、n、y分别是C、N、Al,元素的金属性越强,其最高价氧化物的水化物碱性越强,元素的非金属性越强,其最高价氧化物的水化物酸性越强,这三种元素金属性最强的是Al元素、非金属性最强的是N元素,所以酸性最强的是HNO3 , 碱性最强的是Al(OH)3 , 所以答案是:HNO3;Al(OH)3;(3)气体分子(mn)2为(CN)2 , 电子式为 ![]() ,根据氯气和氢氧化钠溶液反应知,(CN)2和NaOH反应生成NaCN、NaCNO、H2O,反应方程式为2NaOH+(CN)2=NaCN+NaCNO+H2O,所以答案是:
,根据氯气和氢氧化钠溶液反应知,(CN)2和NaOH反应生成NaCN、NaCNO、H2O,反应方程式为2NaOH+(CN)2=NaCN+NaCNO+H2O,所以答案是: ![]() ;2NaOH+(CN)2=NaCN+NaCNO+H2O.
;2NaOH+(CN)2=NaCN+NaCNO+H2O.


科目:高中化学 来源: 题型:
【题目】下面对硝酸的认识不正确的是( )
A. 浓硝酸和稀硝酸都具有氧化性B. 铜与稀硝酸的反应属于置换反应
C. 金属与硝酸反应一定不产生氢气D. 可用铁或铝制品盛装浓硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在量热器中将50mL,0.50molL﹣1CH3COOH溶液与50mL、0.55molL﹣1NaOH溶液混合,温度从25.16℃升高到27.46℃.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J0C﹣1 , C=4.18Jg﹣10C﹣1 , 溶液的密度为1gcm﹣3 . 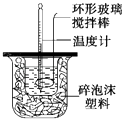
(1)试求CH3COOH的“中和热”.
(2)请你分析(1)中测得的实验值偏差可能是什么原因造成的? .
(3)若HNO3 (aq)+NaOH(aq)=NaNO3(aq)+H2O(l);△H=﹣57.3KJmol﹣1;
现有①稀H2SO4与Ba(OH)2(aq) ②浓H2SO4与Ba(OH)2(aq)
③HNO3与Ba(OH)2(aq)反应生成1molH2O(l) 的反应热分别为△H1、△H2、△H3 ,
则△H1、△H2、△H3三者由小到大的关系为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B.含有0.1NA个CO32﹣的Na2CO3固体的质量为10.6g
C.标准状况下,aL的氧气和氮气的混合物含有的原子数为 ![]() ×NA
×NA
D.标准状况下,11.2LCCl4含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数,下列有关叙述正确的是
A.SiO2的摩尔质量为60
B.过量的Fe粉与1 mol Cl2充分反应转移的电子数目为2NA
C.常温下,pH=2的NaHSO4溶液中所含H+数目为0.01NA
D.标准状况下,2.24 L HF与1.8 g H2O所含电子数目均为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一瓶甲和乙的混合液,已知甲和乙的某些性质如表所示:
物质 | 熔点/℃ | 沸点/℃ | 密度/(g·cm3) | 溶解性 |
甲 | 68 | 115 | 0.93 | 易溶于乙 |
乙 | 84 | 77 | 0.90 | 易溶于甲 |
据此,将甲和乙相互分离的最佳方法是
A.过滤法 B.蒸发法
C.萃取法 D.蒸馏法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com