
【题目】下列烷烃的命名正确的是( )
A.2,4﹣二乙基戊烷
B.4﹣甲基﹣3﹣乙基已烷
C.2﹣甲基﹣3﹣丙基戊烷
D.2,3,3﹣三甲基戊烷
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:
【题目】4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性,回答下列问题: 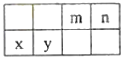
(1)元素x在周期表中的位置是第周期,第族,其单质可采用电解熔融的方法制备.
(2)m、n、y三种元素最高价氧化物的水化物中,酸性最强的是 , 碱性最强的是 . (填化学式)
(3)气体分子(mn)2的电子式为 . (mn)2成为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌.某含锌矿的主要成分是ZnS(还含有少量FeS等其它成分),以其为原料炼锌的工艺流程如图所示: 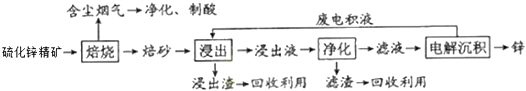
回答下列问题:
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,所产生焙砂的主要成分的化学式为 .
(2)焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的操作.
(3)浸出液“净化”过程中加入的主要物质为 , 其作用是 .
(4)电解沉积过程中的阴极采用铝板,阳极采用Pb﹣Ag合金惰性电极,阳极逸出的气体是 .
(5)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种由工业价值的非金属单质,“氧压酸浸”中发生主要反应的离子方程式为 .
(6)我国古代曾采用“火法”工艺冶炼锌.明代宋应星著《天工开物》中有关“升炼倭铅”的记载:“炉甘石十斤,装载入一尼罐内,…,然后逐层用煤炭饼垫盛,其底铺薪,发火锻红,…,冷淀,毁罐取出,…即倭铅也.”该炼锌工艺主要反应的化学方程式为 . (注:炉甘石的主要成分为碳酸锌,倭铅是指金属锌).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量Fe和Fe2O3的混合物放入300mL 2mol/L的硝酸溶液中,反应完全后无固体剩余,生成4.48L NO气体(标准状况),再向反应后的溶液中加入1mol/L的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积最少是( )
A.400mL
B.500mL
C.450mL
D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镁是科学家们制备的一种重要化合物,它可由单只直接化合而成,它与水作用的产物之一为NH3 . 请回答下列问题:
(1)Na3N是由键形成的化合物,写出它的电子式: .
(2)Na3N与水反应属于(填基本反应类型),写出该反应的化学方程式: .
(3)Na+与N3﹣的半径关系是Na+(填“>”、“<”或“=”)N3﹣ .
(4)Mg3N2与盐酸的反应生成种盐,用电子式表示其中只含有离子键的盐的形成过程 , 写出另一种盐的电子式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行滴定操作:
操作步骤:
A.在250mL容量瓶中配制250mL烧碱溶液
B.用碱式滴定管量取25.00mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品w g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为m mol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1 mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2 mL
附:酸碱指示剂变色范围
指示剂 | 变色范围 | 酸色 | 碱色 |
石蕊 | 5.0﹣8.0 | 红色 | 蓝色 |
酚酞 | 8.0﹣10.0 | 无色 | 红色 |
甲基橙 | 3.1﹣4.4 | 红色 | 黄色 |
请完成下列问题:
(1)选用仪器如下:①量筒;②锥形瓶;③滴定管;④玻璃棒.上列仪器中在使用前需检查是否漏水的是 . (填序号)除以上仪器外还缺的玻璃仪器有、 .
(2)正确的操作步骤是(填写字母)→→→→ .
(3)滴定管读数应注意 .
(4)操作中锥形瓶下垫一张白纸的作用是 .
(5)操作D中液面应调整到;
(6)滴定到终点时锥形瓶内溶液的pH约为;终点时的颜色变化是 .
(7)若酸式滴定管没用标准H2SO4润洗,会对测定结果有何影响(填“偏高”、“偏低”或“无影响”,其他操作均正确).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识,完成题目:
(1)在标准状况下1.7g氨气所占的体积为 , 它与同条件下molH2S含有相同的氢原子.
(2)某气体物质质量为6.4g,含有6.02×1022个分子,则该气体的摩尔质量为 .
(3)100mL、0.5mol/L的(NH4)2SO4溶液中含有NH ![]() mol,这些NH
mol,这些NH ![]() 中所含有的电子的物质的量为 , 质子的物质的量为 .
中所含有的电子的物质的量为 , 质子的物质的量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室通常用MnO2和浓盐酸共热制取Cl2 , 反应的化学方程式为MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O.
MnCl2+Cl2↑+2H2O.
(1)该反应的氧化剂是 , 氧化产物是 , 用双线桥法表示上述反应电子转移方向和数目.
(2)计算当有73.0克HCl完全参加反时,消耗MnO2的物质的量为多少?生成的气体在标准状况下的体积多少升?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国最新战机歼﹣31使用了高强度、耐高温的钛合金材料.工业上冶炼钛的反应如下:
TiCl4+2Mg ![]() Ti+2MgCl2 . 下列有关该反应的说法正确的是( )
Ti+2MgCl2 . 下列有关该反应的说法正确的是( )
A.TiCl4是还原剂
B.Mg被氧化
C.TiCl4发生氧化反应
D.Mg得到电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com