
����Ŀ�����ᡢ�����������г��������ʡ�
��1��25��ʱ��Ũ�Ⱦ�Ϊ0.1mol��L-1������ʹ�����Һ������˵����ȷ����___��
a.����Һ��pH��ͬ
b.����Һ�ĵ���������ͬ
c.����Һ����ˮ�������c(OH-)��ͬ
d.�к͵����ʵ�����NaOH����������Һ�������ͬ
��2��25��ʱ��pH������4�Ĵ�����Һ��������Һ��������Һ��ˮ�������H��Ũ����������Һ��ˮ�������H��Ũ��֮����___��
��3��������Һ�д��ڵ���ƽ�⣺CH3COOH![]() CH3COO-��H����������������ȷ����___��
CH3COO-��H����������������ȷ����___��
a.CH3COOH��Һ������Ũ�ȹ�ϵ���㣺c(H��)=c(OH-)��c(CH3COO)
b.0.1mol��L-1��CH3COOH��Һ��ˮϡ�ͣ���Һ��c(OH��)��С
c.CH3COOH��Һ�м�������CH3COONa���壬ƽ�������ƶ�
d.�����£�pH=2��CH3COOH��Һ��pH=12��NaOH��Һ�������Ϻ���Һ��pH��7
e.������pH=3�Ĵ�����Һ��ˮϡ�ͣ���Һ��![]() ����
����
��4�������£���pH��ͬ�������ͬ�Ĵ��������������Һ����ȡ���´�ʩ��
a.��ˮϡ��10��������Һ�е�c(H��)__(����>����=������<��)������Һ�е�c(H��)��
b.�ӵ�Ũ�ȵ�NaOH��Һ��ǡ���кͣ�����NaOH��Һ�����������__(����>����=������<��)���ᡣ
c.ʹ�¶ȶ�����20�棬��Һ��c(H��)������__(����>����=������<��)���ᡣ
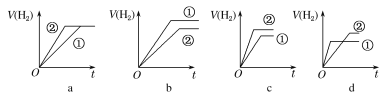
d.�ֱ���������п�۷�����Ӧ�����й����������(V)��ʱ��(t)�仯��ʾ��ͼ��ȷ����__(����ĸ)��(�ٱ�ʾ���ᣬ�ڱ�ʾ����)
��5����0.1mol��L-1��CH3COOH��ˮϡ�ͣ��й�ϡ�ͺ������Һ��˵���У���ȷ����__(����ĸ)��
a.����̶�����
b.��Һ��������������
c.��Һ��������ǿ
d.��Һ�д����������
���𰸡�d 1��1 bd > > > c ab
��������
(1)a��CH3COOH��������ʣ�HCl��ǿ����ʣ���Ũ�ȵ�������Һ��������c(H+)����CH3COOH�����Դ����pH����HCl���ʴ���
b��CH3COOH��������ʣ�HCl��ǿ����ʣ���Ũ�ȵ�������Һ������������Ũ�ȴ��ڴ��ᣬ��Һ�ĵ�������������Ũ�ȳ����ȣ�����HCl��Һ�ĵ�������ǿ���ʴ���
c��������ˮ���룬����������Ũ��Խ�������Ƴ̶�Խ��Ũ�ȵ��������У�HCl��������Ũ�ȴ��ڴ��ᣬ������ˮ�������c(OH-)����������ᣬ�ʴ���
d���к͵����ʵ�����NaOH��Һ�����������������Ũ�ȳɷ��ȣ�����������ʵ���Ũ����ȣ�������Ҫ��������ȣ�����ȷ��
��ѡ�ܣ�
(2)25��ʱ��pH������4�Ĵ�����Һ��������Һ������������c(H+)��ȣ����ˮ�ĵ������Ƴ̶���ͬ�����Դ�����Һ��ˮ�������H��Ũ����������Һ��ˮ�������H��Ũ��֮����1:1��
(3)a��CH3COOH��Һ�У����ݵ���غ��֪��c(H+)=c(OH-)+c(CH3COO)����a��ȷ��
b��0.1mol/L��CH3COOH��Һ��ˮϡ�ͣ���Һ���Լ���������Һ��c(OH-)����b����
c��CH3COOH��Һ�м�������CH3COONa���壬���������Ũ��������ƽ�������ƶ�����c��ȷ��
d�������£�pH=2��CH3COOH��ҺŨ�ȴ���pH=12��NaOH��Һ���������Ϻ������������Һ�����ԣ���Һ��pH��7����d����
e���������ˮ��ƽ�ⳣ��Kh=![]() ���¶Ȳ���ˮ��ƽ�ⳣ�����䣬����������pH=3�Ĵ�����Һ��ˮϡ�ͣ���Һ��
���¶Ȳ���ˮ��ƽ�ⳣ�����䣬����������pH=3�Ĵ�����Һ��ˮϡ�ͣ���Һ��![]() ���䣬��e��ȷ��
���䣬��e��ȷ��
��������ѡbd��
(4)a��pH��ͬ�������ͬ�Ĵ��������������Һ�ֱ��ˮϡ�ͺ���Һ��������Ũ�ȶ���С������pH����������������ڵ���ƽ�⣬�ֵ���������ӣ�������Һ�е�c(H+)��������Һ�е�c(H+)��
b��pH��ͬ�Ĵ�������ᣬ�����Ũ�ȴ������ᣬ�ӵ�Ũ�ȵ�NaOH��Һ��ǡ��ǡ���кͣ�����NaOH��Һ�������������
c��������ǿ�ᣬ�����ڵ���ƽ�⣬�����¶Ȳ�Ӱ�������pH�����������ᣬ��ˮ��Һ�д��ڵ���ƽ�⣬�����¶ȣ��ٽ�������룬���´�����Һ��������Ũ������������Һ��c(H+)��������
d����Ϊǿ����ȫ���룬һԪ���Ჿ�ֵ��룬���Ҫ����ͬ��pHֵ��һԪ�����Ũ�ȱ����ǿ������������ȣ����һԪ��������ʵ�������ǿ�ᣬ��˲�����H2Ҳ��ǿ��࣬�ݴ˿��ų�a��b����ʼʱH+Ũ����ȣ���˷�Ӧ����Ҳ���(��ͼ�з�Ӧ���ʾ���б��)�����ŷ�Ӧ��������H+���ϱ����ĵ�����ʹһԪ����������룬����ӻ���H+Ũ���½������ʣ���ʱ����ķ�Ӧ���ʾ�Ҫ����ǿ��ķ�Ӧ���ʣ�����������H2�����һԪ�����ѡc��
(5)��0.1molL-1��CH3COOH��ˮϡ�ͣ���ҺŨ�ȼ�С�����������ĵ���ƽ�����ƣ�
a����ˮ����ĵ���ƽ�����ƣ��ʵ���̶�����a��ȷ��
b����ˮ����ƽ�����ƣ�����Һ�������������࣬��b��ȷ��
c����ˮ����Ȼ����������ӵ����ʵ������࣬����Һ�������Ũ�ȼ�С������Һ�����Լ�������c����
d����ˮ����ƽ�����ƣ�����Һ�д�����Ӽ��٣���d����
��ѡab��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л������������ȷ����(����)
A. ��֬��ϡ���������������Һ�о��ɷ���ˮ�ⷴӦ������ˮ�������ͬ
B. ȡ������ϡ���Ṳ�Ⱥ����Һ����������������Һ���ȣ�û������������˵��������δˮ������������
C. �ṹʽΪ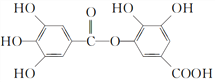 ���л��������ϡ������·���ˮ�ⷴӦ����ˮ�����ֻ��һ��
���л��������ϡ������·���ˮ�ⷴӦ����ˮ�����ֻ��һ��
D. ��ά�ء����ǡ������ǡ���������һ�������¾��ɷ���ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.1 mol��L��1 CH3COOH��Һ�д������µ���ƽ�⣺ CH3COOH ![]() CH3COO����H+�����ڸ�ƽ�⣬����������ȷ���ǣ� ��
CH3COO����H+�����ڸ�ƽ�⣬����������ȷ���ǣ� ��
A. ����ˮʱ��ƽ�����淴Ӧ�����ƶ�
B. ��������NaOH���壬ƽ��������Ӧ�����ƶ�
C. ��������0.1 mol��L��1 HCl��Һ����Һ��c(H+)��С
D. ��������CH3COONa���壬ƽ��������Ӧ�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����������ת�����̵�X�ǣ�������
X![]() ��ҺW
��ҺW![]() Z
Z![]() X
X
A.FeOB.SiO2C.Al2O3D.NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Ȼ��֬A�ķ���ʽΪC57H106O6��1mol����֬��ȫˮ��ɵõ�1mol���͡�1mol������֬����B��2molֱ������֬����C�����ⶨB����Է�������Ϊ280��ԭ�Ӹ�����ΪN(C)��N(H)��N(O)=9��16��1��
��1��д��B�ķ���ʽ��__��
��2��д��C�Ľṹ��ʽ��__��C��������__��
��3��д����5��̼ԭ�ӵ�C��ͬϵ����ܵĽṹ��ʽ��__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ի������Һ�о�����NO3������������ԭ��Ӧ��ת����ϵ����ͼ��ʾ��
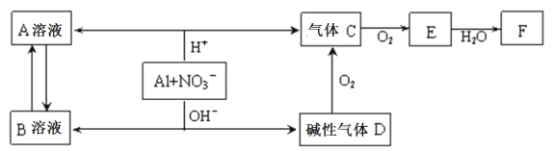
����˵���������
A.B��Һ��[Al(OH)4]��
B.A��Һ��B��Һ�������������
C.D��F��Ӧ������
D.E��������л������Ⱦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Դ�ı��⣬�����ŷḻ�Ļ�ѧԪ�أ����ȡ��塢��ȣ�������Դ���ۺ����þ��зdz�������ǰ����
(1)����˵����ȷ����_________��
a��AgCl��AgBr��AgI����ɫ���α��� b��F��Cl��Br��I�ķǽ�����������ǿ
c��HF��HCl��HBr��HI�Ļ�ԭ�Ե�������ǿ d��F2��Cl2��Br2��I2��H2�������ѱ���
(2)ʵ���ҴӺ��������ȡ���������������ͼ��
![]()
������ʱ�����Լ���MnO2�����������½�����������Ӧ�����ӷ���ʽΪ��_________��
����������٢ڢ۷�������ֱ�Ϊ���ˡ�_________��_________��
(3)�Ӻ�ˮ��ȡ�Ĵ����к���Mg2+��Fe2+��Ca2+��SO42�������ʣ������ӡ������Լ��У��ٹ�����NaOH��Һ�ڹ�����Na2CO3��Һ������������ܹ�����BaCl2��Һ���Լ�������˳��Ϊ_________��
ΪʹCa2+��ȫ��������Һ��c(CO32��)Ӧ��С��_________mol/L��[��֪Ksp(CaCO3)=2.9��10-9������Ũ��С��1��10-5mol/L��Ϊ��ȫ����]
(4)Ŀǰ������ʳ����ȡ������Ҫ����������͡������Ƽ�����ֹ���

�������� NaHCO3��ԭ����_________��
���������������Һ�м���_________����NH3��ѭ��ʹ�ã������������Ķ�����CaCl2���������Ƽ��������Һ�м���ͨ��NH3��������NaCl��ĩ���Ƶø���ĸ�����_________��
�۳����£���ʳ��ˮ��ͨ��NH3��CO2����(HCO3��)=c(NH4+)ʱ����Һ��pH_____7 (�>������<����=��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״�߷��ӻ�����![]() �����л�����ԭ��
�����л�����ԭ��![]() ���������Լ�ͨ���ӳɷ�Ӧ��ˮ�ⷴӦ��������Ӧ�����۷�Ӧ�Ƶã���
���������Լ�ͨ���ӳɷ�Ӧ��ˮ�ⷴӦ��������Ӧ�����۷�Ӧ�Ƶã���![]() �ǣ� ��
�ǣ� ��
A.�Ҵ�B.![]() ����C.��ϩD.1��
����C.��ϩD.1��![]() ����ϩ
����ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л��������˵����ȷ���ǣ� ��
A.��Է�������Ϊ72��ij������һ�ȴ�����4��
B.�ı�����ϩ![]() ������̼ԭ��һ������ͬһƽ��
������̼ԭ��һ������ͬһƽ��
C.��һ�������£�����Һ�塢Ũ���������屽���������ķ�Ӧ������ȡ����Ӧ
D.![]() ��
��![]() ����������һ����-CH2-���������ͬϵ��
����������һ����-CH2-���������ͬϵ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com