
【题目】恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示。已知:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-196.6 kJ/mol。
2SO3(g) ΔH=-196.6 kJ/mol。
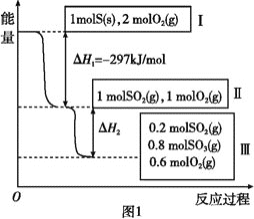
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:________________。
(2)状态Ⅱ到状态Ⅲ放出的热量为__________。
(3)恒温恒容时,1 mol SO2和2 mol O2充分反应,放出热量的数值比∣ΔH2∣_____(填“大”、“小”或“相等”)。
(4)将Ⅲ中的混合气体通入足量的NaOH溶液中消耗NaOH的物质的量为______,若溶液中发生了氧化还原反应,则该过程的离子方程式为:_______________。
【答案】S(s)+O2(g)=SO2(g) ΔH=-297 kJ/mol 78.64 kJ 大 2 mol 2SO2+O2+4OH-=2SO42-+2H2O
【解析】
由图可知,状态Ⅰ到状态Ⅱ为硫燃烧生成二氧化硫的过程,反应的热化学方程式为. S(s)+O2(g)=SO2(g) ΔH=-297 kJ/mol;状态Ⅱ到状态Ⅲ二氧化硫发生催化氧化反应生成三氧化硫,反应的热化学方程式为2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-196.6 kJ/mol。
2SO3(g) ΔH=-196.6 kJ/mol。
(1)燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物放出的热量,由图可知1molS(s)完全燃烧放出的热量为297KJ,则能表示硫的燃烧热的热化学方程式为S(s)+O2(g)=SO2(g) ΔH=-297 kJ/mol,故答案为:S(s)+O2(g)=SO2(g) ΔH=-297 kJ/mol;
(2)由图可知,状态Ⅱ到状态Ⅲ时0.8mol二氧化硫参与反应,则反应放出的热量为![]() =8.64 kJ,故答案为:8.64 kJ;
=8.64 kJ,故答案为:8.64 kJ;
(3)恒温恒容时,开始为1molSO2和2molO2与开始为1molSO2和1molO2相比,氧气的浓度增大,增大反应物浓度,平衡向正反应方向移动,SO2转化率增大,反应放出热量的数值比Q2大,故答案为:大;
(4)将Ⅲ中的混合气体通入足量的NaOH溶液中,三氧化硫与氢氧化钠反应反应生成硫酸钠,混合气体中的二氧化硫和氧气在氢氧化钠溶液中发生氧化还原反应生成硫酸钠和水,反应的离子方程式为2SO2+O2+4OH-═2SO42-+2H2O,因反应最后得到硫酸钠溶液,根据钠原子和硫原子原子守恒可得n(NaOH)=2n(S)=2×(0.2+0.8)mol=2mol,故答案为:2;2SO2+O2+4OH-═2SO42-+2H2O;


 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
【题目】下列有关金属的工业制法中正确的是( )
A.炼铝:用电解氯化铝溶液的方法获得单质铝
B.制钛:用金属钠置换熔融四氯化钛(TiCl4)中的钛
C.制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液
D.炼铁:用焦炭和空气反应产生的CO在高温下还原铁矿石中铁的氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,由CO和CO2组成的混合气体8.96L,质量是16g。此混合物中CO和CO2的物质的量之比是_____________,CO的体积分数是_____________,该混合气体对于氢气的相对密度为________ 。
(2) 1.12g金属铁跟某稀盐酸恰好完全反应,得到100mL溶液,试计算:
①生成的气体在标准状况下的体积是_________________
②反应后所得溶液中溶质的物质的量浓度是______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A. 达到化学平衡时4v正(O2)=5v逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C. 达到化学平衡时,若增大容器容积,则正反应速率减小,逆反应速率增大
D. 化学反应速率关系:2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Cu(s)+2H+(aq)===Cu2+(aq)+H2(g) ΔH1
2H2O2(l)===2H2O(l)+O2(g) ΔH2
2H2(g)+O2(g)===2H2O(l) ΔH3
则反应Cu(s)+H2O2(l)+2H+(aq)===Cu2+(aq)+2H2O(l)的ΔH是
A. ΔH=ΔH1+1/2ΔH2+1/2ΔH3 B. ΔH=ΔH1+1/2ΔH2-1/2ΔH3
C. ΔH=ΔH1+2ΔH2+2ΔH3 D. ΔH=2ΔH1+ΔH2+ΔH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数递增的短周期主族元素,Y的简单气态氢化物水溶液呈弱碱性, Z元素无正价,且基态原子有2个未成对电子,基态W原子价层电子排布式为nsn-1npn-1 ,X与W为同主族元素。基态R原子M能层全充满且核外有且仅有1个未成对电子。请回答下列问题:
(1)基态R原子的核外电子排布式为____________________。R单质晶体晶胞的堆积方式_______________,晶胞的空间利用率为___________________。
(2) X、Y、Z三种元素的第一电离能由小到大的顺序为__________ (填“元素符号”,下同)
(3)YF3分子中Y的杂化类型为______________。该分子的空间构型为_________________。
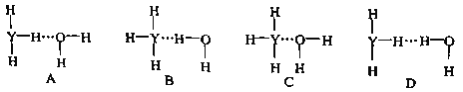
(4)Y的气态氢化物在水中可形成氢键,其氢键最可能的形式为___________________。
(5)X的某气态氧化物的相对分子质量为44,分子中的大π键可用符号Π![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则其气态氧化物中的大π键应表示为_______________,其中σ键与π数目之比为______________。
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则其气态氧化物中的大π键应表示为_______________,其中σ键与π数目之比为______________。
(6)R元素与Y元素形成某种化合物的晶胞结构如图所示(黑球代表R原子),若该晶体的密度为ρg·cm-3,则该晶胞的边长是_________cm (NA表示阿伏伽德罗常数的值)。
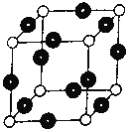
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组从富含NaBr的工业废水中提取 Br2的过程主要包括:氧化、萃取、分液、蒸馏等步骤。已知:可能用到的数据信息和装置如下:
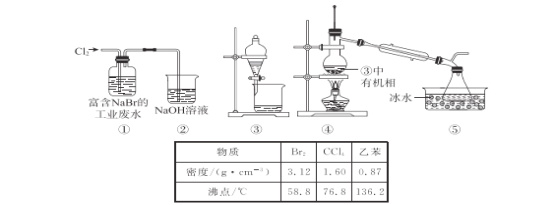
下列说法错误的是
A.实验时,①的反应的离子方程式:Cl2+2Br-=2Cl-+Br2
B.②中的玻璃直管最好换成一个倒扣的漏斗,与NaOH溶液液面相切
C.用③进行萃取时,选择CCl4比乙苯更合理
D.④中温度计水银球低于支管过多,导致Br2的产率低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在制氯气时有如下操作,操作顺序正确的是( )
①连接好装置,检查气密性;
②缓缓加热,加快反应,使气体均匀逸出;
③在圆底烧瓶中加入二氧化锰粉末;
④从盛有浓盐酸的分液漏斗中将浓盐酸缓缓滴入烧瓶中;
⑤将多余的氯气用氢氧化钠溶液吸收;
⑥用向上排空气法收集氯气。
A.①②③④⑤⑥B.③④②①⑥⑤C.①④③②⑥⑤D.①③④②⑥⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为常见的金属单质,根据如下所示的转化关系回答下列问题:
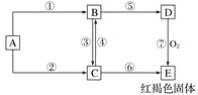
(1)写出下列物质的化学式:
A________,B_______,C_______,D_________,E__________。
(2)反应③的离子方程式为_______________;
反应④的离子方程式为___________;
反应⑦的化学方程式为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com