
����Ŀ�������£���0.01molL��1 NaOH��Һ�ζ�20.00mL 0.01molL��1 CH3COOH��Һ�����õζ�������ͼ������˵����ȷ���ǣ� �� 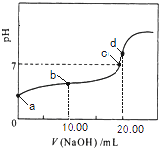
A.a���Ӧ��Һ��pH=2
B.b���Ӧ����Һ�У�c��OH����+c��CH3COO����=c��Na+��+c��H+��
C.c���ʾNaOH��Һ��CH3COOH��Һǡ����ȫ��Ӧ
D.d���Ӧ����Һ�У�ˮ�ĵ���̶�С��ͬ���´�ˮ�ĵ���̶�
���𰸡�B
���������⣺A������Ϊ���ᣬ������ȫ���룬��0.01molL��1 CH3COOH��ҺpH��2����A����B����Һ�д��ڵ���غ㣺c��Na+��+c��H+��=c��OH����+c��CH3COO��������B��ȷ��
C��������������Ʒ�Ӧ���ɴ����ƣ���������ǿ����������ˮ��Һ�ʼ��ԣ������ǡ�÷�Ӧʱ��ҺӦ�óʼ��ԣ���C����Һ�����ԣ�˵�����������C����
D��d��ʱ��Һ�ʼ��ԣ������ǡ���кͣ���ȫ��Ӧ���ɴ����ƣ�ˮ��ʼ��ԣ��ٽ�ˮ�ĵ��룬��D����
��ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�У��������ӿ��ܴ���������ǣ� ��
A.��ˮ�������c��H+��=10��13 mol?L��1����Һ�У�Al3+��K+��NO ![]() ��SO
��SO ![]()
B.ǿ������Һ�У�Cu2+��ClO����Cl����Ba2+
C.0.1 mol?L��1 ��NaHCO3��Һ�У�K+��Al3+��Fe3+��NO ![]()
D.pH=7����Һ�У�K+��Fe3+��Cl����NO ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W��N�����ɶ�����Ԫ����ɵ����ֻ������֪���ֻ�����ˮ��Һ����ɫ��Ӧ���ʻ�ɫ��Y��Z��N��������Ԫ����ɣ��������ĿҪ��ش��������⣮
��1�����廯����XΪdz��ɫ��ĩ���û������к��еĻ�ѧ����������ţ���
A.���Ӽ�
B.���Թ��ۼ�
C.�Ǽ��Թ��ۼ�
D.���
��2��д��X�������̼��Ӧ�Ļ�ѧ����ʽ ��
��3���±�ΪY��Zʵ��IJ������ݣ�
��� | ��Ҫʵ�鲽�輰ʵ������ |
�� | �ں�Y����Һ�У�����ϡ������ã�����dz��ɫ��������ɫ�д̼�����ζ�����壬�������ʹƷ����Һ��ɫ |
�� | �ں�Z����Һ�У��μ����ᣬ��ʼ�а�ɫ�����������μ����ᣬ��ɫ���������Ӻ���ʧ��Ȼ���������İ�ˮ�ֳ��ְ�ɫ���� |
�� | ��ʵ������յõ��Ļ����������������գ����յõ���ɫ���� |
д��Y��ϡ���ᷴӦ�����ӷ���ʽ ��
��4��д����0.1mol Z����Һ��20mL 5molL��1�����ᷴӦ�����ӷ�Ӧʽ �� ʵ��ۼ������������յõ������ղ�����Ҫ�� ��
��5��������W��N�����ת����W ![]() N������W��NxH2O�Ļ����6.52g�����ȵ���ȫ��Ӧ���������ͨ��Ũ��������1.71g��ʣ������ͨ����ʯ������1.10g����������W������Ϊ �� NxH2O�Ļ�ѧʽΪ ��
N������W��NxH2O�Ļ����6.52g�����ȵ���ȫ��Ӧ���������ͨ��Ũ��������1.71g��ʣ������ͨ����ʯ������1.10g����������W������Ϊ �� NxH2O�Ļ�ѧʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25����101kPa�������£�1gҺ̬�״�(CH3OH)ȼ������CO2(g)��Һ̬ˮʱ����22.68kJ�������Ȼ�ѧ����ʽ��ȷ����
A. CH3OH(l)+ ![]() O2(g) =CO2(g)+2H2O(l)����H=725.76 kJ��mol-1
O2(g) =CO2(g)+2H2O(l)����H=725.76 kJ��mol-1
B. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)����H=-1451.52 kJ��mol-1
C. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)����H=-725.76kJ��mol-1
D. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)����H=1451.52kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�����ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã���ͼ��N2(g)��H2(g)��Ӧ����1mo1NH3(g)�����������仯ʾ��ͼ��

��д��N2��H2��Ӧ���Ȼ�ѧ����ʽ��_____________________________��
��2������֪�������ݣ�
��ѧ�� | H-H | N��N |
����/kJmol-1 | 435 | 943 |
�Ը��ݱ��м�ͼ�����ݼ���N-H�ļ���______kJmol-1
��3����֪100ml lmol/L������������Һ������������Һ��ȫ��Ӧ�ų�5.73kJ����������д����ʾ�к��ȵ��Ȼ�ѧ����ʽ________________________________��
��4����֪1��������ȫȼ������Һ̬ˮʱ�ų�akJ����������д����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ____________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ܱ������з�����ӦN2+3H22NH3 �� �ﵽƽ���ֻ�ı�ijһ������ʱ����Ӧ�����뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ��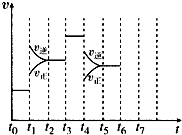
�ش��������⣺
��1������ƽ��״̬��ʱ���������ѡ���
A.t0��t1
B.t1��t2
C.t2��t3
D.t3��t4
E.t4��t5
F.t5��t6
��2��t1��t3��t4ʱ�̷ֱ�ı��һ�������ǣ���ѡ���A������ѹǿ B����Сѹǿ C�������¶�
D�������¶� E���Ӵ��� F�����뵪��
t1ʱ����t3ʱ����
��3�����ݣ�2���еĽ��ۣ�����ʱ����У����İٷֺ�����ߵ�������ѡ���
A.t0��t1
B.t2��t3
C.t3��t4
D.t5��t6
��4��һ�������£��ϳɰ���Ӧ�ﵽƽ��ʱ����û�������а������������Ϊ20%����Ӧ���뷴Ӧǰ�Ļ���������֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������������ҩƷ��ȡ���﴿����������
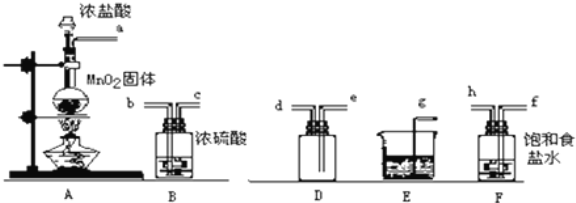
��1�������������ң�װ����ȷ������˳��a�� �� �� �� �� �� ��������ӿ���ĸ��____________
��2��װ��F��������____��װ��E��������____��
��3��װ��A��E�еķ�Ӧ��ѧ����ʽΪ��ÿ��2�֣���A___��E____��
��4������8.7gMnO2�μ��˷�Ӧ��������������ͨ��������KI��Һ���ܲ������ʵ������____g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����5NH4NO3�T 2HNO3+4N2��+9H2O�У�����������Ӧ�ĵ�ԭ�Ӻͷ�����ԭ��Ӧ�ĵ�ԭ�ӵ���������
A. 1��1 B. 3��5 C. 5��3 D. 2��8
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com