
【题目】下列说法正确的是
A. 煤焦油干馏可得到苯、甲苯等
B. 煤裂化可得到汽油、柴油、煤油等轻质油
C. 石油分馏可得到乙烯、丙烯等重要化工产品
D. 油脂皂化反应基本完成的现象是,反应后静置,反应液不分层
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列关于丙烯(CH3﹣CH=CH2)的说法正确的
A. 丙烯分子有7个σ键,1个π键B. 丙烯分子中不含手性碳原子
C. 丙烯分子中3个碳原子都是sp2杂化D. 丙烯分子中所有原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) ![]() 用系统命名法命名:________________;
用系统命名法命名:________________;
(2)下列实验操作或对实验事实的描述中正确的说法有____________________;
① 分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
② 除去甲烷中混有的少量乙烯,可以让混合物通过盛有酸性KMnO4溶液的洗气装置
③ 苯与溴水制溴苯
④ 只用溴水就可将苯、四氯化碳、乙醇、己烯四种液体区别开来
⑤ 用分液法分离苯和硝基苯的混合物
⑥酯类在碱性条件下的水解反应叫皂化反应
⑦裂化的目的主要是制得更多的乙烯、丙烯等不饱和烃
⑧除去乙酸乙酯中的乙酸也可以用氢氧化钠溶液洗涤,然后再分液
⑨煤中含有苯、甲苯,可先干馏后分馏的方法把它们分离出来
⑩乙烷、苯、乙醇、乙酸、乙酸乙酯均可发生取代反应
(3)某芳香烃结构为![]() ,它的分子式为_____,它的一氯代物有____种。
,它的分子式为_____,它的一氯代物有____种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应在体积为5L的恒容密闭容器中进行, 在0-3分钟内各物质的量的变化情况如图所示(A,B,C均为气体,且A气体有颜色)。
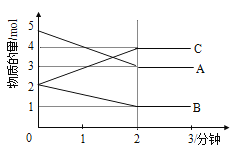
(1)该反应的的化学方程式为_____________________________。
(2)反应开始至2分钟时,B的平均反应速率为_________。
(3)能说明该反应已达到平衡状态的是___________。
a.v(A)= 2v(B) b.容器内各物质的物质的量相等
c.v逆(A)=v正(C) d.容器内气体的颜色保持不变
(4)由图求得平衡时A的转化率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器里,A与B反应生成C,其反应速率分别用vA、vB、vC表示,已知2vB=3vA、3vC=2vB , 则此反应可表示为( )
A.2A+3B=2C
B.A+3B=2C
C.3A+B=2C
D.A+B=C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铜(Cu2(OH)2CO3)是名贵的矿物宝石孔雀石的主要成分,应用广泛,如在无机工业中用于制造各种铜化合物,有机工业中用作有机合成催化剂等等,某化学小组为了探究碱式碳酸铜生成条件对其产率的影响,设计了如下实验:
设计原理:取一定体积的碳酸钠溶液(0.5mol/L)于100mL烧杯中,进行加热,恒温后将硫酸铜溶液(5.00mL. 0.5mol/L)在不断搅拌下以一定速度逐滴加入到上述碳酸钠溶液中,反应达平衡后,静止,减压过滤,洗涤,烘干,即得到最终产品,同时有气体放出。
(1)反应原理为:________________。
(2)探究反应原料用量比对反应产物的影响。
该化学小组根据所提供试剂设汁两个实验来说明反应原料用量对产品的影响
提供试剂:0.5mol/LNa2CO3溶液、0.5mol/LCuSO4溶液。
①请填写下表的空白处:
① | ② | ③ | ④ | |
硫酸铜溶液体积/mL | 2.0 | 2.0 | 2.0 | 2.0 |
碳酸钠溶液体积/mL | 1.6 | 2.0 | 2.8 | |
Na2CO3/CuSO4mol/比) | 0.8 | 1 | 1.4 |
②通过实验画图可知:当比值为______,碱式碳酸铜产量最好。

(3)反应温度对产率的影响
在三支试管中各加入2.0mL0.5 mol/LCuSO4溶液另取四支试管各加入由上述实验得到的合适用量的0.5 mol /L Na2CO3溶液。从这两列试管中各取一支将它们分別置于室温、30℃、50℃、100℃的环境中数分钟后将CuSO4溶液倒入Na2CO3溶液中振荡并观察现象,发现:沉淀颜色分别为蓝色沉淀,绿色沉淀、深绿色沉淀,绿色中带有黑色沉淀,实验结果也如上图所示,请思考,为什么温度过髙产率反而下降_______,该实验加热方式为____________。
(4)分析所制得的碱式碳酸铜的质量分数。
将已准确称量的0.5g试样样品放入300mL的锥形瓶中,加入5mL醋酸,适热使其溶解,再用l00mL水将其稀释。加入2.5gKI振荡混合,经过5分钟后,加入数滴淀粉溶液,用0.1mol/L的硫代硫酸钠溶液进行滴定。当_______时即达滴定的终点。
反应的原理:2Cu2++4I- =2CuI+I2, I2+2S2O32-=2I-+S4O62-
用0.lmol/L硫代硫酸钠40 mL,那么试样中铜的质量百分率为________。
该溶液的滴定度为_______。(毎毫升标准溶液相当于被测物质的质量,单位是g/mL或mg/mL)(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关SO2说法中不正确的是:
A. SO2是污染大气的有害气体之一 B. SO2在大气中与水反应生成硫酸,产生酸雨
C. SO2可使澄清石灰水变浑浊 D. SO2能使品红溶液褪色,加热溶液颜色恢复
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com