
 C�ֱ������ֲ�ͬʵ�������½��У����ǵ���ʼŨ�Ⱦ�Ϊc(A)="0.100" mol��L-1��c(B)="0.200" mol��L-1��c(C)="0" mol��L-1����Ӧ��A��Ũ����ʱ��ı仯����ͼ��ʾ������˵����ȷ���� �� ��
C�ֱ������ֲ�ͬʵ�������½��У����ǵ���ʼŨ�Ⱦ�Ϊc(A)="0.100" mol��L-1��c(B)="0.200" mol��L-1��c(C)="0" mol��L-1����Ӧ��A��Ũ����ʱ��ı仯����ͼ��ʾ������˵����ȷ���� �� ��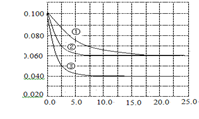
 C����H��0
C����H��0

 �ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
�ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2Z��g�� ��H����a kJ��mol��1��a��0������һ���ݻ��̶��������м���2molX2��1mo1Y2����500��Գ�ַ�Ӧ��ƽ���Z��Ũ��ΪW mol��L��1���ų�����b kJ��
2Z��g�� ��H����a kJ��mol��1��a��0������һ���ݻ��̶��������м���2molX2��1mo1Y2����500��Գ�ַ�Ӧ��ƽ���Z��Ũ��ΪW mol��L��1���ų�����b kJ��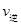 ��X2����2
��X2����2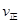 ��Y2�� d�������ڵ��ܶȱ��ֲ���
��Y2�� d�������ڵ��ܶȱ��ֲ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ơ��ƿ��ƿ�����̷��������ĭ |
| B����H2��I2������HI��ɵ�ƽ����ϵ��ѹ����ɫ���� |
| C���ں���Fe��SCN��3�ĺ�ɫ��Һ�м������ۣ����ã� |
| D����ˮӦ�ܱձ��棬�õ��´� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

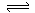 2C0(g) ��H>O��K1 �� ��
2C0(g) ��H>O��K1 �� ��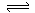 H2(g)+C02(g)��K2 ������ �� ��
H2(g)+C02(g)��K2 ������ �� ��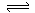 CO(g)+H2(g)��K3 ���������� ��
CO(g)+H2(g)��K3 ���������� ��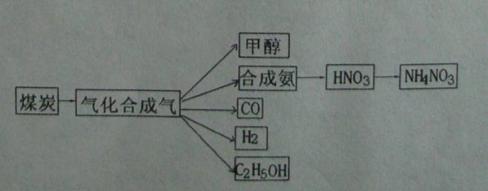

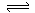 2N02(g) ��H>O�����¶�ΪT1��T2ʱ��ƽ����ϵ��N02�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����( )
2N02(g) ��H>O�����¶�ΪT1��T2ʱ��ƽ����ϵ��N02�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ����( )
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����������������백���ɵ�����֮��Ϊ3��2 |
| B���������ʱ�����������ܶȲ��ٸı� |
| C�����������������백����������֮��Ϊ1��2 |
| D�����������ʵ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��v(��)����v(��)��С��ƽ��������Ӧ�����ƶ���ƽ��ʱSO3�İٷֺ������� |
| B��v(��)����v(��)���䣬ƽ��������Ӧ�����ƶ���ƽ��ʱSO3�İٷֺ������� |
| C��v(��) ��С��v(��)����ƽ��������Ӧ�����ƶ���ƽ��ʱSO3�İٷֺ������� |
| D����ʼʱv(��)����ƽ��������Ӧ�����ƶ���ƽ��ʱSO3�İٷֺ������ֲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ������Ӧ�ﵽƽ��ʱ��CO���������Ϊx����ά��������������¶Ȳ��䣬��ʼ���ʰ�����������ȳ���������У��ﵽƽ��ʱCO�������������x����(����)
������Ӧ�ﵽƽ��ʱ��CO���������Ϊx����ά��������������¶Ȳ��䣬��ʼ���ʰ�����������ȳ���������У��ﵽƽ��ʱCO�������������x����(����)| A��0.5 mol CO��2 mol H2O(g)��1 mol CO2��1 mol H2 |
| B��1 mol CO��1 mol H2O(g)��1 mol CO2��1 mol H2 |
| C��0.5 mol CO��1.5 mol H2O(g)��0.4 mol CO2��0.4 mol H2 |
| D��0.5 mol CO��1.5 mol H2O(g)��0.5 mol CO2��0.5 mol H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 VO2��+ 2H����V2+��
VO2��+ 2H����V2+�� N2(g)+2CO2(g)����H��0��
N2(g)+2CO2(g)����H��0��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com