
����Ŀ��ú������Ҫ�ĺ���������H2S�Լ�COS���л���ú��ȼ�պ������ʻ�ת����SO2�Ӷ����������Ⱦ�����ú����H2S���ѳ��̶��ѳ�Ϊú���ྻ�ȵ�һ����Ҫָ�ꡣ��ش���������:
��1��H2S��ˮ��Һ�еĵ��뷽��ʽΪ___________��
��2���ѳ�ú����COS�ķ�����Br2��KOH��Һ��������H2��ԭ����ˮ�ⷨ�ȡ�
��COS�ķ��ӽṹ��CO2���ƣ�COS�ĽṹʽΪ___________��
��Br2��KOH��Һ��COS����Ϊ�����ε����ӷ���ʽΪ______________��
����֪��H2��COS��H2S��CO��ȼ��������Ϊ285kJ/mol��299kJ/mol��586kJ/mol��283kJ/mol��H2��ԭCOS�����ķ�ӦΪH2(g)+COS(g)=H2S(g)+CO(g)���÷�Ӧ�Ħ�H=_________kJ/mol��
���û��Ԧ�-Al2O3��COSˮ�ⷴӦΪCOS(g)+H2O(g) ![]() CO2(g)+H2S(g) ��H<0����ͬ�������ڴ�������ͣ����ͬʱ��ʱ����ͬ�¶���COS��ת���ʣ�δ�ﵽƽ�⣩��ͼ1��ʾ��ij�¶��£�COS��ƽ��ת������n(H2O)/n(COS)�Ĺ�ϵ��ͼ2��ʾ��
CO2(g)+H2S(g) ��H<0����ͬ�������ڴ�������ͣ����ͬʱ��ʱ����ͬ�¶���COS��ת���ʣ�δ�ﵽƽ�⣩��ͼ1��ʾ��ij�¶��£�COS��ƽ��ת������n(H2O)/n(COS)�Ĺ�ϵ��ͼ2��ʾ��
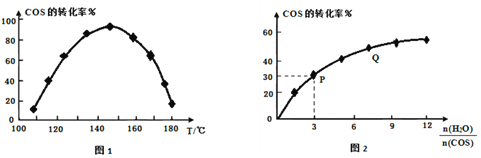
��ͼ1��֪�������������ʱ��Ӧ���¶�ԼΪ______��COS��ת�����ں����½���ԭ����_______________________________________����ͼ2��֪��P��ʱƽ�ⳣ��K=______������2λ��Ч���֣���Q��ת���ʸ���P���ԭ����__________________________________��
���𰸡� H2S![]() H++HS- ��HS-
H++HS- ��HS-![]() H++S2- O=C=S COS+4Br2+12OH-=CO32-+SO42-+8Br-+6H2O 285 150 �����ж�����������Ӧ�Ⱥ����𰸣�ƽ�������ƶ��������һ�ɲ����֣� 0.048 ��ͬ������n(H2O)/n(COS)Խ�ߣ��൱��COSŨ�Ȳ�������£�����ˮ����Ũ�ȣ�ƽ�������ƶ���COSת�������
H++S2- O=C=S COS+4Br2+12OH-=CO32-+SO42-+8Br-+6H2O 285 150 �����ж�����������Ӧ�Ⱥ����𰸣�ƽ�������ƶ��������һ�ɲ����֣� 0.048 ��ͬ������n(H2O)/n(COS)Խ�ߣ��൱��COSŨ�Ȳ�������£�����ˮ����Ũ�ȣ�ƽ�������ƶ���COSת�������
��������(1) H2S��ˮ��Һ�������ᣬ�����ᣬ���ֲ����룬��H2S![]() H++HS- ��HS-
H++HS- ��HS-![]() H++S2-������ֻдH2S
H++S2-������ֻдH2S![]() H++HS-��
H++HS-��
(2) ��CO2�ķ��ӽṹ�Ǻ�C=O��ֱ�����ɣ�����COS�ķ��ӽṹʽΪS=C=O����Br2��KOH��Һ������COSʱ��������Br����S��������أ�C���ɵ�CO2�ڼ�����Һ��ת��ΪCO32-�����Է�Ӧ�����ӷ���ʽΪCOS+4Br2 +12OH��= CO32-+SO42-+8Br��+6H2O������������������ȼ���ȵ��Ȼ�ѧ����ʽ�����ø�˹���ɼ����������H=(285kJ/mol+299kJ/mol)-(586kJ/mol+283kJ/mol)=-285 kJ/mol������ͼ1��֪������ͬʱ���ڣ�ת�������ʱ���������������Ӧ���¶�Ϊ150�����¶ȹ��ߣ�ʹ������ѻ��Լ�����ɥʧ���������ж�������ת���ʼ�С����ͼ2��֪��P��ʱCOS��ת����Ϊ30%��n(H2O)/n(COS)=3���������¹�ϵ��
COS(g)+H2O(g) ![]() CO2(g)+H2S(g)
CO2(g)+H2S(g)
��ʼ���ʵ���(mol) 1 3 0 0
�ı����ʵ���(mol) 0.3 0.3 0.3 0.3
ƽ�����ʵ���(mol) 0.7 2.7 0.3 0.3
��K=![]()
��ͬ������n(H2O)/n(COS)�ı�ֵԽ�ߣ��൱��COSŨ�Ȳ�������£�����Ӧ��ˮ����Ũ�ȣ��ٽ���ѧƽ�������ƶ��������COSת���ʡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������CCl4��ȡ��ˮ�� ˵���в���ȷ����
A. ����CCl4�е��ܽ�ȴ�����ˮ�е��ܽ��
B. ��ȡ��ˮ����ɫ��dz
C. ��ȡ��CCl4��Һ��Ϊ��ɫ
D. ��ȡ��ˮ����ɫ��������²�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������CuSO4��Һ��Fe(OH)3����������ȷ���� �� ��
A.���߶��ܲ��������ЧӦ
B.���߶����ܲ��������ЧӦ
C.CuSO4��Һ�ܲ��������ЧӦ��Fe(OH)3���岻�ܲ��������ЧӦ
D.CuSO4��Һ���ܲ��������ЧӦ��Fe(OH)3�����ܲ��������ЧӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У��ܹ�����ĵ������
A. Cu B. ���ڵ�MgCl2 C. ����������Һ D. ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ƾ��壨Na2MoO4��2H2O��������������ȼ������������ˮϵͳ�Ľ������Ƽ�����ͼ�������⾫����Ҫ�ɷ���MoS2��������PbS�ȣ�Ϊԭ�����������ƾ���Ĺ�������ͼ��

�ش��������⣺
��1����߱���Ч�ʵķ�����____________����дһ�֣�
��2�������ա�ʱMoS2ת��ΪMoO3���÷�Ӧ���̵Ļ�ѧ����ʽΪ________________________������������________��д��ѧʽ����
��3���������ʱ���⻯���������Ҫ��Ӧ�Ļ�ѧ����ʽΪ__________________________��
��4���������ؽ������ӡ�ʱ����ij�����ΪNa2S��������ɷֵĻ�ѧʽΪ________��
��5����á����ؽ������ӡ��в������ӵ�Ũ�ȣ�c(MoO42-)=0.40mol/L��c(SO42-)=0.04mol/L�����ᾧ��ǰ���ȳ�ȥSO42-�������Ǽ���Ba(OH)2���塣�������Ba(OH)2�������Һ������䣬��SO42-��ȫ������c(SO42-)��1.0��10-5mol/L��ʱ��BaMoO4�Ƿ��������____________________________________���������˵����[��֪��Ksp(BaSO4)=1.1��10-10��Ksp(BaMoO4)=4.0��10-8]
��6���⾫���ڼ��������£�����NaClO��Һ��Ҳ�����Ʊ������ƣ�ͬʱ��SO42-���ɣ��÷�Ӧ�����ӷ���ʽΪ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A. NaHSO4ˮ��Һ��ʹʯ���죬��NaHSO4������
B. �е��ʲμӻ��е������ɵķ�Ӧһ����������ԭ��Ӧ
C. ����������һ���Ƿǽ���������
D. 1molCl2�������22.4L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������MgCO3�������Һ�еμ�����Ũ���ᣨ��������仯����������ֵ��С���ǣ�������
A.c��CO32����
B.c��Mg2+��
C.c��H+��
D.Ksp��MgCO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ��������������ȷ����( )
A. 1mol Cl2�μӻ�ѧ��Ӧ��ת�Ƶĵ�����һ��Ϊ2NA
B. 7.8g Na2O2 ������������������Ϊ0.4NA
C. 15.6 g Na2O2�����CO2��Ӧʱ��ת�Ƶĵ�����Ϊ0.2NA
D. ��״���£���0.5mol NO��0.5mol O2��ɵĻ�����壬������ԼΪNA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com