
【题目】下列说法说法正确的是
A.外接电源保护水中钢闸门时,应将钢闸门与电源的正极相连
B.向Na2CO3溶液中加入少量BaCl2固体,CO32-水解程度增大,溶液的pH减小
C.如图表示常温下稀释pH=11的NaOH溶液和氨水时溶液pH的变化,曲线Ⅱ表示氨水
D.2NO(g)+2CO(g)===N2(g)+2CO2(g)在常温下能自发进行,则该反应的ΔH>0
【答案】B
【解析】
A.外接电源保护水中钢闸门时,应将钢闸门与电源的负极相连,故A错误;
B.Na2CO3溶液中,由于碳酸根离子水解使溶液显碱性,向溶液中加入少量BaCl2固体,CO32-与Ba2+结合形成碳酸钡沉淀,碳酸根离子的浓度减小, CO32-水解程度增大,浓度的影响更显著,溶液中氢氧根离子浓度减小,溶液的pH减小,故B正确;
C.等pH的强碱与弱碱,稀释相同倍数时,强碱的pH变化大,弱碱存在电离平衡,则图中Ⅰ表示氨水稀释的情况,故C错误;
D.根据反应,正反应为熵减的反应,即△S<0,常温下能自发进行,根据△HT△S=△G<0反应自发进行,可推知该反应△H<0,故D错误;
答案选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某兴趣小组针对反应![]() 进行研究。下列研究结论正确的是
进行研究。下列研究结论正确的是
A.若向绝热恒容密闭容器中通入一定量的![]() 和
和![]() 进行反应,正反应速率随时间变化的曲线如图Ⅰ所示,则A点反应达到平衡
进行反应,正反应速率随时间变化的曲线如图Ⅰ所示,则A点反应达到平衡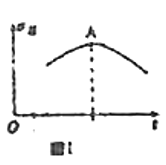
B.若恒温条件下进行反应,Y的平衡转化率![]() 与压强
与压强![]() 的关系如图Ⅱ所示,则B点
的关系如图Ⅱ所示,则B点![]()
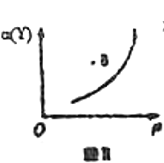
C.若恒温恒容,改变X与Y的投料比![]() 进行反应,平衡时Z的百分含量
进行反应,平衡时Z的百分含量![]() 随
随![]() 变化的曲线如图Ⅲ,则C点
变化的曲线如图Ⅲ,则C点![]()
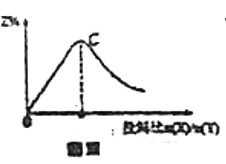
D.若恒容条件下投入一定量的X和Y边加热边进行反应,X的体积分数![]() 随温度的变化如图Ⅳ所示,则该反应反应物的总能量高于生成物的总能量
随温度的变化如图Ⅳ所示,则该反应反应物的总能量高于生成物的总能量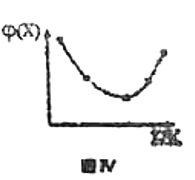
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述正确的是( )
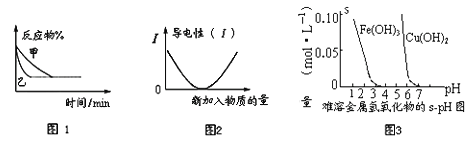
A. 图1可能表示压强对可逆反应A(g)+2B(g) ![]() 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
B. 图2可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
C. 据图3,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量Cu至pH到4左右
D. 当反应COCl2(g) ![]() CO(g) + Cl2(g) △H>0,达到平衡时①升温②减压③加催化剂都能提高COCl2转化率
CO(g) + Cl2(g) △H>0,达到平衡时①升温②减压③加催化剂都能提高COCl2转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨电极完成下列电解实验
实验一 | 实验二 | |
装置 |
|
|
现象 | a、d处试纸变蓝;b处变红,局部褪色;c处无明显变化 | 两个石墨电极附近有气泡产生;n处有气泡产生…… |
下列对实验现象的解释或推测不合理的是( )
A. a、d处:2H2O+2e-=H2↑+2OH- B. b处:2Cl--2e-=Cl2↑
C. c处发生了反应:Fe-2e-=Fe2+ D. 根据实验一的原理,实验二中m处能析出铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如下:

下列说法错误的是( )
A.反应①阶段,参加反应的NaClO3和SO2的物质的量之比为2:1
B.若反应①通过原电池来实现,则ClO2是正极产物
C.反应②中的H2O2可用NaClO4代替
D.反应②条件下,ClO2的氧化性大于H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素铈(Ce)是一种重要的稀土元素。
(1) 工业上用氟碳铈矿(主要成分为CeFCO3)制备CeO2。焙烧过程中发生的主要反应的化学方程式为________。

(2) 已知CeCl3·7H2O在空气中易被氧化成四价铈,反应如下:
① CeCl3·7H2O(s)=CeCl3(s)+7H2O(g);ΔH1=a kJ·mol-1
② 4CeCl3(s)+O2(g)+14H2O(g)=4Ce(OH)4(s)+12HCl(g);ΔH2=b kJ·mol-1
③ Ce(OH)4(s)=CeO2(s)+2H2O(g);ΔH3=c kJ·mol-1
则4CeCl3·7H2O(s)+O2(g)=4CeO2(s)+12HCl(g)+22H2O(g);ΔH=________。
(3) CeO2是汽车尾气净化催化剂中最重要的助剂,工作原理如图1所示。写出过程1发生反应的化学方程式:________________________________。

(4) 已知Ce(OH)4极易分解,用如图2所示装置电解CeCl3溶液在阴极区制得CeO2。电解过程中反应体系的pH随时间t的变化曲线如图3所示。
①电解进行1h内溶液的pH迅速下降,可能原因是________。
②请解释生成CeO2的原理:________。
(5) 常温下,当溶液中某离子浓度≤1.0×10-5时,可认为该离子沉淀完全。用Na2C2O4溶液对电解后的废液处理得到Ce2(C2O4)3固体,则应保持溶液中c(C2O42-)约为________。(已知25 ℃时,Ksp[Ce2(C2O4)3]=1.0×10-25)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是合成一种治疗癌症的药物的中间体,其合成路线如下:
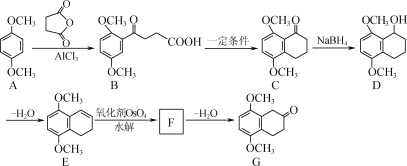
已知:
(1) C中含氧官能团为________(填名称)。
(2) D→E的反应类型为________。
(3) F的结构简式为________。
(4) G的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:________。
①能发生银镜反应;② 水解产物之一能与FeCl3显色;③ 核磁共振氢谱显示有四组峰。
(5) 已知:RCOOH ![]()
![]() 请根据已有知识并结合相关信息,写出以
请根据已有知识并结合相关信息,写出以![]() 、HOOCCH2CH2COOH为原料制备
、HOOCCH2CH2COOH为原料制备![]() 的合成路线(无机试剂任用,合成路线流程图示例见本题题干)。___________
的合成路线(无机试剂任用,合成路线流程图示例见本题题干)。___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用如图所示A、B装置分别探究金属锌与稀硫酸的反应,实验过程中A装置烧杯内的溶液温度升高,B装置的电流计指针发生偏转。
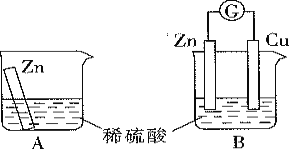
(1)A装置的烧杯中发生反应的离子方程式为______________。
(2)B装置中Zn板是________极;Cu板上的现象是________,其发生的电极反应式是_____ 。若有1 mol电子流过导线,则正极生成的产物的物质的量为_______ 。
(3)从能量转化的角度看,A、B中反应物的总能量________(填“大于”“小于”或“等于”)生成物的总能量,A中主要是将化学能转化为__________,B中主要是将化学能转化为___________。
(4)该小组同学反思原电池的原理,其中观点正确的是___________(填字母)。
A 原电池反应的过程中可能没有电子发生转移 B 原电池装置需要2个电极
C 电极一定不能参加反应 D 氧化反应和还原反应可以拆开在两极发生
(5)有人以化学反应:2Zn+O2+4H+=2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则该原电池的正极发生的电极反应为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,将NO2加热到某温度时,可进行如下反应:2NO2(g) ![]() 2NO(g)+O2(g),达到平衡时各物质的浓度分别是c(NO2)=0.06 mol·L-1,c(NO)=0.24 mol·L-1,c(O2)=0.12 mol·L-1。试求:
2NO(g)+O2(g),达到平衡时各物质的浓度分别是c(NO2)=0.06 mol·L-1,c(NO)=0.24 mol·L-1,c(O2)=0.12 mol·L-1。试求:
(1)该反应的化学平衡常数表达式为:_______ ,值为_______。
(2)开始时NO2的浓度为_______。
(3)NO2的转化率为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com