
【题目】利用反应CCl4 +4Na![]() C(金刚石)+4NaCl可实现人工合成金刚石。下列关于该反应的说法错误的是( )
C(金刚石)+4NaCl可实现人工合成金刚石。下列关于该反应的说法错误的是( )
A.C(金刚石)属于原子晶体
B.该反应利用了Na的强还原性
C.CCl4和C(金刚石)中的C的杂化方式相同
D.NaCl晶体中每个Cl-周围有8个Na+
科目:高中化学 来源: 题型:
【题目】芳香化合物A(C9H9O3Br)可以发生如图所示的转化,合成两种重要的高分子化合物G和H(其他产物和水已略去)。

已知A遇氯化铁溶液显紫色,请回答下列问题:
(1)B的结构简式为____________,其核磁共振氢谱图显示有______种不同环境的氢原子。
(2)D的名称是________________;C和E生成H的反应类型为 _______________
(3)1molA与足量NaOH 溶液充分反应,消耗NaOH的物质的量为____________
(4)C生成D的化学方程式为________________________
(5)W是B的同系物,比B多一个碳原子, 符合下列条件的W的同分异构体有______种。
①遇氯化铁溶液显紫色
②既能发生水解反应又能发生银镜反应
(6)参照上述合成路线,根据信息,以乙醇为原料(无机试剂任选)设计制备 的合成路线_______________
的合成路线_______________
ⅰ.![]()
![]()
![]() +H2O(R1、R2为烃基或氢)
+H2O(R1、R2为烃基或氢)
ⅱ.R-HC![]() CH-R'
CH-R'![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I已知25℃时,醋酸、碳酸、氢氰酸的电离平衡常数如下表(单位省略):
醋酸 | 碳酸 | 氢氰酸 |
Ka=1.7×10-5 | Ka1=4.2×10-7 Ka2=5.6×10-11 | Ka=6.2×10-10 |
(1)写出碳酸的第一步电离方程式___。
(2)25℃时,等浓度的三种溶液①NaCN溶液、②Na2CO3溶液、③CH3COONa溶液,pH由大到小的顺序为___(填序号)。
(3)25℃时,向NaCN溶液中通入少量CO2,反应的离子方程式为___。
(4)将浓度为0.02mol/L的HCN与0.01mol/LNaOH溶液等体积混合,测得混合溶液中c(Na+)>c(CN-),下列关系正确的是___。
a.c(H+)>c(OH-) b.c(H+)+c(HCN)=c(OH-) c.c(HCN)+c(CN-)=0.01mol/L
(5)25℃时,浓度均为0.01mol/L的①NaCN、②CH3COONa、③NaCl溶液中,阴离子总浓度由大到小的顺序为___(填序号)。
Ⅱ.酸性高锰酸钾标准溶液是实验室常用的氧化还原滴定标准试剂。
(6)某同学用0.1000mol/L的酸性高锰酸钾标准溶液滴定某试样中过氧化氢的含量,反应原理为2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑。
①滴定时,用___装KMnO4溶液。
②滴定到达终点的现象是___。
③用移液管吸取25.00m试样置于锥形瓶中,重复滴定四次,每次消耗的酸性KMnO4标准溶液体积如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
体积(mL) | 17.10 | 18.10 | 17.00 | 16.90 |
则试样中过氧化氢的浓度为___mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2 mol N2(g)和1 mol H2(g)置于2L密闭容器中,在一定温度下发生反应:N2(g)+3H2(g)![]() 2NH3(g) H<0,其他条件不变时,改变某一条件对上述反应的影响,得出下列关系图:
2NH3(g) H<0,其他条件不变时,改变某一条件对上述反应的影响,得出下列关系图:


下列说法正确的是
A.图Ⅰ研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B.图Ⅱ研究的是压强对反应的影响,且乙的压强较高
C.图Ⅱ研究的是温度对反应的影响,且乙的温度较高
D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是人类赖以生存的基础。回答下列问题:
(1)下列不属于新能源的是________(填字母)。
a.煤炭 b.太阳能 c.风能 d.地热能
(2)已知:
Ⅰ.H2(g)+![]() O2(g)=H2O(g) H1=-241.8kJmol-1
O2(g)=H2O(g) H1=-241.8kJmol-1
Ⅱ.H2(g)+![]() O2(g)=H2O(l) H2=-285.8kJmol-1
O2(g)=H2O(l) H2=-285.8kJmol-1
气态分子中的化学键 | 断开1 mol化学键所需的能量/kJ |
O-H | 465 |
O=O | 498 |
①氢气的燃烧热为________kJmol-1.
②断开1 mol H-H键需要吸收的能量为________kJ。
③36 g H2O(1)完全分解生成氧气和氧气,需要吸收________kJ的能量。
(3)金刚石和石墨为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时完全燃烧生成二氧化碳,反应中放出的热量如图所示。
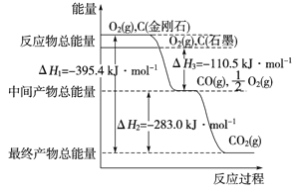
①在通常状况下,金刚石和石墨的稳定性较大的是________ (填“金刚石”或“石墨”)。
②12 g石墨在一定量空气中燃烧,生成36g气体,该过程放出的热量为________kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 X(g)+Y(g) ![]() 2Z(g) △H<0,在一定条件下,反应情况如图所示.若使曲线b变为曲线a可采取的措施是
2Z(g) △H<0,在一定条件下,反应情况如图所示.若使曲线b变为曲线a可采取的措施是
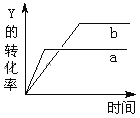
A.加入催化剂B.增大压强
C.升高温度D.保持容器体积不变,冲入He气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用小粒径零价铁(ZVI)的电化学腐蚀处理三氯乙烯,进行水体修复的过程如图所示。H+,O2,NO3-等共存物的存在会影响水体修复效果,定义单位时间内ZVI释放电子的物质的量为nt,其中用于有效腐蚀的电子的物质的量为ne。下列说法错误的是( )

A. 反应①②③④均在正极发生
B. 单位时间内,三氯乙烯脱去amolCl时ne=amol
C. ④的电极反应式为NO3-+10H++8e-=NH4++3H2O
D. 增大单位体积水体中小粒径ZVI的投入量,可使nt增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+3B(g) ![]() 2C(g)+2D(g)在四种不同情况下的反应速率分别为
2C(g)+2D(g)在四种不同情况下的反应速率分别为
①v(A)=0.45 mol·L-1·min-1 ②v(B)=0.6 mol·L-1·s-1 ③v(C)=0.4 mol·L-1·s-1 ④v(D)=0.45 mol·L-1·s-1,该反应进行的快慢顺序为
A. ④>③=②>① B. ④<③=②<① C. ①>②>③>④ D. ④>③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数用![]() 表示,下列叙述正确的是
表示,下列叙述正确的是![]()
①![]() 含有电子数为
含有电子数为![]()
②![]() 中含有的
中含有的![]() 键总数目为
键总数目为![]()
③![]()
![]() 与
与![]() 完全反应时转移电子数为
完全反应时转移电子数为![]()
④![]() 硅晶体中含有
硅晶体中含有![]() 个
个![]() 键
键
⑤![]() 通入足量氢氧化钠溶液中充分反应,转移的电子数等于
通入足量氢氧化钠溶液中充分反应,转移的电子数等于![]()
⑥![]() ,
,![]()
![]() 溶液中,
溶液中,![]() 和
和![]() 离子数的总和是
离子数的总和是![]()
⑦在常温常压下,![]() 铁与
铁与![]()
![]() 充分反应,转移的电子数为
充分反应,转移的电子数为![]()
⑧![]() 和
和![]() 的混合物共
的混合物共![]() ,其中所含原子数一定为
,其中所含原子数一定为![]() .
.
A.①②③⑤⑧B.②④⑥⑦⑧C.①③⑤⑥⑦D.①②④⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com