
| A. | 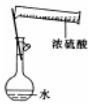 配制一定物质的量浓度的稀硫酸 | B. | 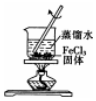 制取少量的Fe(OH)3胶体 | ||
| C. | 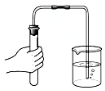 检查气密性 | D. | 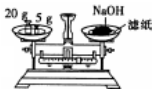 称量NaOH固体 |
分析 A.不能在容量瓶中稀释;
B.氯化铁溶于水得到溶液;
C.双手紧握试管,观察烧杯中气泡冒出;
D.NaOH潮解,具有腐蚀性,应在小烧杯中称量.
解答 解:A.不能在容量瓶中稀释,应在烧杯中稀释、冷却后转移到容量瓶中定容,故A错误;
B.氯化铁溶于水得到溶液,应在沸水中滴饱和氯化铁溶液制备胶体,故B错误;
C.双手紧握试管,观察烧杯中气泡冒出,则图中装置可检验气密性,故C正确;
D.NaOH潮解,具有腐蚀性,图中NaOH应在左侧托盘且小烧杯中称量,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、溶液的配制、胶体制备、实验操作为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:填空题
 ) 可以通过不同的反应得到②~⑤四种物质.
) 可以通过不同的反应得到②~⑤四种物质.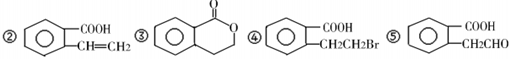
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4与 Ba(OH)2 溶液反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O | |
| B. | 金属钠与水的反应:Na+H2O═Na++OH-+H2↑ | |
| C. | 向足量NaHCO3溶液中滴人少量Ca(OH)2溶液:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| D. | 常温下,将氯气通人水中:Cl2+H2O═2H++2Cl-+ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热 | |
| B. | 分液操作时,静置分层后要先放出分液漏斗中下层液体,再倒出上层液体 | |
| C. | 分液操作时,选择的萃取剂的密度必须比水大 | |
| D. | 用胶头滴管向试管滴加液体时,滴管尖端靠在试管内壁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO32- | B. | CO32-、NO3- | C. | NO3- | D. | CO32-、NO3-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
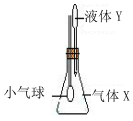 在如图所示示装置中,将液体Y滴入瓶中并摇动,一会儿小气球胀大.则气体X与液体Y可能是( )
在如图所示示装置中,将液体Y滴入瓶中并摇动,一会儿小气球胀大.则气体X与液体Y可能是( )| A | B | C | D | |
| 气体X | NH3 | SO2 | CO2 | HCl |
| 液体Y | 稀硫酸 | 浓NaOH | 饱和NaHCO3 | 水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
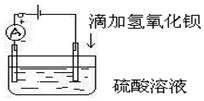 如图所示是某化学兴趣小组探究溶液中离子浓度与溶液导电性的关系.
如图所示是某化学兴趣小组探究溶液中离子浓度与溶液导电性的关系.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com