
【题目】归纳总结是学习化学的一种方法。
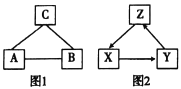
(1)甲同学发现A、B、C三种物质有如图l所示的相互反应关系,“—”表示能反应(部分反应物、生成物以及反应条件省略,下同)。己知A是常见金属,人体缺乏组成A的元素易患贫血症;B胃酸的主要成分;B与C反应产生不溶于稀硝酸的白色沉淀,则A是____(填化学式,下同,C是_______。请写出下列反应的化学方程式:A与B________________;B与C____________________。
(2)乙同学发现X、Y、Z三种物质有如图2所示的循环转化关系“→”表示能转化。
①若X、Y、Z均为含钙化合物,X是一种常用干燥剂,Y俗称熟石灰。则X的化学式为______;请写出Y→Z的反应化学方程式________________。
②若X是碳单质,Y、Z是含有碳元素的氧化物,X、Y、Z的相对分子质量依次增大,则Y的相对分子质量为 ;Z→X可通过以下反应实现:___________________;该反应的基本反应类型是 。
【答案】(1)Fe;AgNO3;Fe+2HCl=FeCl2+H2↑;HCl+AgNO3=AgCl↓+HNO3;
(2)①CaO;Ca(OH)2+CO2=CaCO3+H2O;②28;2Mg+CO2![]() 2MgO+C;置换反应。
2MgO+C;置换反应。
【解析】
试题分析:(1)A是常见金属,人体缺乏组成A的元素易患贫血症,所以A是铁,B是胃酸的主要成分,所以B盐酸,盐酸与C反应产生不溶于稀硝酸的白色沉淀,所以C是硝酸银,铁和盐酸反应生成氯化亚铁和氢气,盐酸和硝酸银反应生成白色的氯化银沉淀和硝酸,铁和硝酸银反应生成硝酸亚铁和银,推出的物质满足题中的转化关系。故A是Fe,C是AgNO3,A与B的反应是铁和盐酸反应生成氯化亚铁和氢气,化学方程式为:Fe+2HCl=FeCl2+H2↑,B与C的反应是盐酸和硝酸银反应生成氯化银沉淀和硝酸,化学方程式为:HCl+AgNO3=AgCl↓+HNO3;(2)①X、Y、Z均为含钙化合物,X是一种常用干燥剂,所以X是氧化钙,Y俗称熟石灰,所以Y是氢氧化钙,依据X、Y、Z三种物质的转化关系可知,Z是碳酸钙,氧化钙和水反应会生成氢氧化钙,氢氧化钙和二氧化碳反应会生成碳酸钙,碳酸钙高温会生成二氧化碳,推出的各种物质均满足题中的转化关系。故X的化学式为CaO,Y→Z的反应是氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3+H2O;②X是碳单质,Y、Z是含有碳元素的氧化物,X、Y、Z的相对分子质量依次增大,依据X、Y、Z三种物质的转化关系可知,Y是一氧化碳,Z是二氧化碳,木炭和氧气反应生成一氧化碳,一氧化碳和氧气反应生成二氧化碳,二氧化碳和活泼金属反应生成碳单质和金属氧化物,木炭、一氧化碳、二氧化碳相对分子质量依次增大,推出的各种物质均满足题中的转化关系。所以Y是一氧化碳,相对分子质量为28,CO2发生反应的化学方程式是2Mg+CO2![]() 2MgO+C,由于反应物是单质和化合物,生成物是一种新的单质和化合物,满足置换反应的条件,所以该反应属于置换反应。
2MgO+C,由于反应物是单质和化合物,生成物是一种新的单质和化合物,满足置换反应的条件,所以该反应属于置换反应。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】化学在生活中有着广泛的应用,下列对应关系错误的是
化学性质 | 实际应用 | |
A | 乙酸具有酸性 | 常用于除水垢 |
B | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
C | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
D | HF与SiO2反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关基本营养物质的说法中,错误的是
A.淀粉遇碘化钾溶液变蓝
B.葡萄糖和果糖互为同分异构体
C.利用油脂在碱性条件下水解可制取肥皂
D.用灼烧并闻气味的方法鉴别羊毛织物和棉织物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“3G”手机出现后,以光导纤维为基础的高速信息通道尤显重要.下列物质中用于制造光导纤维的材料是( )
A.铜合金 B.陶瓷 C.聚乙烯 D.二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化合物的用途叙述正确的是
A.光纤通信使用的光缆的主要成分是晶体Si,太阳能电池使用的材枓主要娃SiO2
B.水玻璃可用作防火剂或防腐剂
C.高锰酸钾溶液、酒精、双氧水都能杀菌消毒,消毒原理相同,都利用了强氧化性
D.SO2可用来漂白纸浆、毛、丝、草帽辫、增白食品等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电离平衡常数是衡量弱电解质电离程度的量。已知如下表数据(25 ℃):
化学式 | 电离平衡常数 |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
(1)25 ℃时,等浓度的三种溶液(A.NaCN溶液、B.Na2CO3溶液、C.CH3COONa溶液)的pH由大到小的顺序为________________________________。(填写序号)
(2)25 ℃时,向NaCN溶液中通入少量CO2,所发生反应的化学方程式为______ ___。
(3)现有浓度为0.02 mol/L的HCN与0.01mol/L NaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是 。
A.c(H+)>c(OH-)
B.c(H+)<c(OH-)
C.c(H+)+c(HCN) = c(OH-)
D.c(HCN)+ c(CN-)=0.01mol/L
(4)浓的Al2(SO4)3溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理_____________________。
(5)已知NaHC2O4水溶液显酸性,请写出该溶液中各离子浓度的大小___________________;电荷守恒表达式 ___________________ 。
(6)H2C2O4溶液和KMnO4酸性溶液可发生反应:H2C2O4+MnO4-+H+→CO2+Mn2++H2O,反应中每生成标况下4.48LCO2气体,转移的电子的物质的量为__________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质在溶液中的行为是化学研究的重要内容。下列有关溶液的叙述不正确的是
A.加热蒸干NaCl、MgCl2溶液时可以得到晶体NaCl、MgCl2
B.相同条件下,等物质的量浓度的溶液导电能力:HC1>NH3·H2O
C.溶液中离子结合质子(氢离子)的能力:C2O42—>HC2O4—>SO42—
D.海洋封存CO2会导致局部海洋水体酸性增强,会破坏海洋生态环境
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸。下图是工业上用印刷电路的蚀刻液的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程:

按要求回答下列问题:
⑴ 废液①的主要含有的金属阳离子是__________(填化学符号,下同);废渣①的成分是_____________,Y为__________。
⑵废液①与Z反应的离子方程式为:______________________。
⑶ 写出废渣②生成二氧化硫的化学方程式_____________________。
⑷ 为得到纯净的CuCl晶体,可用下列_________(填序号)进行洗涤。
a.纯净水 b.乙醇 c.稀硫酸 d.氯化铜溶液
⑸ 生产过程中调节溶液的pH不能过大的原因是___________________。
⑹ 写出产生CuCl的离子方程式_______________________。
⑺ 氯化亚铜的定量分析:
① 称取样品0.25g加入10mL过量的FeCl3溶液250mlL锥形瓶中,不断摇动;
② 待样品溶解后,加水50mL和2滴指示剂;
③ 立即用0.10 mol·L-1硫酸铈标准溶液滴至绿色出现为终点;
④ 重复三次,消耗硫酸铈溶液平均体积为25.00mL。
已知:CuCl的分子式量为99;CuCl + FeCl3 = CuCl2 + FeCl2; Fe2+ + Ce4+ = Fe3+ + Ce3+。
则CuCl的纯度为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com