
����Ŀ���Ȼ���ͭ��CuCl���������л��ϳɹ�ҵ�еĴ�������һ�ְ�ɫ��ĩ������ˮ���������Ҵ���ϡ���ᡣ��ͼ�ǹ�ҵ����ӡˢ��·��ʴ��Һ�ķ�Һ����Fe3+��Cu2+��Fe2+��Cl��������CuCl�����̣�

��Ҫ��ش��������⣺
�� ��Һ�ٵ���Ҫ���еĽ�����������__________���ѧ���ţ���ͬ�����������ijɷ���_____________��YΪ__________��
����Һ����Z��Ӧ�����ӷ���ʽΪ��______________________��
�� д�����������ɶ�������Ļ�ѧ����ʽ_____________________��
�� Ϊ�õ�������CuCl���壬��������_________�������������ϴ�ӡ�
a������ˮ b���Ҵ� c��ϡ���� d���Ȼ�ͭ��Һ
�� ���������е�����Һ��pH���ܹ����ԭ����___________________��
�� д������CuCl�����ӷ���ʽ_______________________��
�� �Ȼ���ͭ�Ķ���������
�� ��ȡ��Ʒ0.25g����10mL������FeCl3��Һ250mlL��ƿ�У�����ҡ����
�� ����Ʒ�ܽ��ˮ50mL��2��ָʾ����
�� ������0.10 mol��L��1���������Һ������ɫ����Ϊ�յ㣻
�� �ظ����Σ�������������Һƽ�����Ϊ25.00mL��
��֪��CuCl�ķ���ʽ��Ϊ99��CuCl + FeCl3 = CuCl2 + FeCl2�� Fe2+ + Ce4+ = Fe3+ + Ce3+��
��CuCl�Ĵ���Ϊ____________��
���𰸡��� Fe2+��1���� Fe��Cu��1���� HCl��1����
�� 2Fe2+ + Cl2 = 2Fe3+ + 2Cl�� �� 2Fe2+ +2H+ + H2O2 = 2Fe3+ + 2H2O ��2���������𰸼�����
�� Cu+2H2SO4��Ũ��![]() CuSO4+ SO2��+2H2O��2������д������1������ b��1����
CuSO4+ SO2��+2H2O��2�����������1������ b��1����
�� ��ֹ����������ͭ�������ֹCuClˮ����2����
�� SO2 + 2Cu2+ + 2Cl�� + 2H2O �T 2CuCl��+ SO42��+ 4H+ ��2���� �� 99% (2��)
��������
�����������ҵ��������ӡˢ��·�ķ�Һ����Fe3+��Cu2+��Fe2+��Cl-��������������ۣ����������������۷�Ӧת��Ϊ���������ӣ�ͭ����������Ӧ����ͭ��Ȼ����ˣ�����Ϊ�������������ɵ�ͭ������ͭ���������ԣ��������������ᣬͭ�������Ӧ�����˵õ�������Ϊͭ����Һ���м���ZΪ��ˮ��˫��ˮ��������������Ϊ�����ӣ��õ�ʴ��Һ��Ȼ��ͭ��Ũ���ᷴӦ��������ͭ�Ͷ�������ͭ��������Ӧ�����Ȼ�ͭ������ͭ�����������Ȼ�ͭ��Ӧ�����Ȼ���ͭ��
��1��ӡˢ��·�ķ�Һ����Fe3+��Cu2+��Fe2+��Cl-���������������������ܹ�ԭ����Ӧ���ɶ��������ӣ�ͭ�����ܹ�������Ӧ����ͭ�����˺������к���ͭ�������������ᣬ�������ᷴӦ�����Ȼ�������ͭ�������Ӧ����ͭ���������
��2���������Ϸ�����֪��Һ����Z��Ӧ�����ӷ���ʽΪ2Fe2+ + Cl2 = 2Fe3+ + 2Cl����2Fe2+ +2H+ + H2O2 = 2Fe3+ + 2H2O��
��3�����������ɶ�������ķ�Ӧ��ͭ��Ũ�����ڼ��������·�Ӧ���ɣ���Ӧ�Ļ�ѧ����ʽΪCu+2H2SO4��Ũ��![]() CuSO4+ SO2��+2H2O��
CuSO4+ SO2��+2H2O��
��4��Ϊ����CuCl����ʧ��������CuCl���岻��ˮ������ˮ�Ҵ�ϴ�ӣ���ѡb��
��5�����������е�����Һ��pH���ܹ����ԭ���Ƿ�ֹ����������ͭ�������ֹCuClˮ�⣻
��6������ͼʾ��֪��CuCl2��CuSO4��SO2��H2O��Ӧ����H2SO4��CuCl������CuCl�Ļ�ѧ����ʽ���ݵ�ʧ�����غ�õ���CuCl2+CuSO4+SO2+2H2O=2CuCl��+2H2SO4����Ӧ�����ӷ���ʽΪ��SO2 + 2Cu2+ + 2Cl�� + 2H2O �T 2CuCl��+ SO42��+ 4H+��
��7���ζ�0.25g��Ʒ�������������Һ��ƽ�������25.00ml����Ϸ���ʽ��֪��CuCl+FeCl3�TCuCl2+FeCl2��CuCl�Ĵ���Ϊ��25.00��103L��0.1mol/L��99g/mol��/0.25g��100%=99%��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ܽ���ѧϰ��ѧ��һ�ַ�����
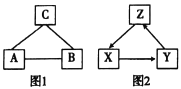
��1����ͬѧ����A��B��C������������ͼl��ʾ�����Ӧ��ϵ����������ʾ�ܷ�Ӧ�����ַ�Ӧ��������Լ���Ӧ����ʡ������ͬ������֪A�dz�������������ȱ�����A��Ԫ����ƶѪ֢��Bθ������Ҫ�ɷ���B��C��Ӧ����������ϡ�����İ�ɫ��������A��____������ѧʽ����ͬ��C��_______����д�����з�Ӧ�Ļ�ѧ����ʽ��A��B________________��B��C____________________��
��2����ͬѧ����X��Y��Z������������ͼ2��ʾ��ѭ��ת����ϵ��������ʾ��ת����
����X��Y��Z��Ϊ���ƻ�������X��һ�ֳ�����������Y�׳���ʯ�ҡ���X�Ļ�ѧʽΪ______����д��Y��Z�ķ�Ӧ��ѧ����ʽ________________��
����X��̼���ʣ�Y��Z�Ǻ���̼Ԫ�ص������X��Y��Z����Է�����������������Y����Է�������Ϊ ��Z��X��ͨ�����·�Ӧʵ�֣�___________________���÷�Ӧ�Ļ�����Ӧ������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����л���C8H16O2��ϡ���������¼��ȵõ�M��N�������ʣ�N���������տɵõ�M����������л���Ľṹ������ ( )
A. 1�� B. 2�� C. 3�� D. 4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʵ�ȼ������ȵ����� ��
A��C��CO B�����Ͱ���
C��3molC2H2����Ȳ����1molC6H6������ D��1gH2��2gH2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A�ǵ��ʣ�D��A��������Ԫ�ص�����������ˮ����ס��ҡ����������ֻ����������붡���������⣬�������ܷ����кͷ�Ӧ����֪������ת����ϵ�����ֲ���ͷ�Ӧ��������ȥ����

�Իش�
(l)д��B�ڹ�ҵ�����е�һ����;��__________________���û�ѧ����ʽ��ʾA�����ڹ�ҵ�����е�һ����;��__________________��
��2��д��Bת��ΪC�Ŀ��ܵ����ӷ���ʽ____________��_____________��
��3����C����Һ�����ԣ������ӷ���ʽ��ʾ�侻ˮ��ԭ��___________________��
��4����CΪ���Σ��ú�m mol C����Һ��1Lnmol/L�������ַ�Ӧ����֪m/n=1/2��������D�����ʵ���Ϊ__________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
(1)����84����Һ�������ʵ���Ũ��ԼΪ________mol��L��1��
84����Һ
��Ч�ɷ� NaClO
��� 1 000 mL
�������� 25%
�ܶ� 1.19 g��cm��3
(2)ijͬѧȡ100mL����84����Һ����ϡ�ͺ�����������ϡ�ͺ����Һ��c(Na��)��______mol��L��1��
(3)��ͬѧ���ĸ���84����Һ�����䷽������NaClO��������480mL��NaClO��������Ϊ25%������Һ������˵����ȷ����________(����ĸ)��
A����ͼ��ʾ�������У��������Dz���Ҫ�ģ�����Ҫһ�ֲ�������
B������ƿ������ˮϴ����Ӧ��ɺ����������Һ����
C�����ƹ����У�δ������ˮϴ���ձ��Ͳ��������ܵ��½��ƫ��
D����Ҫ����NaClO���������Ϊ143.0g
(4)��84����Һ����ϡ������ʹ�ÿ���ǿ����������ij����С����Ա��98%(�ܶ�Ϊ1.84g��cm��3)��Ũ��������2L 2.3mol��L��1��ϡ����������ǿ��84����Һ��������������
�������Ƶ�ϡ�����У�H�������ʵ���Ũ��Ϊ________mol��L��1��
������Ũ��������Ϊ________mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ijNaOH��Һ��ͨ��CO2��������ҺM����CO2ͨ�����IJ�ͬ����ҺM�����Ҳ��ͬ������M����μ������ᣬ�������������V��CO2���������������V��HCl���Ĺ�ϵ������ͼʾ�������������2������OA��AB����3������OA��AB����4������OA > AB,�����з������жϲ���ȷ����������CO2���ܽ���

A��ͼ��1����ʾM��һ���У�c��Na+����c��HCO3������c��OH������c��H2CO3����c��CO32����
B��ͼ��2����ʾM��һ���У�c��NaHCO3����c��Na2CO3��
C��ͼ��3����ʾM��һ���У�c��Na������c��HCO3������2c��CO32������c��OH������c��H +��
D��ͼ��4����ʾM�е������ǣ�NaOH��Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���ܻ�óɹ�����
A��140��ʱ����ˮ�Ҵ���Ũ���Ṳ�ȿ��Ʊ���ϩ
B������֬�м�ϡ������֮���ȿɷ���������Ӧ
C����������Ƿ�ˮ����ȫ������ˮ��Һ�мӵ���Һ�۲��Ƿ����
D����֤�������е���Ԫ�أ���ֱ�Ӽ�AgNO3��Һ�۲��Ƿ��е���ɫ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij�л���X�Ľṹ��ʽΪ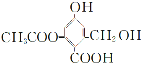 �������й�������ȷ����
�������й�������ȷ����
�� 1 mol X�ֱ���������Na��NaOH��Һ��NaHCO3��Һ��Ӧ���������������ʵ����ʵ����ֱ�Ϊ3 mol��4 mol��1 mol
��X��һ������������FeCl3��Һ������ɫ��Ӧ
��X��һ���������ܷ�����ȥ��Ӧ��������Ӧ
��X�Ļ�ѧʽΪC10H8O6
A���٢� B���٢� C���ڢ� D���ۢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com