
| A. | Ca2+[:$\underset{\stackrel{••}{Cl}}{••}$:]2- | B. | Na+[$\stackrel{•}{X}$$\underset{\stackrel{••}{S}}{••}$$\stackrel{•}{X}$]-2Na+ | ||
| C. | [Mg2+][$\underset{X}{•}$$\underset{\stackrel{••}{O}}{••}$$\underset{X}{•}$]2- | D. | K+[$\stackrel{•}{X}$$\underset{\stackrel{••}{F}}{••}$:]- |
分析 A.氯化钙为离子化合物,氯离子不能合并;
B.硫离子符合错误;
C.镁离子符合错误;
D.KF为离子化合物,由钾离子和F-构成,阴离子用中括号,F周围有8个电子.
解答 解:A.氯化钙为离子化合物,电子式为电子式为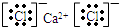 ,故A错误;
,故A错误;
B.硫化钠为离子化合物,由钠离子与硫离子构成,电子式为 ,故B错误;
,故B错误;
C.MgO为离子化合物,电子式为 ,故C错误;
,故C错误;
D.KF为离子化合物,由钾离子和F-构成,阴离子用中括号,F周围有8个电子,电子式为 ,故D正确;
,故D正确;
故选D.
点评 本题考查电子式,为高频考点,把握物质的结构、构成微粒、电子式的书写方法等为解答的关键,侧重分析与应用能力的考查,注意阴离子符号的书写,题目难度不大.


科目:高中化学 来源: 题型:实验题

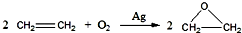
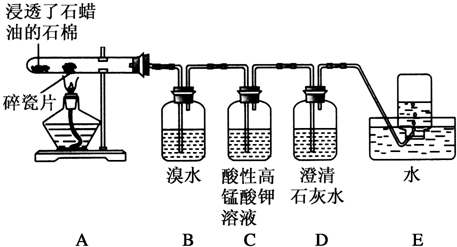
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 组别 | 温度 | KI溶液 | H2SO4溶液 | 淀粉溶液 | 实验目的 | ||
| c(KI) | V | c(H2SO4) | V | ||||
| 1 | 298K | 1mol/L | 5mL | 0.1mol/L | 5mL | 3滴 | 1组和2组探究②0.2mol/L温度对该反应速率的影响;1组和3组探究反应物浓度对该反应速率的影响 |
| 2 | 308K | 1mol/L | 5mL | 0.1mol/L | 5mL | 3滴 | |
| 3 | 298K | 1mol/L | 5mL | ① | 5mL | 3滴 | |
| 实验方案 | 预期实验现象与结论 |
| 取少量碘水于试管中,滴入几滴淀粉溶液,然后逐滴加入1mol/LKOH溶液,观察现象 | 若蓝色不褪色,则假设二正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 (不考虑空间构型,如有配位键,请标出)
(不考虑空间构型,如有配位键,请标出)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 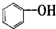 属于醇类化合物 属于醇类化合物 | B. | 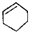 属于芳香族化合物 属于芳香族化合物 | ||
| C. | 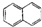 属于脂环化合物 属于脂环化合物 | D. | CH3CH(CH3)2属于链状化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com