
����Ŀ����˹��(FiskerInc.)��˾�������ڿ����Ĺ�̬﮵�������ܶ������е�ص�2.5����������̿ɴ�500Ӣ��(Լ804����)�������ʱ����Է��Ӽƣ������(LiCoO2) ��صĹ���ԭ����ͼ��ʾ��M�������ǽ���﮺�̼�ĸ��ϲ���(̼������﮵�����)�������Ϊһ���ܴ���Li+�ĸ߷��Ӳ��ϡ���Ĥֻ�����ض�������ͨ��������˵����ȷ����
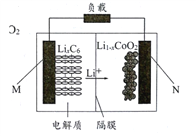
A. ��ص��ܷ�ӦʽΪ:LixC6+Li1-xCoO2==C6+LiCoO2
B. MΪ��ص�����
C. �ŵ�ʱ��NΪ�������缫����������Ӧ
D. ���ʱ��MΪ�������缫����������Ӧ

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���һͭ����ȼ�ϵ�������ߡ��ɱ��ͣ����й����ķ�չǰ�����õ��ͨ��һ�ָ��ӵ�ͭ��ʴ�����������������зŵ����Ϊ2Li+Cu2O+H2O==2Cu+2Li��+2OH��������˵������ȷ����

A. �ŵ�ʱ�������ĵ缫��ӦʽΪCu2O+H2O+2e��=2OH��+2Cu
B. �ŵ�ʱ������������������Li���ƶ�
C. ͨ����ʱ��ͭ�缫����ʴ���������Cu2O
D. ������Ӧ�����У�������ΪO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������CH3COOH�ĵ��볣��K=1.6��10-5��1g4=0.6�����¶��£���20mL0.01 mol��L-1CH3COOH��Һ����μ���0.01 mol��L-1KOH��Һ����pH�仯������ͼ��ʾ(�����¶ȱ仯)������˵����ȷ����
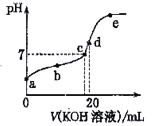
A. �ζ���������ѡ�ü�����ָʾ��
B. a����Һ��c(H+)Ϊ1��10-4 mol��L-1
C. a��b��c��d��e�ĵ���ˮ�ĵ���̶�������e��
D. d ��ʱ���ʵ�ˮ�ⳣ��Ϊ6.25��10-10
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����������ˮ�μӵ�һƬ��ɫʯ����ֽ�ϣ��������ͼ��ʾ�İ뾶�����������������Բ������������ɫ��ͬ�������й�˵��������ȷ���ǣ� ��
A.��ʵ�������ˮ�����ԡ�Ư����
B.�ڻ��ʰ�ɫ����ʺ�ɫ��dz��ɫ
C.�������ɫ�IJ�������˱仯�����У�������ָʾ���ķ�Ӧ��������ԭ��Ӧ��
D.��ˮ���γɴ�����ķ�Ӧ�л�ԭ������HClO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ҷ����һ��ʳƷ���ϣ�������Ҷ������ᷢ��������Ӧ�Ƶá�
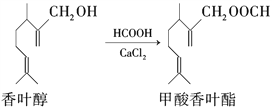
����˵������ȷ����(����)
A. ��Ҷ���ķ���ʽΪC11H18O
B. ��Ҷ����Ũ���ᡢ���������¿ɷ�����ȥ��Ӧ
C. 1mol������Ҷ��������2molH2�����ӳɷ�Ӧ
D. ������Ҷ������������̼ԭ�Ӿ����ܹ�ƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ɽ�д��조ɽˮ�ֳ��С�������о�NOx��SO2�ȴ�����Ⱦ������ƴ���������Ҫ���塣
��1��SO2���ŷ���Ҫ������ú��ȼ�գ���ҵ�ϳ��ð�ˮ���շ�����β���е�SO2����֪���չ�������ط�Ӧ���Ȼ�ѧ����ʽ���£�
SO2(g)+NH3��H2O(aq)![]() NH4HSO3(aq) ��H1=a kJ��mol1��
NH4HSO3(aq) ��H1=a kJ��mol1��
NH3��H2O(aq)+ NH4HSO3(aq)![]() (NH4)2SO3(ag)+H2O(l) ��H 2=b kJ��mol1��
(NH4)2SO3(ag)+H2O(l) ��H 2=b kJ��mol1��
2(NH4)2SO3(aq)+O2(g)![]() 2(NH4)2SO4(aq) ��H 3=c kJ��mol1��
2(NH4)2SO4(aq) ��H 3=c kJ��mol1��
��Ӧ2SO2(g)+4NH3��H2O(aq)+O2(g) ![]() 2(NH4)2SO4(aq)+2H2O(l)�Ħ�H =____kJ��mol1��
2(NH4)2SO4(aq)+2H2O(l)�Ħ�H =____kJ��mol1��
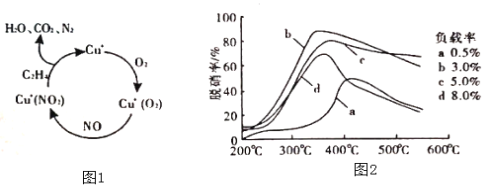
��2������ϩ(C2H4)��Ϊ��ԭ������(NO)������������ͼ1�����ܷ�Ӧ�Ļ�ѧ����ʽΪ_______�����������¶ȡ�������(����ɸ�д�������������)�Ĺ�ϵ��ͼ2��Ϊ�ﵽ�������Ч����Ӧ���õ�������______��
��3��T1�¶�ʱ���ݻ�Ϊ2L�ĺ����ܱ������з�����Ӧ��2NO(g)+O2(g)![]() 2NO2(g) ��H<0��ʵ���ã�����=��(NO)����=2��(O2)����=k��c2(NO)��c(O2)������=(NO2) ����=k��c2(NO2)��k����k��Ϊ���ʳ���ֻ���¶�Ӱ�졣��ͬʱ�̲��������n(NO)��n(O2)�����
2NO2(g) ��H<0��ʵ���ã�����=��(NO)����=2��(O2)����=k��c2(NO)��c(O2)������=(NO2) ����=k��c2(NO2)��k����k��Ϊ���ʳ���ֻ���¶�Ӱ�졣��ͬʱ�̲��������n(NO)��n(O2)�����
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 1 | 0.6 | 0.4 | 0.2 | 0.2 | 0.2 |
n(O2)/mol | 0.6 | 0.4 | 0.3 | 0.2 | 0.2 | 0.2 |
��T1�¶�ʱk��/k��=__________ L/mol��
�������������¶ȸı�ΪT2ʱ��k��=k������T2__________T1(�>������<����=")��
��4����֪��N2(g)+O2(g)![]() 2NO(g) ��H��+181.5 kJ��mol��1��ij����С�鳢�����ù����������ս���NO�ķֽ⡣����
2NO(g) ��H��+181.5 kJ��mol��1��ij����С�鳢�����ù����������ս���NO�ķֽ⡣����![]() ��
��![]() ��
��![]() ��
��![]() �ֱ��ʾN2��NO��O2����������ڹ����������ֽ�NO�Ĺ�����ͼ��ʾ���������������Ĺ����У�����״̬��͵���___(����ĸ���)��
�ֱ��ʾN2��NO��O2����������ڹ����������ֽ�NO�Ĺ�����ͼ��ʾ���������������Ĺ����У�����״̬��͵���___(����ĸ���)��
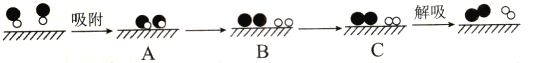
��5�����õ�ⷨ�������¿�����ϡ����NO(O2Ũ��ԼΪNOŨ�ȵ�10��)��װ��ʾ��ͼ���£��������ʿɴ���O2��
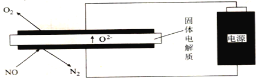
�������ĵ缫��ӦʽΪ______��
������һ������NO�����ĵĵ���ԶԶ�������ۼ����������ܵ�ԭ����(��������������)_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҿ�������ͼʵ��װ�úϳɶ��������ᡣʵ�鲽�����£�
����һ��250 mL������ƿ�м���10 mL������������ʯ����������ƿ������ˮ����ȴ��С�ĵؼ���18 mLŨ���ᡣ
����������ƿ������ԡ�л���������170��180����ά�ִ��¶�2��2.5 h��
������ӦҺ��ȴ��Լ50������ʢ��100 mL��ˮ���ձ��У��ò��������Ͻ��裬��ʹ�������������ˣ���������ˮϴ�ӣ��õ��ľ����Ƕ���������ֲ�Ʒ��
�����ֲ�Ʒ�÷�ˮ�ܽ⣬��ȴ�ᾧ(����Һ��ɫ������û���̿��ɫ)�����ˣ��ռ���Ʒ�����ɡ�(˵����100 mLˮ��20��ʱ���ܽ����������10.8 g����100��ʱ���ܽ�66.7 g)
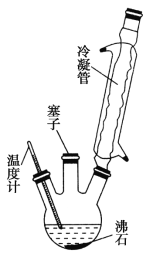
�Իش��������⡣
(1)װ���������ܵ�������___________________��
(2)�������в�����ԡ���ȣ�����˵����ȷ����__________(�����)��
A������ԡ���ȵĺô��Ƿ�Ӧ�����Ⱦ��ȣ����ڿ����¶�
B���˴�Ҳ���Ը���ˮԡ����
C��ʵ��װ���е��¶ȼƿ��Ըı�λ�ã�Ҳ��ʹ��ˮ�������������
(3)��������������ˮϴ�Ӿ���ĺô���______________________��
(4)����������ʱ��Ҫ�����ֲ�Ʒ�÷�ˮ�ܽ⣬��ȴ�ᾧ���������IJ������ж�Σ���Ŀ����_________________________________��
ÿ�ι��˺��Ӧ��ĸҺ�ռ������������ʵ���������Ŀ����__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����600mLij�ֻ������Һ��ֻ���ܺ������������е�������![]()
![]() ��
��![]() ��
��![]() ���ֽ�����Һ�ֳ����ȷݣ���������ʵ��
���ֽ�����Һ�ֳ����ȷݣ���������ʵ��
�����һ���м���AgNO3��Һ���г���������
����ڶ����м�����NaOH��Һ�����Ⱥ��ռ�������0.04 mol����![]() ����Ϊ���ȣ�
����Ϊ���ȣ�
����������м�����BaCl2��Һ�ø���ij���6.27g������������ϴ�ӡ������������Ϊ2.33g��
��������ʵ�飬�����Ʋ������ǣ� ��
A.K+һ������
B.Ba2+��Mg2+һ������
C.Cl- һ������
D.�����Һ��![]() ��Ũ��Ϊ0.1 mol/L
��Ũ��Ϊ0.1 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(��)��
A. ���ݷ�ӦCu��H2SO4![]() CuSO4��H2������֪Cu�Ļ�ԭ�Ա�H2��ǿ
CuSO4��H2������֪Cu�Ļ�ԭ�Ա�H2��ǿ
B. �ڷ�ӦCaH2��2H2O===Ca(OH)2��2H2���У�ˮ��������
C. ��Ӧ3NO2��H2O===2HNO3��NO���������ͻ�ԭ�������ʵ���֮����3��1
D. Cl2��������ǿ��I2�������ԣ����û���ӦI2��2NaClO3===2NaIO3��Cl2���ܷ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com