
【题目】金属活动性顺序是学习化学的重要工具,在工农业生产和科学研究中有重要应用。常见的金属活动性顺序如下:
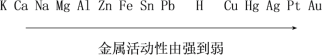
(1)解释不能用铁制容器配制硫酸铜溶液的原因(用化学方程式表示:____________________;
(2)验证镁比锌的金属活动性强,应选用的溶液是________;
(3)从金属活动性顺序中你还能获得哪些信息?(写出一条即可):______________________。
【答案】Fe+CuSO4=Cu+FeSO4 稀盐酸(或稀硫酸、氯化锌等可溶性锌盐溶液) 位于氢前面的金属能置换出酸中的氢(或金属的位置越靠前,它的活动性越强、位于前面的金属可以把位于后面的金属从它们的盐溶液中置换出来等)
【解析】
根据金属与酸反应的条件(位于氢之前的金属能置换出盐酸、稀硫酸中的氢)、金属与盐溶液反应的条件(前换后的原则),我们便能解释不能用铁制容器配制硫酸铜溶液的原因、以及验证镁比锌的金属活动性强,应选用的溶液是什么了。
(1)铁能和硫酸铜溶液反应,故不能用铁制容器配制硫酸铜溶液。反应的化学方程式为:Fe+CuSO4=Cu+FeSO4,因此,本题正确答案是:Fe+CuSO4=Cu+FeSO4;
(2)要验证镁比锌的金属活动性强,我们可以选用稀盐酸或稀硫酸,根据反应的剧烈程度判断即可。还可以选择可溶性锌盐溶液,因此,本题正确答案是:稀盐酸(或稀硫酸、氯化锌等可溶性锌盐溶液);
(3)从金属活动性顺序中还能获得的信息有:位于氢之前的金属能置换出盐酸、稀硫酸中的氢(或金属的位置越靠前,它的活动性越强,因此,本题正确答案是:(位于氢前面的金属能置换出酸中的氢(或金属的位置越靠前,它的活动性越强、位于前面的金属可以把位于后面的金属从它们的盐溶液中置换出来等)。


科目:高中化学 来源: 题型:
【题目】一定温度下,对于可逆反应A(g)+2B(g)![]() 3C(g)的下列叙述中,能说明反应已达到平衡的是
3C(g)的下列叙述中,能说明反应已达到平衡的是
A.单位时间内消耗a mol A,同时生成3a mol CB.容器内的压强不再变化
C.![]() D.C的体积分数不再变化
D.C的体积分数不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1L0.01mol·L-1一元酸HR溶液中逐渐通入氨气[常温下NH3·H2O电离平衡常数K=1.76×10-5],保持温度和溶液体积不变,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述不正确的是
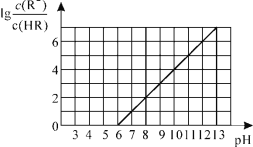
A.0.01mol·L-1HR溶液的pH约为4
B.随着氨气的通入,![]() 逐渐减小
逐渐减小
C.当溶液为碱性时,c(R-)>c(HR)
D.当通入0.01 mol NH3时,溶液中存在:c(R-)>c(NH4+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中的∣△H∣能表示可燃物的燃烧热的是( )
A.H2(g)+![]() O2(g)=H2O(1)△H=-285.8kJ/mol-1
O2(g)=H2O(1)△H=-285.8kJ/mol-1
B.H2(g)+C12(g)=2HCl(g)△H=-184.6kJ/mol-1
C.2CO(g)+O2(g)=2CO2(g)△H= 一566kJ/mol-1
D.CH4(g)+2O2(g)=2H2O(g)+CO2(g)△H= 一802.3kJ/mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠、碳酸氢钠和氯化钠的固体混合物共4 g,把它们加强热到质量不再减轻为止,冷却后称重为3.38 g。在残余固体中加入过量的盐酸,产生二氧化碳0.88 g。回答下列问题:
(1)固体质量减轻了__________g,这是因为发生了反应__________________________(写化学方程式),从化学方程式可计算出原混合物中碳酸氢钠的质量是__________g,加热后新增加了碳酸钠__________g。
(2)残余固体中加入过量盐酸的化学方程式为__________________,通过已知条件“产生的二氧化碳为0.88 g”可以计算出参加反应的碳酸钠是____________g,因为其中有____________g 碳酸钠是加热碳酸氢钠产生的,故原混合物中含碳酸钠____________g。
(3)原混合物中含氯化钠____________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于苯乙烯(![]() )有下列叙述:① 能使酸性KMnO4溶液褪色;② 能使溴的四氯化碳溶液褪色;③ 可溶于水;④ 可溶于苯中;⑤ 能与浓硝酸发生取代反应;⑥ 所有的原子可能共平面。其中正确的是( )
)有下列叙述:① 能使酸性KMnO4溶液褪色;② 能使溴的四氯化碳溶液褪色;③ 可溶于水;④ 可溶于苯中;⑤ 能与浓硝酸发生取代反应;⑥ 所有的原子可能共平面。其中正确的是( )
A. ①②③④⑤ B. ①②⑤⑥ C. ①②④⑤⑥ D. 全部正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如下图,该物质不应有的化学性质是( )
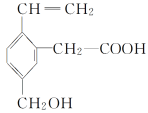
①可燃烧;②可与溴加成;③可使酸性KMnO4溶液褪色;④可与NaHCO3溶液反应;⑤可与NaOH溶液反应;⑥1mol该有机物与Na反应生成2molH2
A.①③B.②⑥C.④⑤D.⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以冶铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下:
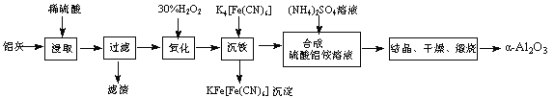
(1)铝灰中氧化铝与硫酸反应的化学方程式为 。
(2)图中“滤渣”的主要成分为 (填化学式)。
(3)加30%的H2O2溶液发生的离子反应方程式为 。
(4)煅烧硫酸铝铵晶体,发生的主要反应为:
4[NH4Al(SO4)2·12H2O]![]() 2Al2O3+ 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。
2Al2O3+ 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。
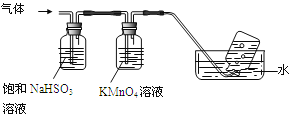
①集气瓶中收集到的气体是 (填化学式)。
②足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有 (填化学式)。
③KMnO4溶液褪色(MnO4-还原为Mn2+),发生的离子反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高聚物![]() 的重要用途之一是生产汽车刹车片,其合成路线如图所示:
的重要用途之一是生产汽车刹车片,其合成路线如图所示:

已知:![]() +
+![]()
![]()
![]()
(1)A→B的反应类型属于_____________,D的名称是_____________,烃F的分子式为____________。
(2)E中含有官能团的名称是___________,C的结构简式为____________。
(3)用文字叙述淀粉转化为A的原理:___________。
(4)写出G→H的化学方程式:__________。
(5)烃F有多种同分异构体,写出其同分异构体中含有2个相同官能团且无支链的链状物质的结构简式:_____(任写三种),其中核磁共振氢谱峰最少的一种物质有______个峰。
(6)写出以2—甲基—1,3—丁二烯和丙烯为原料合成![]() 的合成路线:______(无机试剂任选)。
的合成路线:______(无机试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com