
四种非金属主族元素M、X、Y、Z在周期表中相对位置如图,下列判断不正确的是
| X | ||
| Y | ||
| Z | M |
A.Z的氢化物中中心原子的杂化方式为sp3
B.Z原子的第一电离能小于M原子的第一电离能
C.四种元素全部位于p区
D.M、Y、Z最高价氧化物对应水化物的酸性从强到弱的顺序为:Y>M>Z
科目:高中化学 来源: 题型:
香豆素是一种天然香料,存在于黑香豆、兰花等植物中。工业上常用水杨醛与乙酸酐在催化剂存在下加热反应制得:
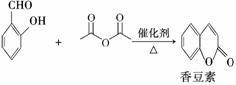
以下是由甲苯为原料生产香豆素的一种合成路线(部分反应条件及副产物已略去):
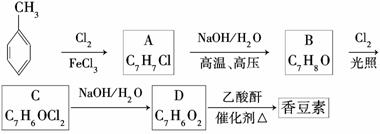
已知以下信息:
①A中有五种不同化学环境的氢;
②B可与FeCl3溶液发生显色反应;
③同一个碳原子上连有两个羟基通常不稳定,易脱水形成羰基。
请回答下列问题:
(1)香豆素的分子式为________;
(2)由甲苯生成A的反应类型为__________,A的化学名称为________;
(3)由B生成C的化学反应方程式为__________________________________
________________________________________________________________________;
(4)B的同分异构体中含有苯环的还有________种,其中在核磁共振氢谱中只出现四组峰的有________种;
(5)D的同分异构体中含有苯环的还有________种,其中:①既能发生银镜反应,又能发生水解反应的是________(写出结构简式);
②能够与饱和碳酸氢钠溶液反应放出CO2的是________(写结构简式)
查看答案和解析>>
科目:高中化学 来源: 题型:
人工合成化合物NH5 可改写成HN4H,能和水反应:NH5 + H2O==NH3.H2O + H2↑.下列说法正确的是( )
A. NH5属于离子化合物,该反应中水做氧化剂
B.该反应属于氧化还原反应,NH5既是氧化剂又是还原剂
C.该反应不属于氧化还原反应,属于复分解反应
D.标准状况下每生成22.4LH2时,转移2NA电子
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮的氢化物。
①NH3分子的空间构型是____________;N2H4分子中氮原子轨道的杂化类型是________。
②肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2N2H4(l)===3N2(g)+4H2O(g)
ΔH=-1 038.7 kJ·mol-1
若该反应中有4 mol N—H键断裂,则形成的π键有____________ mol。
③肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4晶体内不存在________(填标号)。
a.离子键 b.共价键
c.配位键 d.范德华力
(2)(2012·新课标全国节选)ⅥA族元素氧、硫、硒(Se)的化合物在研究和生产中有许多重要用途。请回答下列问题:
①H2Se的酸性比H2S________(填“强”或“弱”)。气态SeO3分子的立体构型为____________,SO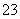 离子的立体构型为____________。
离子的立体构型为____________。
②H2SeO3的K1和K2分别为2.7×10-3和2.5×10-8,H2SeO4第一步几乎完全电离,K2为1.2×10-2,请根据结构与性质的关系解释:
H2SeO4比H2SeO3酸性强的原因:______________________________________
_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是
A.NH4Cl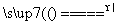 NH3↑+HCl↑
NH3↑+HCl↑
B.NH3+CO2+H2O===NH4HCO3
C.2NaOH+Cl2===NaCl+NaClO+H2O
D.2Na2O2+2CO2===2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是( )
| 选项 | 规律 | 结论 |
| A | 较强酸可以制取较弱酸 | 次氯酸溶液无法制取盐酸 |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | NH3的沸点低于PH3 |
| D | 溶解度小的沉淀易向溶解度更小的沉淀转化 | ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
根据原子结构及元素周期律的知识,下列推断正确的是( )
A.同主族元素含氧酸的酸性随核电荷数的增加而减弱
B.核外电子排布相同的微粒化学性质也相同
C.Cl-、S2-、Ca2+、K+半径逐渐减小
D.  Cl与
Cl与 Cl得电子能力相同
Cl得电子能力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22,下列说法正确的是( )
| X | Y | ||
| W | Z | ||
| T |
A.X、Y、Z三种元素最低价氢化物的沸点依次升高
B.由X、Y和氢三种元素形成的化合物中只有共价键
C.物质WY2、W3X4、WZ4均有熔点高、硬度大的特性
D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4
查看答案和解析>>
科目:高中化学 来源: 题型:
已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO4?5H2O(s) === CuSO4(s)+5H2O(l) △H=+Q2 kJ·mol-1则Q1、Q2的关系为 ( )
A.Q1<Q2 B. Q1>Q2 C. Q1=Q2 D. 无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com