
����Ŀ����ϩ����Ҫ���л�����ԭ�ϡ��Զ�ϩ����ϩΪԭ�Ϸ�Ӧ���ɱ�ϩ�ķ�������Ϊ��ϩ���绯����,��Ҫ��ӦΪ![]()
![]()
![]()
��֪���ȼ��������:
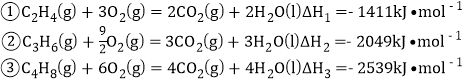
����˵������ȷ���� ( )
A. ���ĵ����ʵ�����ԭ��,��Ӧ�۵ķ���������
B. �ų���ȵ�����,��Ӧ�ٲ�����![]() ����
����
C. ��ϩ���绯����Ӧ������![]() ������
������![]()
D. ��ϩ���绯����Ӧ�жϼ����յ������ȳɼ��ų���������
���𰸡�C
��������
��ȼ���ȵĸ�����㡢��˹���ɡ���Ӧ������ܵĹ�ϵ�����жϡ�
A�ȼ�ո�1molC2H4��C3H6��C4H8����Ӧ��������࣬A����ȷ��
B���Ӧ�٢ڢ�������1molCO2ʱ���ֱ����705.5kJ��683kJ��634.8kJ����ų���ȵ�����ʱ��Ӧ��������![]() ���٣�B����ȷ��
���٣�B����ȷ��
C��ݸ�˹���ɣ���+�����ڡ�2��![]()
![]()
![]() ��H��+148kJ/mol����Ӧ������
��H��+148kJ/mol����Ӧ������![]() ������
������![]() 48kJ��C�����
48kJ��C�����
D���ϩ���绯����Ӧ�����ȷ�Ӧ�����ѷ�Ӧ���еĻ�ѧ�����յ��������γ��������еĻ�ѧ���ų��������࣬D����ȷ��
����ѡC��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����SO2�ֱ�ͨ�����и���Һ�У������й�˵����ȷ����
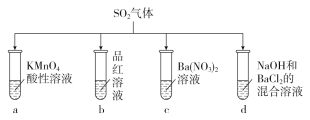
A. �Թ�a��ʵ�����֤��SO2����Ư����
B. �Թ�b����Һ��ɫ��˵��SO2����ǿ������
C. �Թ�c���ܲ�����ɫ������˵��SO2���л�ԭ��
D. �Թ�d���ܲ�����ɫ����������ϡ����������ȫ�ܽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭԪ���ڻ��������仯�ϼۿ��Գ���![]() ��
��![]() �ۡ�
�ۡ�![]() ��
��![]() �dz�����
�dz�����![]() ��ͭ�Ļ����
��ͭ�Ļ����![]() �ǽ�Ϊ������
�ǽ�Ϊ������![]() ��ͭ�Ļ����
��ͭ�Ļ����
(1)ͭԪ��λ�����ڱ���_______����
A��s B��p C��d D��ds E��f
(2)��![]() ��Һ�еμӰ�ˮ�����Եõ�����ɫ����Һ���ټ����Ҵ�����������ɫ���壬д������ɫ����Ļ�ѧʽ__________________���Ƚ�
��Һ�еμӰ�ˮ�����Եõ�����ɫ����Һ���ټ����Ҵ�����������ɫ���壬д������ɫ����Ļ�ѧʽ__________________���Ƚ�![]() ��
��![]() ��
��![]() ���ǵĴ�С��
���ǵĴ�С��![]() ___________
___________![]() �
�![]() ����
����![]() ��
��![]() ��
��
(3)![]() �������ӵĿռ乹��Ϊ_______��NO3-�еĴ�м�Ӧ��ʾΪ______
�������ӵĿռ乹��Ϊ_______��NO3-�еĴ�м�Ӧ��ʾΪ______
[��Ϣ�����������У�������ԭ�ӵ�δ�ӻ���p�������2�����ӣ�������������ԭ�ӵ�p���������1�����ӣ��粢���γ�һ����м�����ʾΪ![]() ��]
��]
![]() �ľ����ṹ��ͼ��ʾ��C1ԭ��λ��������Ķ�������ģ�Cuԭ��λ��Clԭ�ӹ��ɵ����������ġ�
�ľ����ṹ��ͼ��ʾ��C1ԭ��λ��������Ķ�������ģ�Cuԭ��λ��Clԭ�ӹ��ɵ����������ġ�
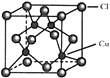
��ÿ��Clԭ����Χ��Clԭ������ҵȾ����Cuԭ����ĿΪ________________��
������ͭԭ��Ϊ���㹹�ɾ���������ԭ��Ϊ________(Cu��Cl)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��������BrFx��ˮ�����ʵ���֮��3 ��5������Ӧ�������Ϊ����(HBrO3)������ᡢ�������������
��BrFx��x=__________��
�ڸ÷�Ӧ�Ļ�ѧ����ʽΪ__________________________________________��
�۴˷�Ӧ����������______________����ԭ����______________��
��2����ƽ���з�Ӧʽ������˫���ű������ת�Ƶķ������Ŀ
____KMnO4 ��____H2O2+____H2SO4 ��____K2SO4��____MnSO4��___ O2�� �� ____H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶���,���ݻ�Ϊ1L���ܱ������г���![]() ��
��![]() ����
����![]() ���
���![]() �����ʵ�����ʱ��ı仯��ͼ��ʾ��(��֪�����¶���,�÷�Ӧ��ƽ�ⳣ��
�����ʵ�����ʱ��ı仯��ͼ��ʾ��(��֪�����¶���,�÷�Ӧ��ƽ�ⳣ��![]() )����˵����ȷ���� ( )
)����˵����ȷ���� ( )
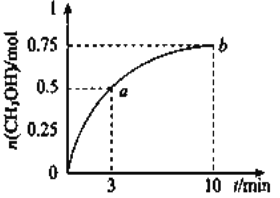
A. ![]()
B. ��b����Ӧ��״̬Ϊ��ѧƽ��״̬
C. ![]() ����������,��a���ڵ�b
����������,��a���ڵ�b
D. ������ƽ��״̬ʱ![]() ,�ɱ���������������,�����¶�
,�ɱ���������������,�����¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ijѧ���Լ��ܽ��һЩ���ɣ�������ȷ����
A.�е�����ѧ��Ӧ�����ڻ��ϡ��ֽ⡢�û������ֽ��е��κ�һ�ַ�Ӧ
B.ij�����ڹ�̬ʱ�ܵ��磬��ȷ�ϸ������ǽ�������
C.һ��Ԫ����ͬһ�����п���ʾ��ͬ��̬����һ���Ǹ�Ԫ�ص����ڼ�̬
D.������ֻ��������������������ǻ�ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2S������Դ������;��֮һ�ǻ����������õ�������Ӧԭ��Ϊ��2H2S(g) + O2(g) = S2(s) + 2H2O(l)��H=��632kJ��mol-1����ͼΪ����ĤH2Sȼ�ϵ�ص�ʾ��ͼ������˵����ȷ���ǣ� ��
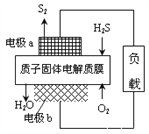
A. ����ڹ���ʱ�������ӵ缫a������������缫b
B. �缫a�Ϸ����ĵ缫��ӦΪ�� 2H2S - 4e- = S2 + 4 H+
C. ����Ӧ����64gS2ʱ������ڲ��ͷ�632kJ����
D. ����·��ͨ��4mol����ʱ����4mol H+������Ĥ���븺����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����þ���������Ļ����Һ�У�c(Mg2+ )��2 mol��L��1��c(SO42-)��6.5 mol��L��1������200 mL�˻��Һ�е�Mg2����Al3�����룬����Ӧ����1.6 mol��L��1����������Һ�������
A��0.5 L B��1.625 LC��1.8 LD��2 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ���ǣ� ��
A. ��״���£�22.4LCl2ͨ��������NaOH��Һ��ַ�Ӧ����NA������ת��
B. 100 mL 1 mol��L1FeCl3��Һ������Fe3+����ĿΪ0.1NA
C. lmolSO2������O2��һ�������·�Ӧ����SO3����ת��2NA������
D. 84gNaHCO3���庬��CO32-���ӵ���ĿΪNA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com