
【题目】如图是中学化学中常用于混合物的分离和提纯的装置。
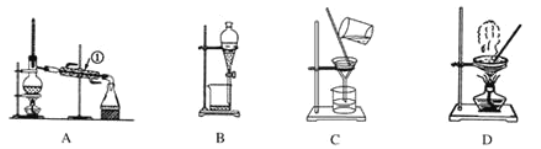
利用以上装置,可以按以下实验方案从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。(已知甲苯和甲醇均为有机溶剂,有机物大多能互溶)
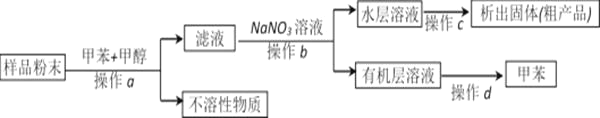
(1)装置A中仪器①的冷却水下进上出的目的是________________________________,使用装置A的操作是__________(填“a”、“b”、“c”或“d”,下同)。
(2)使用装置B的操作是_______(填“a”、“b”、“c”或“d”),使用分液漏斗前应该先_________。
(3)装置C的玻璃棒作用是___________,若所得沉淀不溶于水且需要洗涤,则洗涤的具体操作是________________________________________________________________________________。
(4)使用装置D的操作是_________(填“a”、“b”、“c”或“d”),该操作中玻璃棒的作用是_____________________________________________________________。
【答案】使水充满管道(夹套、通道)加强接触面积,进行充分的热量交换 d b 检查是否漏水 引流 往漏斗中加水至没过沉淀,让水自然流干,重复加水2-3次 c 搅拌,使受热均匀,避免受热不均而引起飞溅
【解析】
操作a是分离固液混合物,其操作为过滤,操作b分离互不相溶的液体混合物,需进行分液,要用到分液漏斗;操作c是从溶液中得到固体,操作为蒸发,需要蒸发皿;操作d是从有机化合物中,利用沸点不同采取蒸馏得到甲苯,以此来解答。
(1)装置A中仪器①是冷凝管,冷却水下进上出的目的是为了使水充满管道(夹套、通道)加强接触面积,进行充分的热量交换,使用装置A的操作蒸馏是d;
(2)装置B是分液,根据以上分析可知使用装置B的操作是b,使用分液漏斗前应该先检查是否漏水;
(3)装置C的玻璃棒作用是引流,若所得沉淀不溶于水且需要洗涤,则洗涤的具体操作是往漏斗中加水至没过沉淀,让水自然流干,重复加水2-3次;
(4)装置D是蒸发,使用装置D的操作是c,该操作中玻璃棒的作用是搅拌,使受热均匀,避免受热不均而引起飞溅。


科目:高中化学 来源: 题型:
【题目】密闭容器中进行的可逆反应:aA(g)+bB(g)![]() cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是
cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是

A.T1<T2,p1<p2,a+b>c,正反应为吸热反应
B.T1>T2,p1<p2,a+b<c,正反应为吸热反应
C.T1<T2,p1>p2,a+b<c,正反应为吸热反应
D.T1>T2,p1>p2,a+b>c,正反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】列各组物质中,分子数相同的是( )
A.9g H2O 和 0.5NA 个 CO2
B.2L CO 和 2L CO2
C.标准状况下 ,1mol O2 和 22.4LCCl4
D.2g H2和标准状况下 2.24L HCl 气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列事实能说明醋酸是弱电解质的组合是__________(填序号)。
①醋酸与水能以任意比互溶 ②用醋酸溶液做导电实验,灯泡很暗
③醋酸溶液中存在醋酸分子 ④0.1 mol/L醋酸溶液的pH为4
⑤醋酸能和碳酸钙反应放出CO2
(2)已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)的值增大,可以采取的措施是____________(填序号)
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)的值增大,可以采取的措施是____________(填序号)
①加少量烧碱溶液 ②升高温度 ③加少量冰醋酸 ④加水
(3)在一定温度下,有a.盐酸 b.硫酸 c.醋酸 三种酸:
①当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是________。(用序号表示,下同)
②同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是________。
③当三者c(H+)相同且体积也相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为________,反应所需时间的长短关系是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H=﹣1269kJ/mol
②
下列说法正确的是
A. 断开1 mol O﹣O键比断开1 mol N﹣N键所需能量少448kJ
B. 断开1 mol H﹣O键比断开1 mol H﹣N键所需能量相差约72.6kJ
C. 由以上键能的信息可知H2O的沸点比NH3高
D. 由元素非金属性的强弱可知 H一O键比H一N键弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠及其化合物有非常重要的用途。
(1)钠的化学性质非常活泼。画出钠的原子结构示意图________。
钠与水反应的实验过程如图①、②、③所示。
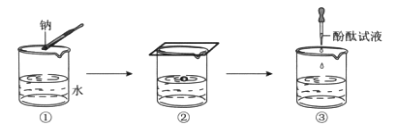
①将图②中的现象与解释用直线连接起来。_________
实验现象 解释
钠熔成小球 产生了气体
钠四处游动,嘶嘶作响 钠的密度比水小
钠浮在水面上 钠与水反应放热且钠的熔点低
②在③中酚酞变红,说明溶液呈_______(填“酸”或“碱”或“中”)性。
③钠与水反应的化学方程式是_________。
(2)过氧化钠可在潜水艇中作为氧气的来源。写出过氧化钠与水反应的化学方程式___,与二氧化碳反应的化学方程式___。
(3)为探究Na2CO3和NaHCO3的热稳定性,某同学设计了如下实验:
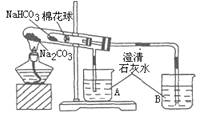
加热一段时间后,________(填“A”或“B”)中澄清石灰水变浑浊,写出澄清石灰水变浑浊的离子方程式:________。写出试管中发生反应的化学方程式________。
(4)我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)。含有氮元素、钾元素、磷元素的某些盐可以作为化肥。
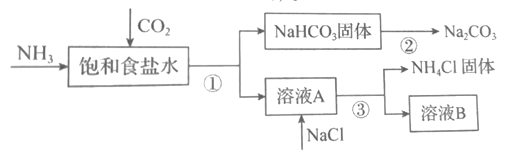
①联合制碱法所制得的“碱”是指_______(填化学式)。
②在①-③所涉及的操作方法中,包含过滤的是_______(填序号)。
③根据图,将化学方程式补充完整:NH3+CO2+___+___=NaHCO3↓+NH4Cl
④NaHCO3溶于水电离的方程式___。
⑤下列说法中,正确的是___(填字母)
a.CO2可循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH4+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷、硫、氯、砷等是农药中的重要组成元素。回答下列问题:
(1)基态砷原子的核外价电子排布式为___________。
(2)生产农药的原料PSCl3中P、S、Cl的第一电离能由大到小的顺序为________,电负性由大到小的顺序为________________________。
(3)H2O 与H2S为同族元素的氢化物,H2O可以形成H3O+或H9O4+等,而H2S几乎不能形成类似的H3S+或H9S4+,其原因是______________________。
(4)COS(羰基硫)可用作粮食的熏蒸剂,其中碳原子的杂化轨道类型为_____________,所含共价键的类型为_____________,N2O与CO2互为等电子体,且N2O分子中O只与一个N相连,则N2O的电子式为_____________________。
(5)AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的熔点为2000℃ ,其晶胞结构如图所示。
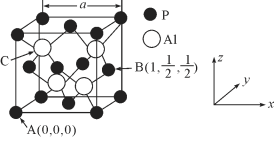
①磷化铝的晶体类型为_____________。
②A、B点的原子坐标如图所示,则C点的原子坐标为_____________。
③磷化铝的晶胞参数a=546.35pm,其密度为_____________(列出计算式即可,用NA表示阿伏加德罗常数的数值)g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用如图装置探究温度对一氧化碳还原氧化铁的影响。
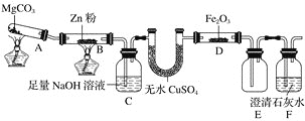
(1)MgCO3的分解产物为____________。
(2)装置C的作用是______________,处理尾气的方法为______________________。
(3)将研究小组分为两组,按如图装置进行对比实验,甲组用酒精灯、乙组用酒类喷灯对装置D加热,反应产物均为黑色粉末(纯净物)。两组分别用产物进行以下实验。已知Fe2+与K3[Fe(CN)6](铁氰化钾)溶液反应生成带有特征蓝色的铁氰化亚铁沉淀。
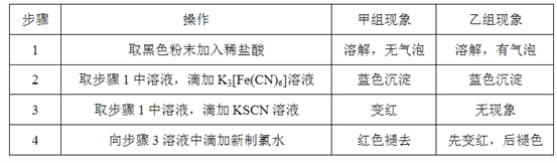
①乙组得到的黑色粉末是______________。
②甲组步骤1中反应的离子方程式为______________。
③乙组步骤4中,溶液变红的原因为______________________;溶液褪色可能的原因及其验证方法为________________________。
④从实验安全考虑,题图装置还可采取的改进措施是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1999年比利时发生奶粉受二噁英污染事件。二噁英是一类芳香族化合物的多氯代衍生物的总称,结构稳定,难以被自然分解,是公认的最危险的致癌物质之一,2,3,7,8-四氯二苯并二噁英是其中的一种,结构如图,下列说法中不正确的是 ( )
![]()
A. 它的分子式为C12H4O2Cl4B. 它不能发生加成反应
C. 它的一溴取代物有一种D. 此分子中共平面的原子最多有22个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com