
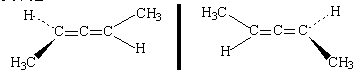
| A、互为同素形体 |
| B、同一物质 |
| C、手性异构体 |
| D、互为同系物 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
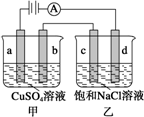
| A、甲中a的电极反应式为4OH--4e-=O2↑+2H2O |
| B、电解时向乙中滴入酚酞溶液,c电极附近首先变红 |
| C、电解后向乙中加入适量盐酸,溶液组成可以恢复原状 |
| D、当b极有64 g Cu析出时,c电极产生2 g气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中OH-向正极移动,K+、H+向负极移动 |
| B、锌发生还原反应,氧化银发生氧化反应 |
| C、锌是负极,氧化银是正极 |
| D、在电池放电过程中,负极区溶液碱性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 空气 |
| △ |
| HNO3(稀) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、b=2a | B、a=2b |
| C、b>2a | D、b<2a |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,1.7g NH3含有NA个电子 |
| B、标准状况下,22.4L水中含H2O分子NA个 |
| C、1molNa完全反应生成NaCl时,失去NA个电子 |
| D、常温常压下,22.4LCO2中含有的CO2分子数小于NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H2S+SO2→3S↓+2H2O |
| B、SO2+2Mg→2MgO+S |
| C、Cl2+SO2+2H2O→H2SO4+2HCl |
| D、SO2+2NaOH→Na2SO3+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com