
【题目】短周期元素W、X、Y、Z的原子序数依次增大,其简单离子都能破坏水的电离平衡的是
A. W2-、X+ B. X+、Y3+
C. Y3+、Z2- D. X+、Z2-
科目:高中化学 来源: 题型:
【题目】“类推”这种思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否,下列几种类推结论中错误的是( )
①钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2
②铁露置在空气中一段时间后就会生锈,性质更活泼的铝不能稳定存在于空气中
③Al(OH)3、Cu(OH)2受热易分解,Fe(OH)3受热也易分解
④不能用电解熔融 的AlCl3来制取金属铝;也不能用电解熔融的MgCl2来制取金属镁
A.①④ B.②④
C.①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将9g由CO和H2组成的混合气体在足量的O2中充分燃烧后,将生成的所有产物通过足量的Na2O2固体,Na2O2固体增加的质量为( )
A.8g B.9g C.12g D.13.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合氯化铝晶体是介于 AlCl3和 Al(OH)3之间的一种水溶性无机高分子聚合物, 是一种高效无机水处理剂, 其制备原料主要是铝加工行业的废渣--铝灰,它主要含 Al2O3、 Al,还有一些不溶于酸的杂质.聚合氯化铝生产工艺流程如下:

(1)反应中副产品E是_________(用化学式表示);
(2)生产过程中可循环使用的物质是_________(用化学式表示);
(3)为使得到的晶体较纯净,生产过程中使pH升高的c 物质可选用_________(填编号);
a. NaOH b. Al c.氨水 d. A12O3 e. NaAlO2
(4)聚合氯化铝晶体的化学式可表示为: [A12(OH)nCl6-n·xH2O]m,实验室为测定化学式中n的值,进行如下实验:
①称取 ag晶体,制成粉末,加热至质量不再变化时,得到bg氧化铝固体.此过程可能用到的下列仪器有___________;(填编号)
a.蒸发皿 b.坩埚 c.研钵 d.试管
②另取ag晶体,进行如下操作:用A 酸溶解→加足量AgNO3溶液→操作c →烘干→称量为c g 固体.试剂A为_______,操作C为_________(填操作名称).n=_________(用含a、b、c的代数式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜板上铁铆钉处的腐蚀原理如图所示,下列有关说法中,不正确的是
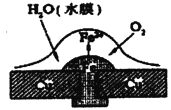
A.正极电极反应式为:2H++2e-=H2↑
B.此过程中还涉及到反应:4Fe(OH)2+O2+2H2O=4Fe(OH)3
C.此过程中铜并不被腐蚀
D.此过程中电子从Fe移向Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁和铝的混合物投入100mL盐酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaoH溶液的体积关系如下图所示。 若不考虑金属和盐酸反应时HCI的挥发,则下列说法不正确的是( )
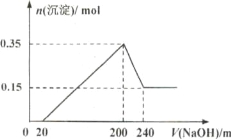
A.镁和铝的总质量为9 g
B.盐酸的物质的量浓度为10 mol/L
C.NaOH溶液的物质的量浓度为5 mol/L
D .生成的氢气在标准状况下的体积为11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列10种物质:
①H2 ②铝 ③CaO ④CO2 ⑤浓硫酸 ⑥石英 ⑦Cu ⑧氨水 ⑨HNO3 ⑩明矾
(1)上述物质属于氧化物的是 ;属于电解质的是 (填物质编号)。
(2)上述物质中有一种物质在饮用水处理中常做净水剂,则该物质在水中的电离方程式为 。
(3)上述物质中有一种物质遇酚酞试剂会变红色,受热后红色变浅或褪去,则该物质是 (填物质名称)
(4)物质⑤与⑦发生反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸雨的pH______(>,<,=)5.6,写出形成硫酸型酸雨的相关的化学方程式:二氧化硫与雨水_______________________,再被氧化成硫酸___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,等体积的两容器内分别充满14N16O和13C16O气体,下列对两容器中气体的判断正确的是( )
A. 中子数相同 B. 分子数不同
C. 质子数相同 D. 气体质量相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com