
【题目】下列食物中,富含蛋白质的是( )
A.馒头B.蔬菜C.鱼肉D.肥膘肉
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】如图表示在不同条件下酶促反应速率的变化曲线,请分析回答下列问题
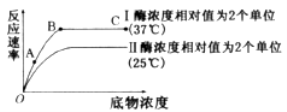
(1)酶促反应速率可以用单位时间单位体积的 来表示。
(2)Ⅱ和Ⅰ相比,酶促反应速率慢,这是因为 。
(3)图中AB段和BC段影响反应速率的主要限制因子分别是 和 。
(4)为了探究pH对酶活性的影响,有人做了如下实验:
试管编号 | 加入物 | 现象 |
1 | 2ml猪肝研磨液 + 1ml蒸馏水 + 2ml 3%的过氧化氢 | 放出大量的气泡 |
2 | 2ml猪肝研磨液 + 1ml NaOH + 2ml 3%的过氧化氢 | 无气泡 |
3 | 2ml猪肝研磨液 + 1ml HCl + 2ml 3%的过氧化氢 | 无气泡 |
实验中的底物是 ,自变量是 ,因变量是 ,无关变量是 (至少写出一个)。
(5)有同学准备以H2O2为材料来研究温度对H2O2酶活性的影响?你认为是否妥当? ;原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 自然界中硅以游离态和化合态两种形式存在
B. 二氧化硅有结晶形和无定形两种存在形态
C. 石英、水晶、玛瑙都是结晶形的
D. 无定形的二氧化硅主要存在于硅藻土中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室配制500mL 0.2mol/L的FeSO4溶液,实验操作步骤有:
①在天平上称出27.8g绿矾(FeSO47H2O),把它放在烧杯里,用适量的蒸馏水使它完全溶解
②把制得的溶液小心地注入500mL容量瓶中
③继续向容量瓶中加蒸馏水至液面距刻度1~2cm处.改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀
⑤将容量瓶塞塞紧,充分摇匀
请填写下列空白:
(1)操作步骤的正确顺序为(填序号) .
(2)本实验用到的基本仪器已有烧杯、天平(带砝码、镊子)、玻璃棒,还缺少的仪器是、 .
(3)某同学观察液面的情况如图所示,对所配溶液浓度有何影响?会(填“偏高”、“偏低”或“无影响”). 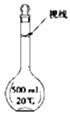
(4)若出现如下情况,所配溶液浓度将偏高还是偏低:没有进行操作步骤④,会;加蒸馏水时不慎超过了刻度,会 . 向容量瓶中转移溶液时(实验步骤②)不慎有液滴掉在容量瓶外面,会 .
(5)若实验过程中出现如下情况应如何处理?加蒸馏水时不慎超过了刻度,应 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中是生物体内几种有机物组成以及它们各自功能的关系图,m1、m2、m3、m4分别是大分子物质M1、M2、M3、M4的组成单位。下列说法正确的是( )

A. 相同质量的M1和M2被彻底氧化分解,则M1的耗氧量多
B. 同一个体不同细胞中M3的种类不同取决于基因的选择性表达
C. m3和m4之间的区别主要是五碳糖和碱基的种类不同
D. 不同的M4在结构上的区别主要是m4的连接方式不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在C(s)+CO2(g) = 2CO(g)的反应中,现采取下列措施:①缩小体积,增大压强②增加碳的量③通入CO2④恒容下充入N2⑤恒压下充入N2。其中能够使反应速率增大的措施是( )
A. ①④ B. ②③⑤ C. ①③ D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
C. 第二阶段,Ni(CO)4分解率较低
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是人体不可缺少的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去.某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:在溶液中KIO3+5KI+3H2SO4═3I2+3H2O+3K2SO4
(1)改写成离子反应方程式后,并用双线桥表示该反应中电子转移的方向和数目:该反应中氧化产物与还原产物的质量比是 , 21.4gKIO3参加反应时转移电子mol
(2)实验结束后分离I2和K2SO4溶液所用的试剂是
A.Na2SO4溶液 B.酒精 C. CCl4 D.食盐水
所用的分离方法是 , 所用的玻璃仪器有 , 出现什么现象可以确定该食盐中含碘 .
(3)上面实验中用到一定物质的量浓度的稀硫酸,若配制0.5mol/L的稀硫酸溶液450mL,需用98%的浓硫酸(其密度为1.84g/cm3)mL,配制中需要用到的主要玻璃仪器是(填序号) .
A.100mL量筒 B.托盘天平 C.玻璃棒 D.100mL容量瓶
E.50mL 量筒 F.胶头滴管 G.烧杯 H.500mL容量瓶
(4)下面操作造成所配稀硫酸溶液浓度偏高的是
A.溶解的时候溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可降解塑料PCL的结构可表示为 ![]() .其合成路线如下.
.其合成路线如下. 
已知:
① ![]()
②R﹣CH=CH﹣CH3 ![]() R﹣CH=CH﹣CH2Br
R﹣CH=CH﹣CH2Br
③ ![]()
回答下列问题:
(1)由苯酚生成B的反应试剂和条件为
(2)D的结构简式是 . 上述生成D的反应类型是 .
(3)PCL属于(填“线型”或“体型”)高分子材料. 与D具有相同官能团的同分异构体E经下列合成路线可转化为D.![]()
(4)E的结构简式是 .
(5)由H生成K的化学方程式是 .
(6)M的氧化产物己二酸是合成尼龙的原料之一,用B做原料三步反应可制得己二酸. B﹣W→X→己二酸
写出W、X的结构简式:W、X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com