
【题目】工业上常将铬镀在其他金属表面,同铁、镍组成各种性质的不锈钢,在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电板上无气体产生,铬电极上产生大量有色气体,则下列叙述正确的是
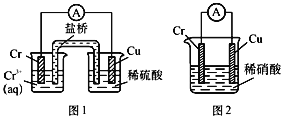
A. 图1为原电池装置,盐桥中的阴离子移向Cu电极的烧杯中
B. 由实验现象可知:金属活动性Cu>Cr
C. 图2装置中Cu电极上发生的电极反应式为:Cu-2e-=Cu2+
D. 两个装置中,电子均由Cr电极流向Cu电极
 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
【题目】下图所示为镍锌可充电电池放电时电极发生物质转化的示意图,电池使用KOH和K2Zn(OH)4为电解质溶液,下列关于该电池说法正确的是
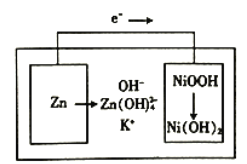
A. 放电时溶液中的K+移向负极 B. 充电时阴极附迁的pH会降低
C. 理论上负极质量每减少6.5g,溶液质量增加6.3g D. 放电时正极反应为H++NiOOH+e-=Ni(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学探究KI的化学性质。
(1)KI组成中含有钾元素,可知它能发生__________反应。
(2)①根据碘元素的化合价可推知KI有__________性。
②与KI反应,能体现上述性质的试剂有_________(填序号)
a、Fe2+ b、Fe3+ c、Br- d、Cl2
(3)兴趣小组的同学们猜测:Cu2+有可能氧化I-,为了验证,他们做了如下实验。(已知:CuI为不溶于水的白色沉淀)
操作 | 现象 |
| 溶液分层,上层显紫色,有白色沉淀生成 |
结论:Cu2+_________(填能或不能)氧化I-。若能氧化,写出反应的离子方程式_____________________ (若认为不能氧化,此空不用填写)。
(4)①同学们依据(3)的结论推测:Ag+能氧化I-,原因为___________。
他们做了如下实验进行探究
实验一:
操作 | 现象 |
| 生成黄色沉淀 |
②发生反应的化学方程式为_________________________________。
实验二:
操作 | 现象 |
| 3分钟后KI溶液开始变黄,随后溶液黄色加深,取出该烧杯中溶液滴入盛有淀粉溶液的试管,溶液变蓝。 |
③甲同学认为根据上述实验现象不能说明Ag+能氧化I-,原因是_______________________________。
乙同学在上述实验基础上进行了改进,并得出结论:Ag+能氧化I-。发生反应的离子方程式为____________________________________。
由以上两个实验得出的结论为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是( )
A.在常温、常压下,11.2 L N2含有的分子数为0.5 NA
B.标准状况下,22.4 L H2和O2的混合物所含分子数为NA
C.标准状况下,18 g H2O的体积是22.4 L
D.1 mol SO2的体积是22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下CH3COOH的电离常数K=1.6×10-5,1g4=0.6。该温度下,向20mL0.01 mol·L-1CH3COOH溶液中逐滴加入0.01 mol·L-1KOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法正确的是
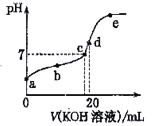
A. 滴定过程中宜选用甲基橙作指示剂
B. a点溶液中c(H+)为1×10-4 mol·L-1
C. a、b、c、d、e四点中水的电离程度最大的是e点
D. d 点时溶质的水解常数为6.25×10-10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、根据分子中所含官能团可预测有机化合物的性质。
(1)下列化合物中,常温下易被空气氧化的是_______________(填字母)。
a.苯 b.甲苯 c.苯甲酸 d.苯酚
(2)下列化合物中能发生消去反应的是_______________(填字母)。
a.苯甲醇 b. (CH3)3CCl c. (CH3)2CHOH d. 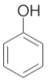
(3)苯乙烯是一种重要为有机化工原料。
①苯乙烯的分子式为___________________。
②苯乙烯在一定条件下能和氢气完全加成,加成产物的一溴取代物有__________种。
Ⅱ、按要求写出下列反应的化学方程式:
(1)(CH3)2C(OH)CH(OH)CH2OH发生催化氧化反应:_________________________________。
(2)1,2-二溴丙烷发生消去反应:_________________________________。
(3)![]() 发生银镜反应:_________________________________。
发生银镜反应:_________________________________。
Ⅲ. 水杨酸的结构简式为:![]() ,用它合成的阿司匹林的结构简式为:
,用它合成的阿司匹林的结构简式为: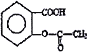
(1)将水杨酸与_________溶液作用,可以生成![]() , 请写出将
, 请写出将![]() 转化为
转化为![]() 的化学方程式___________________________________。
的化学方程式___________________________________。
(2)阿司匹林与足量NaOH溶液发生反应的化学方程式是______________________________。
(3)写出同时符合下列条件的水杨酸的同分异构体:_____________。
①能发生银镜反应 ②能与氯化铁溶液显色 ③核磁共振氢谱1∶2∶2∶1 ④能够水解
(4)与阿司匹林互为同分异构体的芳香二元羧酸共有___________种(不含立体异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原
B.含有最低价元素的化合物不一定具有很强的还原性
C.阳离子只能得电子被还原,阴离子只能失电子被氧化
D.在化学反应中,得电子越多的氧化剂,其氧化性就越强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.Na2O2能与水反应,所以Na2O2可以作气体的干燥剂
B.钠可以从AgNO3溶液中置换出金属银
C.钠能与水反应,所以钠着火不能用水灭火,要用泡沫灭火器
D.Na2O、Na2O2、NaOH和NaHCO3均是强电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com