
����Ŀ��ij��ѧ��ȤС���ͬѧ̽��KI�Ļ�ѧ���ʡ�
��1��KI����к��м�Ԫ������֪���ܷ���__________��Ӧ��
��2���ٸ��ݵ�Ԫ�صĻ��ϼۿ���֪KI��__________�ԡ�
����KI��Ӧ���������������ʵ��Լ���_________������ţ�
a��Fe2+ b��Fe3+ c��Br- d��Cl2
��3����ȤС���ͬѧ�Dz²⣺Cu2+�п�������I-��Ϊ����֤��������������ʵ�顣����֪��CuIΪ������ˮ�İ�ɫ������
���� | ���� |
| ��Һ�ֲ㣬�ϲ�����ɫ���а�ɫ�������� |
���ۣ�Cu2+_________(���ܻ���)����I-������������д����Ӧ�����ӷ���ʽ_____________________ ������Ϊ�����������˿ղ�����д����
��4����ͬѧ��������3���Ľ����Ʋ⣺Ag+������I-��ԭ��Ϊ___________��
������������ʵ�����̽��
ʵ��һ��
���� | ���� |
| ���ɻ�ɫ���� |
��������Ӧ�Ļ�ѧ����ʽΪ_________________________________��
ʵ�����
���� | ���� |
| 3���Ӻ�KI��Һ��ʼ��ƣ������Һ��ɫ���ȡ�����ձ�����Һ����ʢ�е�����Һ���Թܣ���Һ������ |
�ۼ�ͬѧ��Ϊ��������ʵ��������˵��Ag+������I-��ԭ����_______________________________��
��ͬѧ������ʵ������Ͻ����˸Ľ������ó����ۣ�Ag+������I-��������Ӧ�����ӷ���ʽΪ____________________________________��
����������ʵ��ó��Ľ���Ϊ________________________________��
���𰸡� ��ɫ ��ԭ�� b��d )�� 2Cu2++4I-=2CuI��+I2 Ag+�������Դ���Cu2+ AgNO3+KI=AgI��+KNO3 �п����ǿ�����O2������KI��Һ������������ 2Ag++2I-=2Ag+I2 Ag+��I-�ܷ���������Ӧ�����ܷ���������ԭ��Ӧ������������Һ�нӴ�ʱ�� ������Ӧ���ȷ�����
����������1����Ϊ���Ƿdz����õĽ����������Ԫ�صķ���������ɫ��Ӧ���𰸣���ɫ��
��2����KI�еĵ�Ԫ��Ϊ��ͼ�̬-1�ۣ����Կ���֪KI�л�ԭ�ԡ��𰸣���ԭ����
����ΪFe3+ ��Cl2���к�ǿ�������ԣ���������KI������������KI�Ļ�ԭ�ԡ��ʴ𰸣�b d��
��3����������Һ�ֲ㣬�ϲ�����ɫ���а�ɫ��������˵��������I2��CuI��˵��Cu2+������I-����Ӧ�����ӷ���ʽ2Cu2++4I-=2CuI��+I2 ����ΪCu2+������I-��Ag+�����Դ���Cu2+������Ag+Ҳ���Ի�I-��
��������Ӧ�Ļ�ѧ����ʽΪAgNO3+KI=AgI��+KNO3��
��KI��Һ��ʼ��ƣ������Һ��ɫ���������Ag++I-= AgI![]() ��ȡ�����ձ�����Һ����ʢ�е�����Һ���Թܣ���Һ������˵�� KI��������I2�����ˣ� �������Ag+�����ã��Ϳ����ǿ�����O2������KI��Һ������������ ��
��ȡ�����ձ�����Һ����ʢ�е�����Һ���Թܣ���Һ������˵�� KI��������I2�����ˣ� �������Ag+�����ã��Ϳ����ǿ�����O2������KI��Һ������������ ��
Ag+������I-�����ӷ���ʽΪ2Ag++2I-=2Ag+I2��
����������Ag+��I-�ܷ���������Ӧ�����ܷ���������ԭ��Ӧ������������Һ�нӴ�ʱ�� ������Ӧ���ȷ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����ijNa2CO3��Һ�м���ϡ���ᣬ��Һ�к�̼�������ʵ����������գ�����ҺpH�仯�IJ��������ͼ��ʾ������˵������ȷ����
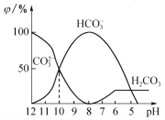
A. Na2CO3��Һ��c(Na+)=c(CO32-��+ c(HCO3-��+ c(H2CO3��
B. pH=8ʱ����Һ��c(Cl-)=c(Na+)
C. pH =7ʱ����Һ�е�c(Na+)>c(Cl-)>c(HCO3-)>c(H+)=c(OH-)
D. 25��ʱ��CO32-+H2O![]() HCO3-+OH-��Kh=10��10mol��L��1
HCO3-+OH-��Kh=10��10mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҵ��ķе���78�棬����ˮ������Ȼ��ܡ����ѵķе�Ϊ34.6�棬������ˮ���ڱ���Na2CO3 ��Һ�м������ܣ����Ѽ���ȼ�ա�ʵ�������ѵķ�Ӧԭ���ǣ�
2CH3CH2OH��H2O + CH3CH2��O��CH2CH3 (����)
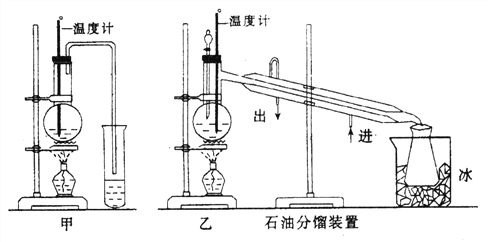
��1����ͼ����ͼ������ʵ���������ѵ�װ�ã�ѡװ��_________(��ס����ҡ�)�������������______________________________��
��2����ӦҺ��Ӧ�����ʯ����������____________________��
��3����Ӧ���¶ȼƵ���ȷλ����ˮ��������____________________��
��4����װ�����Ƶõ������п��ܺ��д��������ʣ���������__________����ȥ�������ʵļ�������__________________����ʾ�����Ѳ�����ˮ���Ҵ���ˮ���ܣ���
��5������¶�̫�ߣ����ᷢ������Ӧ�����������Ϊ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������У��ֱ��������ƣ��ֺ�NaOH��Һ��Ӧ����
A. ��ˮ�ƾ� B. ���� C. �� D. 75%�ľƾ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɼ����ɺϳɶ����л���

��֪��
![]()
��1��A�Ľṹ��ʽΪ________________
��2��D�����Ĺ���������Ϊ_______ ��B��C�ķ�Ӧ����_____________
��3����֪1molE��һ�������º�1mol H2��Ӧ�ɳ�F��д��E��F�Ļ�ѧ����ʽ_____________________________________
��4��E��˳ʽ�ṹ��ʽΪ_____________________
��5������I��˵����ȷ����______________________
A.������ˮ�����ӳɷ�Ӧ B.�ܷ���������Ӧ
C.�˴Ź���������3�����շ� D.����NaHCO3��Һ��Ӧ
��6��д��C��M��Ӧ�Ļ�ѧ����ʽ_______________________________
��7����CH3CHOΪ�л�ԭ�ϣ�ѡ�ñ�Ҫ�����Լ��ϳ�CH3CHOHCHOHCH2OH,д���ϳ�·�ߣ��ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ������____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϵͳ��������д�����л�������Ƽ��й����ݣ�
��1��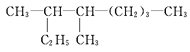 ��������________________
��������________________
��2��2��6-����-4-�һ�����Ľṹ��ʽ��________________________��1 mol������ȫȼ����Ҫ��������________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����![]() Ϊԭ����ȡ
Ϊԭ����ȡ![]() ���ǻ�����������ͪ�Ļ���ԭ�����������кϳ�·����գ�
���ǻ�����������ͪ�Ļ���ԭ�����������кϳ�·����գ�
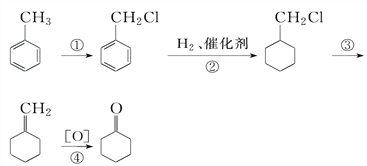
��1����Ӧ�ٵ�������___________________________________________________����Ӧ�۵�������_____________________________________________________��
��2��д����Ӧ�ڢۢܵĻ�ѧ����ʽ��ע����Ӧ���ͣ�
��________________________________________________________��
��____________________________________________________________��
��_________________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ��������������������棬ͬ��������ɸ������ʵIJ���֣�����ͼװ���У��۲쵽ͼ1װ��ͭ�缫�ϲ�����������ɫ���ݣ���ͼ2װ����ͭ�������������������缫�ϲ���������ɫ���壬������������ȷ����
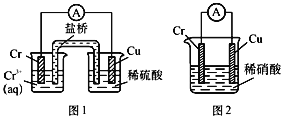
A. ͼ1Ϊԭ���װ�ã������е�����������Cu�缫���ձ���
B. ��ʵ�������֪���������Cu>Cr
C. ͼ2װ����Cu�缫�Ϸ����ĵ缫��ӦʽΪ��Cu-2e-=Cu2+
D. ����װ���У����Ӿ���Cr�缫����Cu�缫
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�Ƿ�������ʱ���õ��������ش���������:
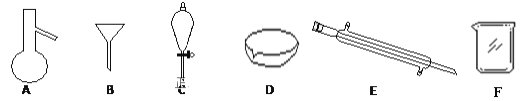
��1�������A��E������________��________��
��2������Cװ���м����ˮ������CCl4�����ã���۲쵽ʲô����________��
��3����������Һ�к���������CaCl2��MgCl2��MgSO4��Ϊ������Щ���ʵõ�������ʳ�Σ������μ���Ļ�ѧ�Լ���________��д��ѧʽ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com