
【题目】25℃时,向某Na2CO3溶液中加入稀盐酸,溶液中含碳微粒的物质的量分数(φ)随溶液pH变化的部分情况如图所示。下列说法中正确的是
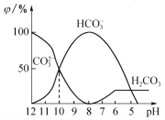
A. Na2CO3溶液中c(Na+)=c(CO32-)+ c(HCO3-)+ c(H2CO3)
B. pH=8时,溶液中c(Cl-)=c(Na+)
C. pH =7时,溶液中的c(Na+)>c(Cl-)>c(HCO3-)>c(H+)=c(OH-)
D. 25℃时,CO32-+H2O![]() HCO3-+OH-的Kh=10-10mol·L-1
HCO3-+OH-的Kh=10-10mol·L-1
【答案】C
【解析】A.根据物料守恒可知,Na2CO3溶液中c(Na+)=2c(CO32-)+ 2c(HCO3-)+ 2c(H2CO3),A错误; B. pH=8时,由图像可知Na2CO3与盐酸完全反应生成碳酸氢钠和氯化钠,溶液中: c(Cl-)<c(Na+),B错误;C. pH =7时,溶液中存在电荷守恒:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)+ c(Cl-),且c(H+)=c(OH-),所以离子浓度大小关系为:c(Na+)>c(Cl-)>c(HCO3-)>c(H+)=c(OH-),C正确;D. pH=10时,c(CO32-)=c(HCO3-),CO32-+H2O![]() HCO3-+OH-的Kh=
HCO3-+OH-的Kh=![]() = c(OH-)=
= c(OH-)=![]() mol·L-1,D错误;答案选C.
mol·L-1,D错误;答案选C.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
【题目】常温下,用0.01mol/LNaOH溶液滴定20.00mL0.01mol/LCH 3COOH溶液,所得滴定曲线如右图。下列说法正确的是
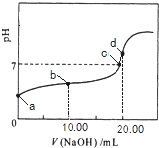
A. b点对应的溶液中: c(OH—)+c(CH3COO—) = c(Na+)+c(H+)
B. a点对应溶液的pH= 2
C. C点表示NaOH溶液与CH3COOH溶液恰好完全反应
D. d点对应的溶液中,水的电离程度小于同温下纯水的电离程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将11.65gBaSO4粉末置于盛有250mL蒸馏水的烧杯中,然后向烧杯中加入Na2CO3固体(忽视溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是
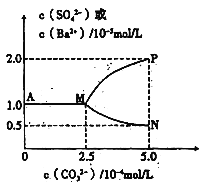
A. 相同温度时,Ksp(BaSO4)>Ksp(BaCO3)
B. BaSO4在水中的溶解度、Ksp均比在BaCl2溶液中的大
C. 若使0.05molBaSO4全部转化为BaCO3,至少要加入1.25molNa2CO3
D. 0.05molBaSO4恰好全部转化为BaCO3时,溶液中离子浓度大小为:c(CO32-)>c(SO42-)>c(Ba2+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有 X、Y、Z 三种元素,X 是有机化合物中必含的元素, Y 是地壳里含量最多的元素,Z 是质 量最轻的元素。X、Y、Z 三种元素组成的有机物 M 能被酸性高锰酸钾氧化生成 N。为了测定有机物 M 的结构,做如下实验:
①将 4.6 g 有机物 M 完全燃烧,测得生成 0.2mol CO2 和 5.4 g 水; ②用质谱仪检测有机物 M,得到如图 1 所示的质谱图; ③用核磁共振仪处理有机物 M,得到如图 2 所示图谱。

试回答下列问题:
(1)M 的结构简式是___________________,N 中含有的官能团的结构简式为_____________。
(2)写出 M 在铜作催化剂且加热条件下与氧气发生反应的化学方程式___________________。
(3)写出 M 与 N 在浓 H2SO4加热条件下发生反应的化学方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯催化氧化成乙醛可设计成如图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应式为2CH2===CH2+O2===2CH3CHO。下列有关说法正确的是
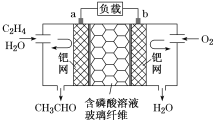
A. 每有0.1 mol O2反应,则迁移H+0.4 mol
B. 负极反应式为CH2===CH2-2e-+H2O===CH3CHO+2H+
C. 电子移动方向:电极a→磷酸溶液→电极b
D. 该电池为二次电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有一种变化的反应类型与其他三种变化不同的是( )
A. CH3CH2OH + CH3COOH![]() CH3COOCH2CH3 + H2O
CH3COOCH2CH3 + H2O
B. CH3CH2OH![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O
C. 2CH3CH2OH![]() CH3CH2OCH2CH3 + H2O
CH3CH2OCH2CH3 + H2O
D. CH3CH2OH + HBr=CH3CH2Br + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示为镍锌可充电电池放电时电极发生物质转化的示意图,电池使用KOH和K2Zn(OH)4为电解质溶液,下列关于该电池说法正确的是
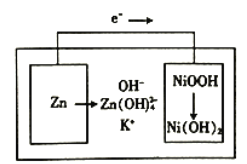
A. 放电时溶液中的K+移向负极 B. 充电时阴极附迁的pH会降低
C. 理论上负极质量每减少6.5g,溶液质量增加6.3g D. 放电时正极反应为H++NiOOH+e-=Ni(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学探究KI的化学性质。
(1)KI组成中含有钾元素,可知它能发生__________反应。
(2)①根据碘元素的化合价可推知KI有__________性。
②与KI反应,能体现上述性质的试剂有_________(填序号)
a、Fe2+ b、Fe3+ c、Br- d、Cl2
(3)兴趣小组的同学们猜测:Cu2+有可能氧化I-,为了验证,他们做了如下实验。(已知:CuI为不溶于水的白色沉淀)
操作 | 现象 |
| 溶液分层,上层显紫色,有白色沉淀生成 |
结论:Cu2+_________(填能或不能)氧化I-。若能氧化,写出反应的离子方程式_____________________ (若认为不能氧化,此空不用填写)。
(4)①同学们依据(3)的结论推测:Ag+能氧化I-,原因为___________。
他们做了如下实验进行探究
实验一:
操作 | 现象 |
| 生成黄色沉淀 |
②发生反应的化学方程式为_________________________________。
实验二:
操作 | 现象 |
| 3分钟后KI溶液开始变黄,随后溶液黄色加深,取出该烧杯中溶液滴入盛有淀粉溶液的试管,溶液变蓝。 |
③甲同学认为根据上述实验现象不能说明Ag+能氧化I-,原因是_______________________________。
乙同学在上述实验基础上进行了改进,并得出结论:Ag+能氧化I-。发生反应的离子方程式为____________________________________。
由以上两个实验得出的结论为________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com