
����Ŀ�������£���0.01mol/LNaOH��Һ�ζ�20.00mL0.01mol/LCH 3COOH��Һ�����õζ���������ͼ������˵����ȷ����
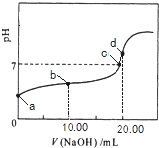
A. b���Ӧ����Һ��: c(OH��)+c(CH3COO��) = c(Na+)+c(H+)
B. a���Ӧ��Һ��pH= 2
C. C���ʾNaOH��Һ��CH3COOH��Һǡ����ȫ��Ӧ
D. d���Ӧ����Һ�У�ˮ�ĵ���̶�С��ͬ���´�ˮ�ĵ���̶�
���𰸡�A
��������A���ɵ���غ��֪��c(OH-)+c(CH3COO-)=c(Na+)+c(H+)��ѡ��A��ȷ��B��CH3COOH�����ᣬ����ȫ���룬��0.01mol/LCH3COOH��ҺpH>2��a���Ӧ��Һ��pH>2��ѡ��B����C��c���ʾNaOH��Һ��CH3COOH��Һ��Ӧ����Һ�����ԣ����ỹû��ȫ��Ӧ��ѡ��C����D��d���Ӧ����ҺΪ��ȫ��Ӧ��Ĵ�������Һ�������Ƶ�ˮ��ٽ�ˮ�ĵ��룬�ʸõ���ˮ�ĵ���̶ȴ���ͬ���´�ˮ�ĵ���̶ȣ�ѡ��D����ѡA��


 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO��H2��һ�������ºϳɼ״��ķ�ӦΪ��CO(g)+2H2(g)![]() CH3OH(g) ��H1�������ݻ���Ϊ1L��a��b��c��d��e����ܱ������зֱ����1molCO��2molH2�Ļ�����壬�����¶ȣ�����ʵ�飬������������ͼ��ͼ1���¶ȷֱ�Ϊ300�� ��500����ܱ������У��״������ʵ�����ͼ2���¶ȷֱ�ΪTl��T5���ܱ������У���Ӧ�����е�5minʱ�״������������������������ȷ����
CH3OH(g) ��H1�������ݻ���Ϊ1L��a��b��c��d��e����ܱ������зֱ����1molCO��2molH2�Ļ�����壬�����¶ȣ�����ʵ�飬������������ͼ��ͼ1���¶ȷֱ�Ϊ300�� ��500����ܱ������У��״������ʵ�����ͼ2���¶ȷֱ�ΪTl��T5���ܱ������У���Ӧ�����е�5minʱ�״������������������������ȷ����
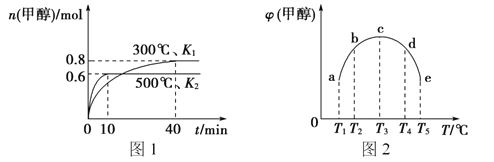
A. �÷�Ӧ�ġ�H1>0����K1>K2
B. ������c�е�ƽ��״̬ת�䵽����d�е�ƽ��״̬,�ɲ�ȡ�Ĵ�ʩ�����»��ѹ
C. 300��ʱ����ƽ�����������ٳ���0.8molCO, 0.6molH2��0.2molCH3OH��ƽ�������ƶ�
D. 500��ʱ����ƽ�����������ٳ���1molCH3OH������ƽ���H2Ũ�ȺͰٷֺ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������д����л�ѧ�����������ѧ���Ļ�ѧ֪ʶ���ж�����˵���д������
A. ҽ���ϳ����������Ϊ70%-75%�ľƾ���������
B. Ϊ��ֹ���д�Ⱦ���ɽ������Ŵ��رպ���ʳ��Ѭ������������
C. ���ʡ������ʳƷ�ø�������(��ȩ��Һ)���ݷ�������
D. ��մ�����������þƾ�ϴ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1) ______mol CO2�к�����ԭ������1.806��1024��H2O���Ӻ��е���ԭ������ͬ��
(2)0.4 mol SiH4����������ԭ������________g HCl����������ԭ������ȡ�
(3)��״���µļ����һ����̼�Ļ������8.96 L��������Ϊ7.60 g�����������м�������Ϊ____________��һ����̼������Ϊ___________��
(4)�����ʵ���O2�ͳ���(O3)��������֮��Ϊ______________����O2��O3������ȣ�����ԭ����֮��Ϊ_____________��
(5)��MgCl2��KCl��Na2SO4�������ʵĻ��Һ�У���֪���к�Cl��1.5 mol��K����Na����1.5 mol��Mg2��Ϊ0.5 mol����SO42-������Ϊ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ʣ���ʯī�� ���Ȼ������壻 �۾ƾ��� ������ �ݶ�����̼��
��̼�����ƹ��壻������������Һ�� ��Һ̬��� ���Ȼ������壻 �ⰱ����
��1�������ܵ�����ǣ�______________________________��
��2�����ڷǵ���ʵ��ǣ�___________________________��
������ͭ��һ�ֺ�ɫ���壬������ϡ���ᣬijͬѧ��֪����ϡ�������������(H2O��H����SO42-)��ʹ����ͭ�ܽ⣬�������һ��ͨ����ͼ��ʾ��͢�����ʵ��������̽�����

(3)ͨ��ʵ������֤��_____________________________________________________��
(4)Ҫ֤���������������ܷ�������ͭ��Ӧ������Ҫ����ʵ���͢��ڢ��м���ϡ���������ͭ�ܽ⣬���һ��ȷ�ϵ�ʵ������ǣ��ڢ����ȼ���_________���ټ���___________��
(5)̽�����Ϊ_____________________________________________________________��
(6)��Ӧ�����ӷ���ʽΪ_____________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵȼ��ú��ʯ�͵Ȼ�ʯȼ���ͷų������������NOx����CO2��SO2�����壬������Ⱦ�������Է���������������̼����������ʵ����ɫ�������������á�
��.��������֪��H2��ȼ����Ϊ285.8kJ/mol N2(g) +2O2(g) = 2NO2(g)��H = +133kJ/mol��H2O(g) = H2O(l) ��H = -44kJ/mol�����������£�H2��ԭNO2����ˮ���������������ʵ��Ȼ�ѧ����ʽΪ_____________________��
��.��̼����2L�ܱ������м���2molCO2��6molH2�����ʵ��Ĵ��������£�������Ӧ��CO2(g) + 3H2(g) ![]() CH3OH(l) + H2O(l) ��H < 0
CH3OH(l) + H2O(l) ��H < 0
��1���ٸ÷�Ӧ�Է����е�������__________������¡��������¡��������¶ȡ�����
������������˵���˷�Ӧ�ﵽƽ��״̬����___________��
a.��������ƽ��ʽ�����ֲ��� ��b.CO2��H2������������ֲ��䣻
c. CO2��H2��ת������� ��d.���������ܶȱ��ֲ���
e.1molCO2���ɵ�ͬʱ��3molH��H������
��CO2��Ũ����ʱ�䣨0~t2���仯��ͼ��ʾ����t2ʱ�������ݻ���Сһ����t3ʱ�ﵽƽ�⣬t4ʱ�����¶ȣ�t5ʱ�ﵽƽ�⣬�뻭��t2~t6��CO2��Ũ����ʱ��ı仯_____��

��2���ı��¶ȣ�ʹ��ӦCO2(g) + 3H2(g) ![]() CH3OH(g) + H2O(g) ��H < 0�е��������ʶ�Ϊ��̬����ʼ�¶������ͬ��T1�桢2L�ܱ�����)����Ӧ�����в������ݼ��±���
CH3OH(g) + H2O(g) ��H < 0�е��������ʶ�Ϊ��̬����ʼ�¶������ͬ��T1�桢2L�ܱ�����)����Ӧ�����в������ݼ��±���

�ٴﵽƽ��ʱ����Ӧ��Աȣ�ƽ�ⳣ��K(I)_______K(II)���>������<����=������ͬ����ƽ��ʱCH3OH��Ũ��c(I)_______c(II)��
�ڶԷ�Ӧ��ǰ10min�ڵ�ƽ����Ӧ����v(CH3OH)=_______________�����������������£���30minʱֻ�ı��¶�ΪT2 �棬��ʱH2�����ʵ���Ϊ3.2mol����T1______T2���>������<����=��������30minʱ���������ٳ���1molCO2��1molH2O(g)����ƽ��_________�ƶ��������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤��������ֵ�������й������������
A. 80gCuO��Cu2S�Ļ�����У�����ͭԭ����ΪNA
B. 1molNaBH4������ˮ��Ӧ(NaBH4+H2O=NaBO2+H2��)ʱת�Ƶĵ�����Ϊ:4NA
C. pH=13��Ba(OH)2��Һ�У�����OH-0.2NA��
D. �ܱ�������PCl3��Cl2��Ӧ����molPCl5(g)������2A��P-C1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����ijNa2CO3��Һ�м���ϡ���ᣬ��Һ�к�̼�������ʵ����������գ�����ҺpH�仯�IJ��������ͼ��ʾ������˵������ȷ����
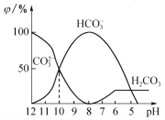
A. Na2CO3��Һ��c(Na+)=c(CO32-��+ c(HCO3-��+ c(H2CO3��
B. pH=8ʱ����Һ��c(Cl-)=c(Na+)
C. pH =7ʱ����Һ�е�c(Na+)>c(Cl-)>c(HCO3-)>c(H+)=c(OH-)
D. 25��ʱ��CO32-+H2O![]() HCO3-+OH-��Kh=10��10mol��L��1
HCO3-+OH-��Kh=10��10mol��L��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com