
【题目】设NA为阿伏伽德罗常数的值。下列有关叙述错误的是
A. 80gCuO和Cu2S的混合物中,所含铜原子数为NA
B. 1molNaBH4与足量水反应(NaBH4+H2O=NaBO2+H2↑)时转移的电子数为:4NA
C. pH=13的Ba(OH)2溶液中,含有OH-0.2NA个
D. 密闭容器中PCl3与Cl2反应生成molPCl5(g),增加2A个P-C1键
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000mol·L-1NaOH溶液滴定20.00mL0.1000 mol·L-1的CH3COOH溶液所得滴定曲线如图。下列说法正确的是
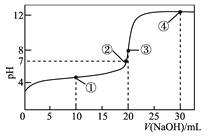
A. 点①所示溶液中:c(Na+)+c(H+)<CH3COOH)+c(OH-)
B. 点②所示溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH)
C. 点③所示溶液中:c(H+)= c(CH3COOH)+c(OH-)
D. 点④所示溶液中:2c(OH-)-2c(H+)= c(CH3COO-)+3c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A是一种重要的化工原料,其气体密度是相同条件下H2的14倍,E是一种能使溴的四氯化碳溶液褪色的乙酸酯。A、B、C、D、E在一定条件下存在如下转化关系:
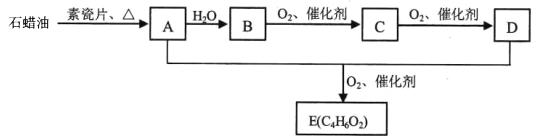
请回答:
(1)有机物C中含有的官能团名称是________ ;工业上,由石蜡油→ A的加工过程称为________。
(2)写 出 A+D+O2→ E的化学反应方程式________。
(3)下列说法不正确的是________。
A,75%(体积分数)的B溶液常用于医疗消毒
B.有机物E在 碱性条件下可发生皂化反应
C.有机物A能 与溴发生氧化反应使溴水褪色
D.用新制银氨溶液可鉴别有机物C、D、E
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.01mol/LNaOH溶液滴定20.00mL0.01mol/LCH 3COOH溶液,所得滴定曲线如右图。下列说法正确的是
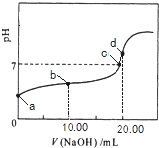
A. b点对应的溶液中: c(OH—)+c(CH3COO—) = c(Na+)+c(H+)
B. a点对应溶液的pH= 2
C. C点表示NaOH溶液与CH3COOH溶液恰好完全反应
D. d点对应的溶液中,水的电离程度小于同温下纯水的电离程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】法医常用马氏试砷法检验是否砒霜( As2O3)中毒,涉及的反应如下:
I:6Zn+As2O3+12HCl=6ZnCl2+2AsH3(砷烷)↑+3H2O
Ⅱ:2AsH3=2As(黑色砷镜)+3H2
(1)写出砷的基态原子价电子排布图______________。
(2)砷烷的空间结构为_______;砷烷中心原子杂化方式为________。
(3)砷烷同族同系列物质相关性质如下表:
NH3 | PH3 | AsH3 | SbH3 | |
熔点/℃ | -77.8 | -133.5 | -116.3 | -88 |
沸点/℃ | -34.5 | -87.5 | -62.4 | -18.4 |
从PH3→AsH3→SbH3熔沸点依次升高的原因是_________;NH3分子例外的原因是_______。
(4)第一电离能数据I(As)>I(Se),可能的原因是_____________。
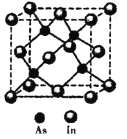
(5)砷与铟(In)形成的化合物(X)具有优良的光电性能,广泛应用于光纤通信用激光器,其晶胞结构如图所示,则其化学式为______;晶胞边长a= 666.67pm,则其密度为_____g/cm3(边长a可用![]() 近似计算,设NA=6.0×1023/mol)。
近似计算,设NA=6.0×1023/mol)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用18 mol·L-1 浓硫酸配制90 mL 3.0 mol·L-1 稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积
②量取一定体积的浓硫酸
③溶解
④
⑤转移、洗涤
⑥定容、摇匀
⑦装瓶贴标签
完成下列问题:
(1)所需浓硫酸的体积是_____________,量取浓硫酸所用的量筒的规格是 _____________(从下列中选用A.10 mL B.25 mL C.50 mL D.100 mL)。浓硫酸稀释的操作______________。
(2)第④步实验的操作是_______________________________________________________
(3)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.用量筒量取浓硫酸后洗涤量筒并将洗涤液注入容量瓶内___________________;
B.容量瓶用蒸馏水洗涤后残留有少量的水________________;
C.所用过的烧杯、玻璃棒未洗涤________________;
D.定容时俯视刻度线________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚![]() ,同时利用此装置的电能在铁上镀铜,下列说法正确的是
,同时利用此装置的电能在铁上镀铜,下列说法正确的是
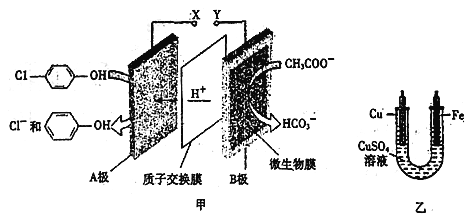
A. 当外电路中有0.2mole-转移时,A极区增加的H+的个数为0.2NA
B. A极的电极反应式为![]()
C. 铁电极应与Y相连接
D. 反应过程中甲中右边区域溶液pH逐渐升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将11.65gBaSO4粉末置于盛有250mL蒸馏水的烧杯中,然后向烧杯中加入Na2CO3固体(忽视溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是
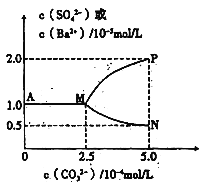
A. 相同温度时,Ksp(BaSO4)>Ksp(BaCO3)
B. BaSO4在水中的溶解度、Ksp均比在BaCl2溶液中的大
C. 若使0.05molBaSO4全部转化为BaCO3,至少要加入1.25molNa2CO3
D. 0.05molBaSO4恰好全部转化为BaCO3时,溶液中离子浓度大小为:c(CO32-)>c(SO42-)>c(Ba2+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有一种变化的反应类型与其他三种变化不同的是( )
A. CH3CH2OH + CH3COOH![]() CH3COOCH2CH3 + H2O
CH3COOCH2CH3 + H2O
B. CH3CH2OH![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O
C. 2CH3CH2OH![]() CH3CH2OCH2CH3 + H2O
CH3CH2OCH2CH3 + H2O
D. CH3CH2OH + HBr=CH3CH2Br + H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com