
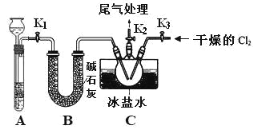
【题目】亚硝酰氯(NOCl)是有机物合成中的重要试剂,为红褐色液体或黄色气体,室温下为不稳定的黄色气体, 具刺鼻恶臭味,遇水分解,某学习小组用 C12 和 NO 制备 NOCl 装置如图。下列说法错误的是
A.氯气在反应中做氧化剂
B.装入药品后,要先打开 K2、K3,反应一段时间后,再打开 K1
C.利用 A 装置还可以做 Na2O2 和水制氧气的实验
D.若没有 B 装置,C 中可能发生反应:2NOCl+H2O=2HCl+NO↑+NO2↑
【答案】C
【解析】
由装置A制备NO,用铜和稀硝酸反应制备,制得的NO中可能有挥发的硝酸,故装置B用来净化和干燥NO,将氯气和NO干燥后在装置C中发生反应,在冰盐中冷凝收集NOCl,氯气、NO以及NOCl均不能排放到空气中,用氢氧化钠溶液吸收,NOCl遇水易水解,故在收集装置和尾气处理装置之间应该需加一个干燥装置。
A. 根据Cl2和NO反应生成了NOCl,氯元素化合价降低,得电子,Cl2为氧化剂,故A正确;
B. 先打开K2、K3,通入一段时间氯气,排尽三颈烧瓶中的空气,防止NO、NOCl 变质,然后再打开K1,通入NO,故B正确;
C. 该装置能制备用块状固体和液体反应生成的气体,过氧化钠为粉末状固体,所以不可以做Na2O2和水制氧气的实验,故C错误;
D. 若无装置B,C中亚硝酰氯与水反应生成氯化氢、NO和二氧化氮,可能发生反应:2NOCl+H2O═2HCl+NO↑+NO2↑,故D正确;
故选:C。


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:
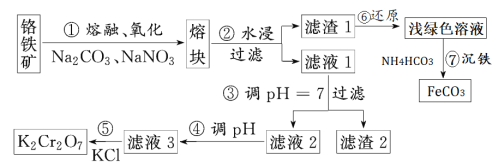
【题目】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质。制备流程如图所示:
回答下列问题:
(1)步骤①的主要反应为:FeO·Cr2O3+Na2CO3+NaNO3→Na2CrO4+Fe2O3+CO2+NaNO2。上述反应配平后NaNO3与FeO·Cr2O3与的系数比为___。该步骤不能使用陶瓷容器,原因是___。
(2)滤渣1中主要成分是___,滤渣2中含量最多的金属元素名称是___。
(3)步骤④调滤液2的pH变小的目的是___(用离子方程式表示)。
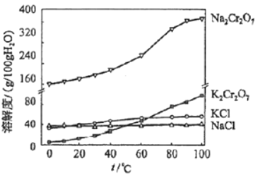
(4)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,___、___,过滤得到K2Cr2O7固体。该反应的反应类型是___。
(5)写出步骤7中涉及的离子方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过渡金属元素在日常生活中有广泛的应用。
(1)金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价层电子的排布式为 __________;基态 Mn原子核外有____种运动状态不同的电子,M层的电子云有_______种不同的伸展方向。
(2)第四周期元素的第一电离能随原子序数增大,总趋势是逐渐增大的,但Ga的第一电离能明显低于Zn,原因是 ____________________________________
(3)NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验 K+的存在。与NO2-互为等电子体的微粒__________(写出一种),K3[Co(NO2)6]中存在的作用力有___________a.σ键 b.π键 c.配位键 d.离子键 e.范德华力
(4)锰的一种配合物的化学式为 Mn(BH4)2(THF)3,BH4-的空间构型为____________
(5)FeO 是离子晶体,其晶格能可通过下图中的 Born—Haber 循环计算得到。
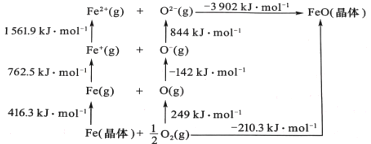
可知,O原子的第一电子亲和能为 ________kJmol-1,FeO晶格能为________kJmol-1。
(6)铜与氧可形成如图所示的晶胞结构,其中 Cu 均匀地分散在立方体内部,a、b的坐标参数依次为(0,0,0)、(1/2,1/2,1/2),则 d 点的坐标参数为_______________,已知该晶体的密度为ρgcm-3,NA是阿伏伽德罗常数的值,则晶胞参数为_________pm
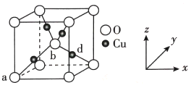
(列出计算式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿(CuFeS2)是炼铜的主要矿物,在野外很容易被误会为黄金,因此被称为愚人金。回答下列问题:
(1)处于激发态的S原子,其中1个3s电子跃迁到3p轨道上,该激发态S原子的核外电子排布式为__。同族元素的氢化物中,H2O比H2Te沸点高的原因是__。
(2)检验Fe2+的试剂有多种,其中之一是铁氰化钾(K3[Fe(CN)6]),又称赤血盐。
①在配合物K3[Fe(CN)6]中,易提供孤电子对的成键原子是__(填元素名称),含有12molσ键的K3[Fe(CN)6]的物质的量为__mol。
②赤血盐中C原子的杂化方式为__;C、N、O三种元素第一电离能由大到小的排序为___;写出与CN-互为等电子体的一种化合物的化学式__。
③Fe、Na、K的晶胞结构相同,但钠的熔点比钾更高,原因是___。
(3)CuFeS2的晶胞结构如图所示。已知:晶胞参数a=0.524nm,c=1.032nm。则CuFeS2的晶胞中每个Cu原子与__个S原子相连,晶体密度ρ=__g·cm-3(列出计算表达式)。
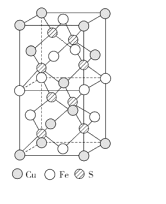
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,由图中数据分析,反应物是____,t2时,N的浓度是_______________;若t2=1 min,从反应开始到t2 ,M的平均反应速率为_____________; 该反应的化学方程式为______;在反应达到化学平衡时,各组分的浓度保持______(填“相等”或“不变”)且_______(填“一定”或“不一定”相等,各物质的反应速率之比_______(填“一定”或“不一定”)等于化学计量数之比。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列转化过程分析不正确的是
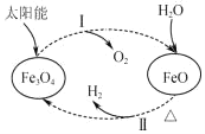
A.Fe3O4 中 Fe 元素的化合价为+2、+3
B.过程Ⅰ中每消耗 58 g Fe3O4 转移 1 mol 电子
C.过程Ⅱ的化学方程式为 3FeO+H2O![]() Fe3O4+H2↑
Fe3O4+H2↑
D.该过程总反应为 2H2O═2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组用如装置比较氯、溴、碘的非金属性强弱实验(夹持仪器已略去,气密性已检验)。
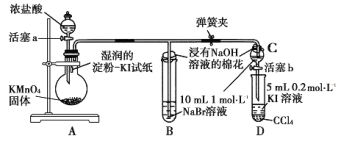
实验步骤:
①打开弹簧夹,打开活塞a,滴加浓盐酸;
②当B和C中的溶液都变为黄色时,夹紧弹簧夹;
③当B中溶液由黄色变为棕红色时,关闭活塞a;
④打开活塞b,将少量C中溶液滴入试管D中,关闭活塞b,取下试管D振荡,静置后CCl4层变为紫红色。请回答:
(1)装置A中证明氯的非金属性强于碘的实验现象是_______________________。
(2)B中溶液发生反应的离子方程式是____________________________________。
(3)步骤③实验的目的是确认C的黄色溶液中无_____(填化学式)。步骤④能否说明非金属性:Br>I_______(填“能”或“否”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 的两种一元酸
的两种一元酸![]() 和
和![]() ,体积均为
,体积均为![]() ,稀释过程中
,稀释过程中![]() 与溶液体积的关系如图所示。分别滴加
与溶液体积的关系如图所示。分别滴加![]() 溶液(
溶液(![]() )至
)至![]() ,消耗
,消耗![]() 溶液的体积为
溶液的体积为![]() 、
、![]() ,则( )
,则( )
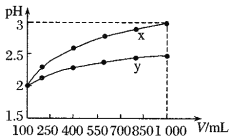
A.![]() 为弱酸,
为弱酸,![]()
B.![]() 为强酸,
为强酸,![]()
C.![]() 为弱酸,
为弱酸,![]()
D.![]() 为强酸,
为强酸,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学按照实验要求,用50 mL 0.50 mol·L-1的盐酸与50 mL 0.55 mol·L-1的NaOH 溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量计算中和热。下列说法中正确的是

A. 实验过程中没有热量损失
B. 图中实验装置缺少环形玻璃搅拌棒
C. 烧杯间填满碎纸条的作用是固定小烧杯
D. 若烧杯上不盖硬纸板,测得的ΔH将偏小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com