
| 3000m |
| 112V |
| 3000m |
| 112V |
| m |
| M |
| V |
| Vm |
| m |
| 56 |
| 3 |
| 2 |
| 3m |
| 112 |
| ||
| V×10-3L |
| 3000m |
| 112V |
| m |
| M |
| V |
| Vm |
| m?Vm |
| V |
| 1.28g×22.4L/mol |
| 0.448L |
| 1 |
| 4 |
| 11g |
| 44g/mol |
| 1 |
| 4 |
| 4g |
| 32g/mol |
| 1 |
| 8 |
| 1 |
| 4 |
| 1 |
| 4 |
| 1 |
| 8 |
| 3000m |
| 112V |


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:阅读理解
 Ⅰ.玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流.下列有关实验过程中,肯定不需要使用玻璃棒进行操作的是
Ⅰ.玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流.下列有关实验过程中,肯定不需要使用玻璃棒进行操作的是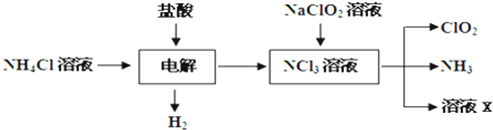
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
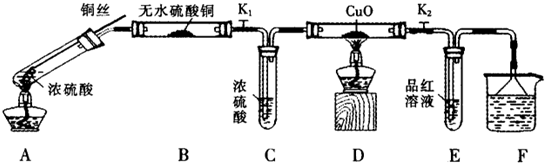
| 硫酸/mol?L-1 | 黑色物质出现的温度/℃ | 黑色物质消失的温度/℃ |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省乐山市高三“一调”考试理综化学试卷(解析版) 题型:实验题
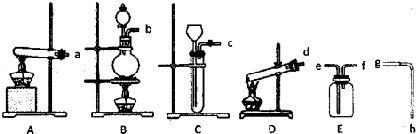
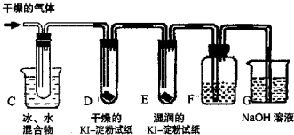
Ⅰ.玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流。下列有关实验过程中,肯定不需要使用玻璃棒进行操作的是 (可以多选)
A.用pH试纸测定Na2CO3溶液的pH
B.从氯酸钾和二氧化锰制取氧气的剩余固体中提取KCl
C.实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
D.配制一定物质的量浓度的氯化钠溶液
E.取某溶液做焰色反应实验,说明该溶液中含有钠元素
F.用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
G.促使过饱和的硝酸钾溶液析出晶体
Ⅱ.二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。ClO2是一种黄绿色的气体,易溶于水。实验室以NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:

(1)写出电解时发生反应的化学方程式: ;
(2)除去ClO2中的NH3可选用的试剂是 ;(填序号)
A.饱和食盐水 B.碱石灰 C.浓硫酸 D.水
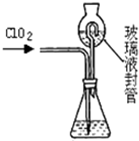
(3)测定ClO2(如右图)的过程如下:在锥形瓶中加入足量的碘化钾,用100mL水溶解后,再加3mL足量硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收(假设吸收完
全);将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用c mol/L硫代硫酸钠标准溶液滴定
(I2+2S2O32-=2I- +S4O62-),共用去V mL硫代硫酸钠溶液。

① 装置中玻璃液封管的作用是 ;
② 请写出上述二氧化氯气体与碘化钾溶液反应的离子方程式 ;
③ 测得ClO2的质量m(ClO2)= 。(用含c、V的代数式表示)
查看答案和解析>>
科目:高中化学 来源:2012年苏教版高中化学选修6 6.1食醋总酸含量的测定练习卷(解析版) 题型:填空题
(1)邻苯二甲酸氢钾(相对分子质量为204.2)可以用于标定NaOH溶液的浓度,反应如下:KHC8H4O4+NaOH===KNaC8H4O4+H2O
准确称取0.5105 g KHC8H4O4晶体,溶于水后加入酚酞指示剂,用NaOH溶液滴定溶液由无色变为浅红色,消耗20.00 mL NaOH。计算NaOH溶液的浓度为________(结果保留四位有效数字)。
(2)测定食醋的总酸度。食酸中除醋酸(CH3COOH)外,还含有少量其他有机酸。食醋的总酸度以每1000 mL食醋中含醋酸(其他酸也折算作醋酸)的质量(g)表示,通常写作w(CH3COOH)。用移液管移取50.00 mL市售食醋,置于250 mL容量瓶中,用水稀释至刻度。再从中量取25.00 mL,用(1)小题已知浓度的NaOH溶液滴定,消耗碱液的体积为V(mL),请写出w(CH3COOH)的计算式____________________________________________________。
(3)已知0.1 mol·L-1邻苯二甲酸溶液的pH大于1,取等体积的邻苯二甲酸溶液和某KOH溶液混合,测得混合溶液的pH等于7,则碱与酸的浓度比值x为________(选填下列选项编号)。
A.x>2 B.x=2
C.2>x>1 D.x=1
E.1>x> F.x=
F.x=
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com