
焦亚硫酸钠(Na2S2O5)在食品加工中常用作防腐剂、漂白剂和疏松剂。焦亚硫酸钠为黄色结晶粉末,150℃时开始分解,在水溶液或含有结晶水时更易被空气氧化。实验室制备焦亚硫酸钠过程中依次包含以下几步反应:
2NaOH + SO2 = Na2SO3 + H2O……(a)
Na2SO3+ H2O + SO2 = 2NaHSO3 ……(b)
2NaHSO3 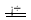 Na2S2O5 + H2O……(c)
Na2S2O5 + H2O……(c)
实验装置如下:

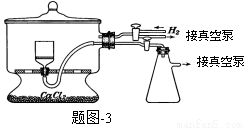
(1)实验室可用废铝丝与NaOH溶液反应制取H2,制取H2的离子方程式为 。
(2)题图-1装置中,导管X的作用是 。
(3)通氢气一段时间后,以恒定速率通入SO2,开始的一段时间溶液温度迅速升高,随后温度缓 慢变化,溶液开始逐渐变黄。“温度迅速升高”的原因为 ;
慢变化,溶液开始逐渐变黄。“温度迅速升高”的原因为 ;
实验后期须保持温度在约80℃,可采用的加热方式为 。
(4)反应后的体系中有少量白色亚硫酸钠析出,参照题图-2溶解度曲线,除去其中亚硫酸钠固体的方法是 ;然后获得较纯的无水Na2S2O5应将溶液冷却到30℃左右抽滤,控制“30℃左右”的理由是 。
(5)用题图-3装置干燥Na2S2O5晶体时,通入H2的目的是 ;真空干燥的优点是 。
(6)测定产品中焦亚硫酸钠的质量分数常用剩余碘量法。已知:S2O52-+2I2+3H2O=2SO42-+4I-+6H+;2S2O32-+I2 = S4O62-+2I-
请补充实验步骤(可提供的试剂有:焦亚硫酸钠样品、标准碘溶液、淀粉溶液、酚酞溶液、标准Na2S2O3溶液及蒸馏水)。
①精确称取产品0.2000g放入碘量瓶(带磨口塞的锥形瓶)中。
②准确移取一定体积和已知浓度的标准碘溶液(过量)并记录数据,在暗处放置5min,然后加入5mL冰醋酸及适量的蒸馏水。
③用标准Na2S2O3溶液滴定至接近终点。④ 。 ⑤ 。
⑥重复步骤①~⑤;根据相关记录数据计算出平均值。
科目:高中化学 来源:2015-2016学年浙江省高一上10月月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.NH3的水溶液能导电,所以NH3是电解质
B.BaSO4其水溶液几乎不导电,但BaSO4是电解质
C.液溴不导电,所以液溴是非电解质
D.食盐水能导电,故其属于电解质
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高一上学期期中测试化学试卷(解析版) 题型:计算题
把6.5gZn放入足量的稀盐酸中,锌完全反应。计算:
(1)参加反应的HCl的物质的量。
(2)生成氢气的体积(标准状况)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二上学期期中测试化学试卷(解析版) 题型:实验题
50ml0.50mol•L﹣1盐酸与50mL0.55mol•L﹣1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
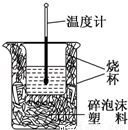
(1)从实验装置上看,有两处缺点,其一是有 处错误安
处错误安 装会导致热量散失较大,应该加 ,其二尚缺少一种玻璃仪器是 。
装会导致热量散失较大,应该加 ,其二尚缺少一种玻璃仪器是 。
(2)若操作时分几次注入反应液,求得的反应热数值 (填“偏大”“偏小”或“无影响 ”).
”).
(3)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会 (填“偏大”、“偏小”或“无影响”).
(4)若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差t2﹣t1分别为①2.2℃②2.4℃③3.4℃,则最终代入计算式的温差均值为 ℃
查看答案和解析>>
科目:高中化学 来源:2016届福建省四地六校高三上学期第二次联考化学试卷(解析版) 题型:选择题
下列实验过程中产生的现象与右边座标图形相符合的是
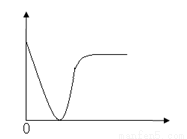
A.稀盐酸滴加到一定量NaOH溶液中(横坐标是稀盐酸的体积,纵坐标为钠离子物质的量)
B.铁粉加到一定量CuSO4溶液中(横坐标是铁粉的质量,纵坐标为沉淀质量)
C.CO2通入一定量NaOH溶液中(横坐标是CO2的体积,纵坐标为溶液的导电能力)
D.稀硫酸滴加到Ba(OH)2溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上学期期中测试化学试卷(解析版) 题型:填空题
用化学用语完成以下各题:
(1)硫化氢在水中的电离方程式
(2)已知通常状况下,1.6g甲烷完全燃烧放出89.03kJ的热量,表示甲烷燃烧热的热化学方程式为
(3)通常状况,稀硫酸和氢氧化钠溶液发生中和反应的热化学方程式可表示为
(4)工业上采用合适的条件合成氨,其化学反应方程式为
(5)用CO可以合成甲醇。已知:
CH3OH(g)+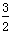 O2(g)===CO2(g)+2H2O(l) ΔH=-764.6kJ·mol-1
O2(g)===CO2(g)+2H2O(l) ΔH=-764.6kJ·mol-1
CO(g)+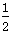 O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
H2(g)+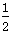 O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
则CO(g)与H2(g)合成 CH3OH(g)的 热化学方程式为
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省宜昌市高二上期中测试化学试卷(解析版) 题型:选择题
已知3mol碳在2mol氧气中燃烧,至反应物耗尽,测得放出热量a kJ。又知0.1mol碳完全燃烧,放出热量为 b kJ。则热化学方程式C(s)+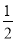 O2(g)===CO(g) ΔH=Q中Q等于
O2(g)===CO(g) ΔH=Q中Q等于
A.-(a-b) kJ·mol-1
B.-(a+b) kJ·mol-1
C.-(5a-0.5b) kJ·mol-1
D.-(0.5a-5b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省滕州市高一上学期期中测试化学试卷(解析版) 题型:选择题
下列对于“摩尔”的说法正确的是
A.摩尔是国际科学界建议采用的一种物理量
B.摩尔可以把物质的宏观数量与微观粒子的数量联系起来
C.1摩尔是0.012 kg碳原子所含有的碳原子的物质的量
D.摩尔是物质的量的单位,简称摩,符号为mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省扶余市高一上学期期中测试化学试卷(解析版) 题型:选择题
在下列物质分类中,前者包括后者的是
A.化合物、电解质 B.电解质、干冰 C.溶液、胶体 D.溶液、分散系
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com