
【题目】现有四种元素的基态原子的电子排布式如下: ①1s22s22p63s23p4 ②1s22s22p63s23p3 ③1s22s22p3 ④1s22s22p5 则下列有关比较中正确的是
A. 电负性:④>③>②>① B. 原子半径:④>③>②>①
C. 第一电离能:④>③>②>① D. 最高正化合价:④>③=②>①
【答案】C
【解析】
①1s22s22p63s23p4为S,②1s22s22p63s23p3为P,③1s22s22p3为N,④1s22s22p5为F。A项,根据同周期从左到右元素的电负性增大,同主族从上到下元素的电负性减小,电负性:④(F)![]() ③(N)
③(N)![]() ②(P)、①(S)
②(P)、①(S)![]() ②(P),A项错误;B项,根据“层多径大,序大径小”,原子半径:②(P)
②(P),A项错误;B项,根据“层多径大,序大径小”,原子半径:②(P)![]() ①(S)
①(S)![]() ③(N)
③(N)![]() ④(F),B项错误;C项,根据同周期从左到右第一电离能呈增大趋势(IIA、VA族反常),同主族从上到下第一电离能减小,第一电离能:④(F)
④(F),B项错误;C项,根据同周期从左到右第一电离能呈增大趋势(IIA、VA族反常),同主族从上到下第一电离能减小,第一电离能:④(F)![]() ③(N)
③(N)![]() ②(P)
②(P)![]() ①(S),C项正确;D项,④(F)没有正价,S的最高正化合价为+6价,N、P的最高正化合价都为+5价,D项错误;答案选C。
①(S),C项正确;D项,④(F)没有正价,S的最高正化合价为+6价,N、P的最高正化合价都为+5价,D项错误;答案选C。


科目:高中化学 来源: 题型:
【题目】已知:
①2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
②2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1
③H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1
则下列说法正确的是
A. H2(g)的燃烧热为571.6 kJ·mol-1
B. ![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)===
Ba(OH)2(aq)===![]() BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
C. 同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多
D. 2molH2(g)在足量氧气中完全燃烧生成气态水放出热量大于571.6kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水四氯化锡常用作媒染剂和有机合成中的氯化催化剂。实验室可用熔融的锡(熔点232℃)与Cl2反应制备SnCl4,装置如图。
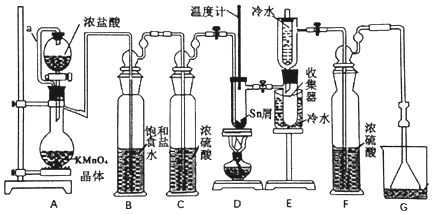
已知:①SnCl2、SnCl4有关物理性质:
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | ﹣33 | 114 |
②SnCl4极易水解生成SnO2H2O。
回答下列问题:
(1)导管a的作用是____________________________________________________________,装置A中发生反应的离子方程式为________________________________________。
(2)当观察到装置F液面上方______________时才开始点燃D处的酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的是____________________________。
(3)若上述装置中缺少装置C(其它均相同),则D处具支试管中发生的主要副反应化学方程式为____________________________________________________________。
(4)Cl2和锡的反应产物有SnCl4和SnCl2,为防止产品中带入过多的SnCl2,可采取的措施是____________________________________________________________。
(5)滴定分析产品中2价Sn(II)的含量:用分析天平称取5.000 g产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用0.1000 molL﹣1的碘标准溶液滴定至终点时消耗20.00 mL,则产品中Sn(II)的含量为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子或离子中键角由大到小排列的是
①BCl3 ②NH3 ③H2O ④PCl4+ ⑤BeCl2
A. ⑤④①②③ B. ④①②⑤③ C. ⑤①④②③ D. ③②④①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下将容器中充入0.8molSO2, 0.2molO2, 0.6molSO3体积为2L的密闭容器中,发生反应:2SO2 (g)+ O2 (g)2SO3(g),达到化学反应限度时,SO3物质的量可能是:( )mol
A. 0B. 0.3C. 1.0D. 1.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面对宏观事实的微观解释不正确的是( )
A.湿衣服晾在阳光充足的地方,容易干――温度升高,分子运动加快
B.固体碘(I2)和碘蒸气(I2)都能使淀粉溶液变蓝――同种分子化学性质相同
C.液态水变为水蒸气――分子体积变大
D.氧化汞受热分解生成汞和氧气――化学反应中分子发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的酸度(用AG表示)定义为c(H+)与 C(OH-)比值的对数,即AG=lg![]() 。常温下,下列各组离子在AG=12的无色溶液中能大量共存的是( )
。常温下,下列各组离子在AG=12的无色溶液中能大量共存的是( )
A. Mg2+、Ca2+、HCO3-、Cl-
B. K+、I-、SO42-、Br-
C. MnO4-、Ca2+、Cl-、NO3-
D. Na+、Al(OH)4-、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
① H2(g)+![]() O2(g)=H2O(l) ΔH =―285kJ/mol
O2(g)=H2O(l) ΔH =―285kJ/mol
② H2(g)+![]() O2(g)=H2O(g) ΔH =―241.8kJ/mol
O2(g)=H2O(g) ΔH =―241.8kJ/mol
③ C(s)+![]() O2(g)=CO(g) ΔH =―110.4 kJ/mol
O2(g)=CO(g) ΔH =―110.4 kJ/mol
④ C(s)+ O2(g)=CO2(g) ΔH =―393.5 kJ/mol
回答下列各问:
(1)上述反应中属于放热反应的是___________。
(2)C的燃烧热为_________________。
(3)燃烧10g H2生成液态水,放出的热量为_____________________。
(4)CO燃烧的热化学方程式为______________________。
(5)为了控制温室效应,各国科学家提出了不少设想。有人根据液态CO2密度大于海水密度的事实,设想将CO2液化后,送入深海海底,以减少大气中的CO2。为使CO2液化,可采取的措施________。
a 减压、升温 b 增压、降温
c 减压、降温 d 增压、升温
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com