
����Ŀ����֪�����Ȼ�ѧ����ʽ��
�� H2(g)+![]() O2(g)��H2O(l) ��H ���D285kJ/mol
O2(g)��H2O(l) ��H ���D285kJ/mol
�� H2(g)+![]() O2(g)��H2O(g) ��H ���D241.8kJ/mol
O2(g)��H2O(g) ��H ���D241.8kJ/mol
�� C(s)+![]() O2(g)��CO(g) ��H ���D110.4 kJ/mol
O2(g)��CO(g) ��H ���D110.4 kJ/mol
�� C(s)+ O2(g)��CO2(g) ��H ���D393.5 kJ/mol
�ش����и��ʣ�
��1��������Ӧ�����ڷ��ȷ�Ӧ����___________��
��2��C��ȼ����Ϊ_________________��
��3��ȼ��10g H2����Һ̬ˮ���ų�������Ϊ_____________________��
��4��COȼ�յ��Ȼ�ѧ����ʽΪ______________________��
��5��Ϊ�˿�������ЧӦ��������ѧ������˲������롣���˸���Һ̬CO2�ܶȴ��ں�ˮ�ܶȵ���ʵ�����뽫CO2Һ������������ף��Լ��ٴ����е�CO2��ΪʹCO2Һ�����ɲ�ȡ�Ĵ�ʩ________��
a ��ѹ�����¡��������������� b ��ѹ������
c ��ѹ�����¡��������������� d ��ѹ������
���𰸡��٢ڢۢܣ� 393.5 kJ/mol�� 1425 kJ CO(g)+![]() O2(g)��CO2(g) ��H ���D283.1kJ/mol�� b
O2(g)��CO2(g) ��H ���D283.1kJ/mol�� b
��������
��1�����ȷ�Ӧ����H<0��
��2��ȼ���ȣ�1 mol��������ȫȼ�������ȶ���������ʱ���ų���������
��3���������ʵ���������ϵ����ų���������
��4���ɸ�˹���ɼ��㣻
��5����ѹ���¿ɼ�С����֮��ļ����ʹ������̼�������ΪҺ�塣
��1�����ȷ�Ӧ����H<0���ʢ٢ڢۢܶ��Ƿ��ȷ�Ӧ��
��2��1 mol��������ȫȼ�������ȶ���������ʱ���ų�������Ϊȼ���ȣ���Ӧ����C��ȫȼ�գ�C��ȼ����Ϊ393.5 kJ/mol��
��3��ȼ��10g H2��5mol H2����Һ̬ˮ���ų�������Ϊ285kJ![]() 5=1425 kJ��
5=1425 kJ��
��4���ɢ�C(s)+![]() O2(g)��CO(g) ��H ���D110.4 kJ/mol����C(s)+ O2(g)��CO2(g) ��H ���D393.5 kJ/mol����-�ۿɵ�COȼ�յ��Ȼ�ѧ����ʽΪCO(g)+
O2(g)��CO(g) ��H ���D110.4 kJ/mol����C(s)+ O2(g)��CO2(g) ��H ���D393.5 kJ/mol����-�ۿɵ�COȼ�յ��Ȼ�ѧ����ʽΪCO(g)+![]() O2(g)��CO2(g) ��H ���D283.1kJ/mol��
O2(g)��CO2(g) ��H ���D283.1kJ/mol��
��5�������ʵ���̬�仯��֪���ڴ��������£�������̼����ɫ��ζ�����壬�����¶ȵ���31.2��ʱ����ѹ��ʹCO2��ΪҺ̬������ѹ���¿ɼ�С����֮��ļ����ʹ������̼�������ΪҺ�壬��ɽ�CO2Һ������������ף��Լ�С������CO2��Ũ�ȣ���ѡb��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ԫ�صĻ�̬ԭ�ӵĵ����Ų�ʽ���£� ��1s22s22p63s23p4 ��1s22s22p63s23p3 ��1s22s22p3 ��1s22s22p5 �������йرȽ�����ȷ����
A. �縺�ԣ���>��>��>�� B. ԭ�Ӱ뾶����>��>��>��
C. ��һ�����ܣ���>��>��>�� D. ��������ϼۣ���>�ۣ���>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������仯ʾ��ͼ�������Ȼ�ѧ����ʽ��ȷ����

A. 2A��g��+ B(g)=2C��g����H=a��a��0��B. 2A��g��+ B(g)=2C��g����H=a��a��0��
C. 2A + B=2 C��H=a��a��0��D. 2C=2A +B��H=a��a��0��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����е�ʵ�����������������������
A.��25 mL�ļ�ʽ�ζ�����ȡ14.80 mL NaOH��Һ
B.��100 mL��Ͳ��ȡ5.2 mL����
C.��������ƽ��ȡ25.20 g�Ȼ���
D.��150 mL����ƿ����50 mL 0.1 mol/L����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. 500�桢30MPa������0.5mol N2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3(g)������19.3kJ�����Ȼ�ѧ����ʽΪ��N2(g)��3H2(g)![]() 2NH3(g) ��H=��38.6kJ��mol��1
2NH3(g) ��H=��38.6kJ��mol��1
B. �����ȼ����Ϊ-890.3kJ��mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4(g)+2O2(g)=CO2(g)+2H2O(g) ��H= ��890.3kJ��mol-1
C. ԭ����з����ķ�Ӧ�ﵽƽ��ʱ���õ�����е�������
D. 500 mL 2.0 mol��L-1��HCl(aq)��500 mL 2.0 mol��L-1��NaOH(aq)��Ӧ����������������57.3 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA���������ӵ���������ֵ��������Ȼ�ѧ����ʽC2H2(g)��![]() O2(g)===2CO2(g)��H2O(l)����H����1300 kJ��mol��1��˵���У���ȷ������ ��
O2(g)===2CO2(g)��H2O(l)����H����1300 kJ��mol��1��˵���У���ȷ������ ��
A. ת��10NA������ʱ���÷�Ӧ�ų�1300 kJ������
B. ����NA��Һ̬ˮ����ʱ������1300 kJ������
C. ��2NA��̼�����õ��Ӷ�����ʱ���ų�1300 kJ������
D. ��10NA��̼�����õ��Ӷ�����ʱ���ų�1300 kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£��ڱ������ˮϡ�͵Ĺ����У���Һ�ĵ���������I�����ż���ˮ�����V�仯��������ͼ��ʾ������˵����ȷ������ ��
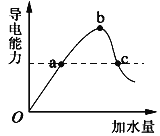
A��a��c����pH��ͬ
B����c��Һ�м�ˮ����Һ����������Ũ�ȶ���С
C������ʪ���pH��ֽ��b��pH���ƫ��
D��![]() b�����c��
b�����c��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£��������ݻ���ͬ�ĺ����ܱ������а���ͬ��ʽͶ�뷴Ӧ�������Ӧ 2SO2(g) + O2(g)![]() 2SO3(g)(����Ӧ����)�������������������˵����ȷ������ ��
2SO3(g)(����Ӧ����)�������������������˵����ȷ������ ��
���� 1 | ���� 2 | ���� 3 | |
��Ӧ�¶� T/K | 700 | 700 | 800 |
��Ӧ��Ͷ���� | 2molSO2�� 1molO2 | 4molSO3 | 2molSO2�� 1molO2 |
ƽ������(SO2 )/mol��L-1��s-1 | ��1 | ��2 | ��3 |
ƽ�� c(SO3 )/ mol��L-1 | c1 | c2 | c3 |
ƽ����ϵ��ѹǿ p/Pa | p1 | p2 | p3 |
���ʵ�ƽ��ת������ | ��1(SO2) | ��2(SO3) | ��3(SO2) |
ƽ�ⳣ�� K | K1 | K2 | K3 |
A. ��1<��2��c2<2c1 B. K1>K3��p2>2p3
C. ��1< ��3����1(SO2) > ��3(SO2) D. c2>2c3����2(SO3) +��3(SO2)<1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��COCl2(g)![]() CO(g)��Cl2(g)����H��0������Ӧ�ﵽƽ��ʱ�����д�ʩ�������¡��ں���ͨ��ϡ�����塡������COŨ�ȡ��ܼ�ѹ���ݼӴ�������ѹͨ��ϡ�����壬�����COCl2ת���ʵ���(����)
CO(g)��Cl2(g)����H��0������Ӧ�ﵽƽ��ʱ�����д�ʩ�������¡��ں���ͨ��ϡ�����塡������COŨ�ȡ��ܼ�ѹ���ݼӴ�������ѹͨ��ϡ�����壬�����COCl2ת���ʵ���(����)
A. �٢ڢ� B. �٢ܢ� C. �ڢۢ� D. �ۢݢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com