
【题目】自然界中,金属元素大多以化合态存在,通过金属冶炼得到金属单质。
工业上生产Na、Ca、Mg都用电解其熔融的氯化物,但生产钾是用金属钠和熔化的KCl在一定的条件下反应制取:
KCl + Na![]() NaCl + K + Q (Q<0)
NaCl + K + Q (Q<0)
有关数据如下表:
熔点℃ | 沸点℃ | 密度 (g/cm3) | |
Na | 97.8 | 882.9 | 0.97 |
K | 63.7 | 774 | 0.86 |
NaCl | 801 | 1413 | 2.165 |
KCl | 770 | 1500 | 1.984 |
(1)请结合平衡移动理论分析,为什么能用该反应制备金属钾。
_______________________________________。
(2)在常压下金属钾转为气态从反应混合物中分离的最低温度约为_____℃,而反应的最高温度应低于_____℃。
(3)在制取金属钾的过程中,为了提高原料的转化率可采取的措施有__________。(任写两点)
(4)相比于电解熔融氯化钾,此方法的优点有_____________________。
(5)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为![]() ________。
________。
【答案】 钾蒸气逸出使生成物浓度减小,平衡向正反应方向移动,可不断得到金属钾。 774℃ 882.9℃ 升高温度、降低压强或移去钾蒸气 能耗低、无污染 c(K)/c(Na)
【解析】(1)工业上制取金属钾的化学原理是钾蒸气逸出使生成物浓度减小,平衡向正反应方向移动,可不断得到金属钾。故答案为:钾蒸气逸出使生成物浓度减小,平衡向正反应方向移动,可不断得到金属钾;
(2)在常压下金属钾转为气态从反应混合物中分离的最低温度约为774℃,而反应的最高温度应低于882.9℃,故答案为: 774℃;882.9℃;
(3)在制取金属钾的过程中,为了提高原料的转化率可采取的措施是适当的降低温度或移去钾蒸气,故答案为:当的降低温度或移去钾蒸气;
(4)相比于电解熔融氯化钾,此方法具有能耗低、无污染等优点,故答案为:能耗低、无污染;
(5)当反应温度升高到900℃时,只有Na、K为气体,K=![]() ,故答案为:K=
,故答案为:K=![]()


科目:高中化学 来源: 题型:
【题目】碳及其化合物广泛存在于自然界中,试回答下列问题:
(1)某处碳循环如图所示,CaCO3转化为HCO3-的离子方程式为_____________。

(2)常温常压下,空气中的CO2溶于水,达到平衡时,无机碳在浓液中以4种形式存在,其转化关系如下:
①CO2(g)+H2O![]() H2CO3 K=10-2.8
H2CO3 K=10-2.8
②H2CO3![]() H++HCO3- K1=10-3.5,
H++HCO3- K1=10-3.5,
③HCO3-![]() H++CO32- K2=10-10.3,
H++CO32- K2=10-10.3,
若溶液中。c(CO2)=1.0×10-5mol/L,且忽略水的电离及H2CO3的第二级电离,则溶液pH=_____。
(3)某化学小组为了测量湖水中无机碳的含量,量取 100mL湖水,酸化后用N2吹出CO2,再用NaOH溶液吸收,将吸收液用0.10mol/L盐酸滴定,生成的V(CO2)随V (盐酸)变化关系如图2所示,则吸收液中离子浓度由大到小的顺序为______________(不用写出H+),湖水中无机碳的浓度为_______mol/L。

(4)—定条件下,CO2和H2O可以转化为CO和H2,通过反应:CO(g)+2H2(g) ![]() CH3OH(g)制备甲醇,若起始时在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡时CO转化率a (CO)随T、P的变化关系如图3所示。
CH3OH(g)制备甲醇,若起始时在密闭容器中按物质的量之比1:2充入CO和H2,测得平衡时CO转化率a (CO)随T、P的变化关系如图3所示。

①P1__P2(填“大于”、“小于”或“等于”);
②该反应在195℃、P2条件下达到平衡后,c(H2)=0.5 mol/L ,则该反应的平衡常数为______。
③已知CH3OH和CO的燃烧热分别725.8kJ/mol、283.0 kJ/mol,1mol液态水变成气态水吸热44.0kJ,写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式:_________________。
(5)用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图4,则c电极的反应方程式为:_______________ 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于药物的说法不正确的是
A. OTC表示非处方药
B. 氢氧化铝是抗酸药的主要成分
C. 麻黄碱可用于治疗支气管哮喘
D. 青霉索是重要的抗生索,可以放心大量使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子在溶液中能大量共存的是( )
A.H+、AlO2﹣、CO32﹣
B.K+、Ba2+、SO42﹣
C.NH4+、OH﹣、NO3﹣
D.Fe3+、NO3﹣、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是生命物质的重要组成元素之一,含氮物质与人类的生活密切相关。
(1)氮原子最外层电子排布式为:_________;氮离子![]() 核外有___种运动状态不同的电子;N4分子的空间结构如图:
核外有___种运动状态不同的电子;N4分子的空间结构如图:![]() ,它是一种_____分子。(填“极性”或“非极性”)
,它是一种_____分子。(填“极性”或“非极性”)
(2)氨气是人工固氮的产物,它极易溶于水(![]() ),生成NH3 · H2O。请设计实验证明NH3 · H2O是弱碱_______________________________。
),生成NH3 · H2O。请设计实验证明NH3 · H2O是弱碱_______________________________。
(3)向100mL 0.1mol/L的盐酸中通入0.02mol氨气,充分吸收后测得溶液呈碱性。则该溶液中NH3 · H2O、![]() 、
、![]() 三种微粒的物质的量浓度大小关系为____________。
三种微粒的物质的量浓度大小关系为____________。
(4)铵盐可用作氮肥,实验室检验铵盐中的![]() 时,可取少量铵盐样品于试管中,加入强碱浓溶液,加热,若产生的气体能使________________________________,说明有
时,可取少量铵盐样品于试管中,加入强碱浓溶液,加热,若产生的气体能使________________________________,说明有![]() 。
。
(5)NaN3可用于制造汽车安全气囊,当汽车遇到撞击时,NaN3能迅速分解产生Na和N2。请写出该反应的化学方程式_______________________,每生成3mol N2时,转移电子_____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】菠萝酯(F)是一种具有菠萝香味的赋香剂,其合成路线如下:
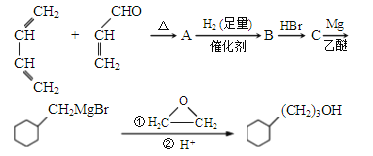


(1)A的结构简式为________,A中所含官能团的名称是_____。
(2)A→B反应类型是________; B→C反应,除HBr之外还需要的试剂和条件是________。
(3)E的某种同分异构体的一氯代物只有一种,该同分异构体的结构简式为________。
(4)1mol菠萝酯(F)与氢气反应,最多消耗氢气____mol。
(5)结合题干信息,以乙烯和环氧乙烷(![]() )为原料制备1丁醇,设计合成路线________(其它试剂任选)。
)为原料制备1丁醇,设计合成路线________(其它试剂任选)。
(合成路线常用表示方法为:A ![]() B ……
B ……![]() 目标产物)
目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近在-100℃的低温下合成了一种化合物X,此分子的模型如图所示,其中黑圆代表碳原子,白圆代表氢原子,下列说法中不正确的是( )

A. 该分子的分子式C5H4
B. 1mol该物质完全燃烧生成CO2与H2O时需耗6 mol O2
C. 该物质完全燃烧生成的CO2与H2O的分子数比为5:4
D. 1mol该物质完全燃烧生成CO2与H2O时转移电子数为24 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙是一种安全无毒的物质,可杀菌和供氧,用于鱼苗养殖。带有数量不等的结晶水,通常还含有部分氧化钙.
(1)称取0.542 g过氧化钙样品,灼热时发生如下反应:2(CaO2xH2O)![]() 2CaO+O2↑+2xH2O,得到的O2在标准状况下体积为67.2 mL.该样品中CaO2的物质的量为_______________.
2CaO+O2↑+2xH2O,得到的O2在标准状况下体积为67.2 mL.该样品中CaO2的物质的量为_______________.
(2)另取同一样品0.542 g,溶于适量的稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 0.70 g.
①试列式计算样品中CaO的质量_______________.
②试列式计算样品中CaO2xH2O的x值________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com